��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
p; c.Cu2S d.Al2O3
 ��2����ͭ��Cu2S���ɷ�����Ӧ2Cu2S+2H2SO4+5O2==4CuSO4+2 H2O���÷�Ӧ�Ļ�ԭ���� ����1mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ mol����CuSO4��Һ�м���þ��ʱ���������ɣ���������
��2����ͭ��Cu2S���ɷ�����Ӧ2Cu2S+2H2SO4+5O2==4CuSO4+2 H2O���÷�Ӧ�Ļ�ԭ���� ����1mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ mol����CuSO4��Һ�м���þ��ʱ���������ɣ���������
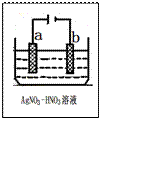
��3����ͼΪ��⾫������ʾ��ͼ�� ����a��b����Ϊ�������ʵĴ�������b������������ɫ�������ɣ������ɸ�����ĵ缫��ӦʽΪ
��4��Ϊ������������ĺڰߣ�Ag2S�������������������������ʳ��ˮ�в������Ӵ���Ag2Sת��ΪAg��ʳ��ˮ������Ϊ
29����15�֣���ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ��
��1�����á���ѧ����ת�Ʒ����Ʊ�TaS2���壬�������·�Ӧ
TaS2��s��+2I2��g�� TaI4��g��+S2��g�� ��H��0 ��I��
TaI4��g��+S2��g�� ��H��0 ��I��
��Ӧ��I����ƽ�ⳣ������ʽK= ����K=1����ij�����ܱ������м���1mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ
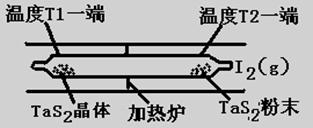 ��2����ͼ��ʾ����Ӧ��I����ʯӢ��չ��н��У������¶�ΪT2��һ�˷���δ�ᴿ��TaS2��ĩ������I2��g����һ��ʱ������¶�ΪT1��һ�˵õ��˴�����TaS2���壬���¶�T1 T2���������������=������������Ӧ��ϵ��ѭ��ʹ�õ������� ��
��2����ͼ��ʾ����Ӧ��I����ʯӢ��չ��н��У������¶�ΪT2��һ�˷���δ�ᴿ��TaS2��ĩ������I2��g����һ��ʱ������¶�ΪT1��һ�˵õ��˴�����TaS2���壬���¶�T1 T2���������������=������������Ӧ��ϵ��ѭ��ʹ�õ������� ��
��3������I2�������Կɲⶨ��������ĺ����������ǽ������е���ת��ΪH2SO3��Ȼ����һ��Ũ�ȵ�I2��Һ���еζ�������ָʾ��Ϊ ���ζ���Ӧ�����ӷ���ʽΪ
��4��25��ʱ��H2SO3  HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh= mol L-1������NaHSO3��Һ�м���������I2������Һ��
HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh= mol L-1������NaHSO3��Һ�м���������I2������Һ�� �� ���������С�����䡱����
�� ���������С�����䡱����
30����15�֣�TiO2�����Ʊ��������ѻ������ԭ�ϣ�����һ����������İ�ɫ���ϡ�
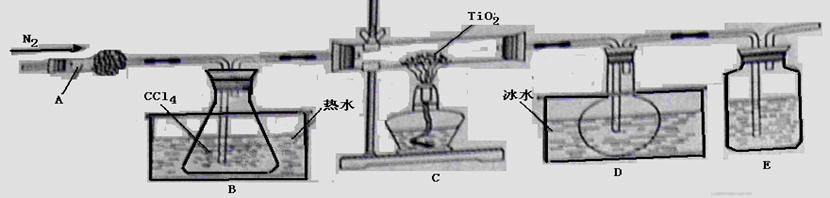
��1��ʵ�������÷�ӦTiO2��s��+2CCl4��g��==TiCl4��g��+CO2��g��������ˮ���������£���ȡTiCl4ʵ��װ��ʾ��ͼ����
�й��������±�
|
���� |
�۵�/�� |
�е�/�� |
���� |
|
CCl4 |
-23 |
76 |
��TiCl4���� |
|
TiCl4 |
-25 |
136 |
����ʪ������������ |
����A�������� ��װ��E�е��Լ��� ����Ӧ��ʼǰ���ν������²�������ֹͣͨ������Ϩ��ƾ�������ȴ�����¡���ȷ��˳��Ϊ ������ţ���������D�е�Һ̬���������ò����������� ��
��2����ҵ����������FeTiO3��(��Fe2O3��SiO2������)�Ʊ�TiO2���йط�Ӧ������
����FeTiO3��s��+2H2SO4��aq��==FeSO4��aq��+ TiOSO4��aq��+ 2H2O��l��
ˮ��TiOSO4��aq��+ 2H2O��l��== H2TiO3��s��+H2SO4��aq��
��Ҫ�����������£�
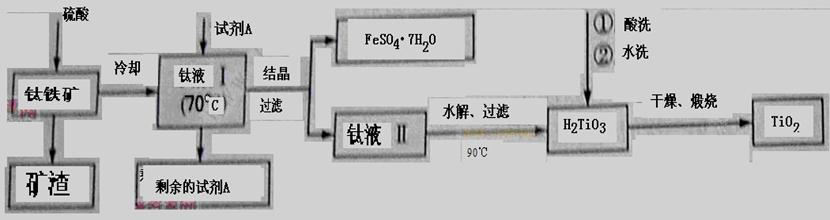
���Լ�AΪ ����Һ������ȴ��70�����ң����¶ȹ��ᵼ�²�Ʒ���ʽ��ͣ�ԭ����
��ȡ������ϴ���H2TiO3���������Ტ���μ�KSCN��Һ�������������ټ�H2O2�������ɫ��˵��H2TiO3�д��ڵ����������� ������H2TiO3��ʹ��ˮ���ϴ�ӣ����պ��õ�TiO2Ҳ�ᷢ�ƣ����Ƶ������� ���ѧʽ����
��ѡ������24�֡�
31��8�֣�����ѧ������ѧ�뼼����
�Ͼ�Ӳ�ʽ��к�̼���٣�WC���������ܣ�Co�������������������õ�ⷨ�ɻ���WC��Co���������̼�ͼ���£�
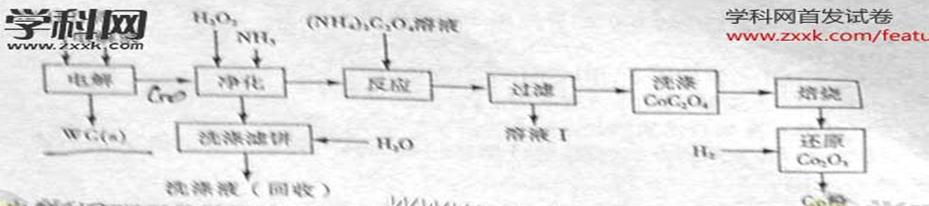
��1�����ʱ�Ͼɵ������������������������HCL��ҺΪ���Һ��������Ҫ�ĵ缫��ӦʽΪ ��
��2���������������˱�����Ҫ�ɷ��� �����յ�ϴ��Һ����ˮ���Ƶ��Һ��Ŀ���ǻ����������е� ��
��3����ҺI����Ҫ�ɷ��� ��ϴ��CoC2O4����ֶ����ղ�Ʒ���Ȳ�������Ӱ�죬������ʱ����ɻ�����Ⱦ��ԭ���� ��
��4����Co2O3��ԭ��Co�۵Ļ�ѧ��Ӧ����ʽΪ ��
32����8�֣�����ѧ�������ʽṹ�����ʡ�
±��Ԫ�ذ���F��CL��Br�ȡ�
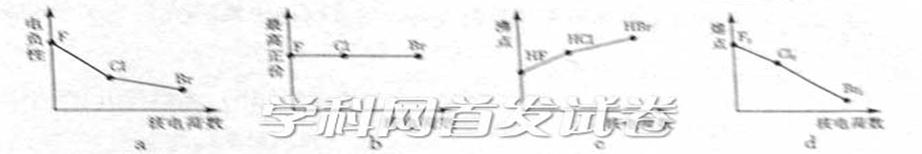
��1���������߱�ʾ±��Ԫ��ij��������˵�����ı仯���ƣ���ȷ���� ��
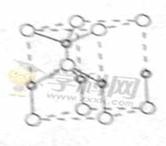 ��2�����á�±�����ɺϳɺ�B��N����Ԫ�صĹ����մɣ���ͼΪ�侧���ṹʾ��ͼ����ÿ�������к���Bԭ�ӵĸ���Ϊ ���ù����մɵĻ�ѧʽΪ ��
��2�����á�±�����ɺϳɺ�B��N����Ԫ�صĹ����մɣ���ͼΪ�侧���ṹʾ��ͼ����ÿ�������к���Bԭ�ӵĸ���Ϊ ���ù����մɵĻ�ѧʽΪ ��
��3��BCL3��NCL3����ԭ�ӵ��ӻ���ʽ�ֱ�Ϊ �� ����һ�����ܽ���B��N֮��ĵڶ�����Ԫ���� �֡�
��4����BCL3��XYn ͨ��Bԭ����Xԭ�Ӽ����λ������γ��������������ṩ�¶Ե��ӵ�ԭ���� ��
33����8�֣�����ѧ�����л���ѧ������
��������66������������������������ɡ������˿���֯�����������·�ߺϳɣ�

��1������������Һ��Ӧ��B��ͬ���칹��Ľṹ��ʽΪ
��2��D�Ľṹ��ʽΪ ���ٵķ�Ӧ����Ϊ
��3��Ϊ����D�еĹ����ţ������Լ�����NaOHˮ��Һ��
��4����F��G����H�ķ�Ӧ����ʽΪ