��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1��д�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽCu2++2OH-=Cu��OH��2����______
��2��д��H2SO4�ĵ��뷽��ʽ��______
��3����ȥ�����е����ʣ�д�������Լ�����Ӧ�Ļ�ѧ����ʽ��
NaCl��Na2SO4���������Լ���______����ѧ����ʽΪ______��
FeCl2��CuCl2���������Լ���______����ѧ����ʽΪ______��
�ο��𰸣���1���������ͭ����ǿ�Ӧ���ɿ������κ�������ͭ������Cu2++2OH-=Cu��OH��2����ʾ����CuCl2+2NaOH=Cu��OH��2��+2NaCl��
�ʴ�Ϊ��CuCl2+2NaOH=Cu��OH��2��+2NaCl��
��2����ǿ�������ȫ���룬��H2SO4�ĵ��뷽��ʽΪH2SO4�T2H++SO42-���ʴ�Ϊ��H2SO4�T2H++SO42-��
��3��NaCl�л���Na2SO4��ѡ��������BaCl2�������Ʒ�Ӧ��ȥ���ʣ�����Һ�з����ķ�ӦΪNa2SO4+BaCl2�TBaSO4��+2NaCl��Ȼ����ˡ������ɵô�����NaCl��
FeCl2�л���CuCl2��ѡ�������Fe�ۣ�����Һ�з���Fe+CuCl2�TFeCl2+Cu��Ȼ����ˣ���HCl�����������õ��������Ȼ�������
�ʴ�Ϊ��BaCl2��Na2SO4+BaCl2�TBaSO4��+2NaCl��Fe��Fe+CuCl2�TFeCl2+Cu��
���������
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д�������
[? ]
A��������ˮ��Ӧ��Cl2��H2O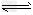 2H����Cl����ClO��
2H����Cl����ClO��
B����ˮ�μӵ�AgNO3��Һ�У�Cl����Ag��===AgCl��
C��̼��������ᷴӦ��CaCO3��2H��===Ca2����H2O��CO2��
D��������������Һ����������Cl2��2OH��===Cl����ClO����H2O
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��ȷ���ǣ�?��
A������ʯ��ˮ��ͨ������������̼��Ca(OH)2+ CO 2�� CaCO3�� + H2O
B��ͭ��FeCl3��Һ��Ӧ�� Cu + Fe3+�� Cu2+ + Fe2+
C��������Һ������������Һ��Ӧ�� SO42�� + Ba2+ �� BaSO4��
D������ͨ��FeCl2��Һ�� Cl2+ 2Fe2+�� 2Fe3++ 2Cl-
�ο��𰸣�D
���������A ������ʯ��ˮӦд��������ʽ
B ����ɲ��غ�Cu + 2Fe3+�� Cu2+ + 2Fe2+
C ����2H����SO42����Ba2����2OH��=BaSO4����2H2O
D ��ȷ��
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д��ȷ����(? )
A����������Һ�м������������������Һ��Al3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O
B����ʳ�׳�ȥˮƿ�е�ˮ����CO32-��2CH3COOH=2CH3COO��+CO2����H2O
C���������������м���������ϡ���Fe(OH)2+2H+=Fe2++2H2O
D�������������Һ��ͨ��������������2ClO-+ SO2 + H2O = SO32- + 2HclO
�ο��𰸣�A
���������ˮ����Ҫ�ɷ���̼��ƣ���������ɲ�B�����������ǿ�����ԣ������ᱻ��������������C�������������ǿ�����ԣ���������ᱻ�������������D���� ��ѡA��
���������ӷ���ʽ����д���ж�Ҫ���ܹ��������գ��ر�Ҫע��ǿ�����Ե����ӡ����ӷ���ʽ�����ж�Ҫע�⣺��ԭ���Ƿ���Ͽ���ʵ�����Ƿ���������غ㡢���Ƿ���ϵ���غ㡢���Ƿ���ϵ�ʧ������ȡ����ܵ���������ʲ�����ӡ�ע������������������ȡ�
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ��д��ȷ����
A������ˮ�⣺S2����2H2O  H2S����2OH��
H2S����2OH��
B��̼�������ڴ�����Һ�У�CO32���� 2 H���� H2O �� CO2��
C�����������Һ��ͨ�����������̼��Ca2+ + 2ClO��+H2O+CO2��CaCO3��+2HClO
D����������������������������Һ��Ӧ��Ba2����2OH����2H����SO42����BaSO4����2H2O
�ο��𰸣�D
���������
��ȷ�𰸣�D
A������ȷ�����Ʒֲ�ˮ�⣺S2����H2O  ?HS�D��OH��
?HS�D��OH��
B������ȷ��̼�������ڴ�����Һ�У�CO32���� 2 CH3COOH��2H2O �� CO2����2CH3COO�D
C������ȷ�����������Һ��ͨ�����������̼�� ClO��+H2O+CO2��HCO3�D +HClO
D.��ȷ��
�����Ѷȣ�һ��