微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业制CuSO4时,不是直接用铜跟浓硫酸在加热条件下反应,而是将铜丝浸入稀硫酸中,再不断由容器下部吹入细小的空气泡。这样做的好处是?。
参考答案:①减少了硫酸的用量,提高了硫酸的利用率。②不会产生对大气有污染的SO2。
本题解析:铜与浓硫酸的反应为:Cu+2H2SO4(浓)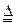 CuSO4+SO2↑+2H2O。分析反应方程式可知:由于浓H2SO4有1/2表现氧化性,1/2表现酸性,导致浓H2SO4的利用率只有50%。又由于生成的二氧化硫是有毒气体,也是引起酸雨的主要成分,所以工业上一般不采用此法。本题所给方法的反应方程式为:2Cu+2H2SO4+O2
CuSO4+SO2↑+2H2O。分析反应方程式可知:由于浓H2SO4有1/2表现氧化性,1/2表现酸性,导致浓H2SO4的利用率只有50%。又由于生成的二氧化硫是有毒气体,也是引起酸雨的主要成分,所以工业上一般不采用此法。本题所给方法的反应方程式为:2Cu+2H2SO4+O2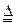 2CuSO4+2H2O。可知:硫酸仅表现酸性。对比以上两种方法,不难看出,这样做的好处主要有两条:①减少了硫酸的用量,提高了硫酸的利用率②不会产生对大气有污染的二氧化硫。
2CuSO4+2H2O。可知:硫酸仅表现酸性。对比以上两种方法,不难看出,这样做的好处主要有两条:①减少了硫酸的用量,提高了硫酸的利用率②不会产生对大气有污染的二氧化硫。
本题难度:简单
2、选择题 足量的下列物质分别与同体积同浓度的稀硫酸反应后,所得溶液的质量分数最小的是……( )
A.Zn
B.ZnO
C.Zn(OH)2
D.ZnCO3
参考答案:C
本题解析:Zn+H2SO4=ZnSO4+H2↑
ZnO+H2SO4=ZnSO4+H2O
Zn(OH)2+H2SO4=ZnSO4+2H2O
ZnCO3+H2SO4=ZnSO4+CO2↑+H2O
比较上述反应可知Zn(OH)2与H2SO4反应得溶液的质量分数最小。
本题难度:简单
3、选择题 下列叙述或操作正确的是(?)
A.浓硫酸具有强氧化性,稀硫酸无氧化性。
B.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌。
C.浓硫酸不慎沾到皮肤上,应立即用布拭去,再用水冲洗。
D.浓硫酸与铜的反应中,浓硫酸只表现强氧化性。
参考答案:C
本题解析:略
本题难度:简单
4、实验题 (18分)甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性己检验)。

实验操作和现象:

(1)A中反应的化学方程式是?。
(2)C中白色沉淀是?,该沉淀的生成表明SO2,具有?性。
(3)C中液面上方生成浅棕色气体的化学方程式是?。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲同学认为是空气参与反应,乙同学认为
是白雾参与反应。
①为证实各自的观点,在原实验基础上/甲同学在原有操作之前增加一步操作,该操作是
?;乙同学在A、B间增加洗气瓶D,D
中盛放的试剂是?。
②甲、乙两同学分别改进实验后,B装置中现象分别为:
检验白色沉淀,发现均不溶于稀盐酸。请用离子方程式解释甲、乙两同学改进实验后仍然产生沉淀的原因,甲:?,乙:?。
(5)合并(4)中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是?。
参考答案:

本题解析:略
本题难度:困难
5、选择题 打雷放电时,空气中有极少量的氧气转化为臭氧(3O2放电2O3),下列说法正确的是(? )
A.此变化属于物理变化
B.O2和O3是同位素
C.O2和O3是不同物质
D.O2和O3的性质完全相同
参考答案:C
本题解析:因为O2和O3的分子组成不同,性质不同,因此是两种不同的物质,互为同素异形体,其相互转化为化学变化。
本题难度:简单