|
高考化学试题《物质的量》高频试题预测(2017年最新版)(二)
2017-08-10 00:15:03
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某盐的混合物中含有0.2mol Na+、0.4mol Mg2+、0.4mol Cl-,则SO42-为( )
A.0.1mol
B.0.3mol
C.0.5mol
D.0.15mol
|
参考答案:B
本题解析:根据电荷守恒n(Na+)+2n(Mg2+)=n(Cl-)+2n(SO42-),求得n(SO42-)=0.3mol。答案选B。
考点:电荷守恒
点评:本题基础简单。
本题难度:一般
2、填空题 (1)18gH2O的物质的量是 ,含有 个氢原子(填具体数字);这些H2O与 gOH-所含电子数相等。
(2)标准状况下,①6.72L CH4 ②3.01×1023HCl分子 ③0.2molNH3 ,这三种气体按物质的量由大到 小排列的顺序是(填物质的数字代号,下同) ,按氢原子数由多到少排列的顺序是 ,密度由大到小排列的顺序是 。
参考答案:(1)1mol(1分); 1.204×1024(1分); 17(1分);
(2)?(1分); ?(1分); ?(1分);
本题解析:
(1)18gH2O的物质的量n="m" /M =18g/18g/mol=1mol;1molH2O含有2mol氢原子,即2×NA=1.204×1024个;1molH2O含有10mol电子,含有10mol电子的OH-的物质的量为1mol,1molOH-的质量为17g。
(2):①n(CH4)=6.72L/22.4L/mol=0.3mol,m(CH4)=0.3mol×16g/mol=4.8g,N(H)=4×0.3mol×NA/mol=1.2NA,ρ="M/" Vm ="16/" 22.4g/L;
②n(HCl)="N" /NA =3.01×1023 /6.02×1023/mol=0.5mol,m(HCl)=0.5mol×36.5g/mol=18.25g,N(H)=N(HCl)=0.5NA,ρ="M/" Vm =36.5/22.4g/L;
③m(NH3)=0.2mol×17g/mol=3.4g,N(H)=3×0.2mol×NA/mol=0.6NA,ρ="M" /Vm ="17/" 22.4g/L;
所以:三种气体按质量由大到小排列的顺序是②>①>③;氢原子数由多到少排列的顺序是①>③>②密度由大到小排列的顺序是②>③>①,
考点:阿伏加德罗定律及推论
本题难度:一般
3、选择题 化学家从腐败草料中提取出双香豆素,结构简式如右下图。1mol双香豆素与NaOH溶液反应,最多可消耗NaOH的物质的量是?(?)

A.2mol
B.4mol
C.6mol
D.8mol
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列溶液中含Cl-浓度最小的是?
A 、10ml? 0.1mol/L AlCl3的溶液? B 、 20ml ?0.2mol/LCaCl2的溶液
C 、 30ml ?0.2mol/LKCl的溶液? D 、 100ml? 0.25mol/LNaCl的溶液
参考答案:C
本题解析:A项中Cl-浓度为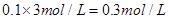
B项中Cl-浓度为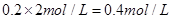
C项中Cl-浓度为0.2mol/L
D项中Cl-浓度为0.25mol/L,故溶液中含Cl-浓度最小的是C。
点评:考查C溶液离子浓度的计算,难度不大,解题时需特别注意不同物质的化学式中所带的离子个数,否则容易计算错误。
本题难度:简单
5、填空题 (1)氢气、甲烷(CH4)、水各1g,其中含分子数最多的是 ;含氢原子最多的是 ;
氢气、甲烷、水各1mol,含分子数是否一样多? (填“是”或“否”)
含氢原子数最多的是 。
(2)6.02×1024个Na+约含 mol Na+,其质量为 g;49gH2SO4约含
有 个H,共含有 mol原子。
参考答案:(8分,每空1分)(1)H2、H2;是、CH4
(2)10、230; 6.02×1023、3.5
本题解析:(1)等质量的物质分子数较多的也即物质的量较大的,所以摩尔质量最小的物质的物质的量大,所以氢气、甲烷(CH4)、水各1g时分子数最多的是H2;氢气、甲烷(CH4)、水各1g时各物质的物质的量是1/2mol、1/16mol、1/18mol,则所含H原子的物质的量分别是1mol、0.25mol、1/9mol,所以H原子数最多的还是H2;当三者的物质的量相同时,所含的分子数一样多;物质的量相同时,分子数相同,而1个甲烷分子中含有4个H原子,所以所含的H原子最多的是CH4;
(2)6.02×1024个Na+约含6.02×1024/6.02×1023mol-1="10mol" Na+,其质量是10mol×23g/mol=230g;49gH2SO4的物质的量是49g/98g/mol=0.5mol,1个硫酸分子中含有2个H原子,所以约含有0.5mol×2×6.02×1023mol-1=6.02×1023个H原子,1个硫酸分子中含有7个原子,所以含有的原子总物质的量是0.5mol×7=3.5mol.
考点:考查物质的量的有关计算
本题难度:一般
|