��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ö��Ե缫���NaCl��NaHCO3�Ļ����Һ�������Һ��pH�仯��ͼ��ʾ��
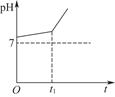
��1����0��t1ʱ���ڣ������缫�ϵĵ缫��ӦʽΪ��
������________________________________________________________________________��
������________________________________________________________________________��
��2�������ӷ���ʽ��ʾ0��t1ʱ���ڣ���ҺpH���߱Ƚϻ�����ԭ��____________________________________________________________________________��
�ο��𰸣���1��2Cl����2e��=Cl2����2H����2e��=H2��
��2��HCO3-��OH��=CO32-��H2O
�������������HCO3-��Na�������ŵ磬��������ӦʽΪ2Cl����2e��=Cl2����������ӦʽΪ2H����2e��=H2�������ŷ�Ӧ�Ľ���c��OH��������HCO3-��OH��=CO32-��H2O���ʶ���ʼpH�仯��������HCO3-��ȫ��Ӧ��pH�����Ӵ�
�����Ѷȣ�һ��
2������� ��Pt�缫���500mL��KNO3��NaCl�����Һһ��ʱ�䣬�����������ɱ�״���µ�����11.2L�����ǰ����Һ������䣬д������������Ӧʽ����������Һ��NaOH�����ʵ���Ũ�ȣ�
�ο��𰸣���Pt�缫���500mL��KNO3��NaCl�����Һʱ�������������ӷŵ������������������������ӷŵ����������������������ӷŵ���������������11.2L�����õ����ӵ����ʵ���=11.2L22.4L/mol��2=1mol������11.2L����ʧȥ���ӵ����ʵ����T11.2L22.4L/mol��2=1mol������11.2L����ʧȥ���ӵ����ʵ����T11.2L22.4L/mol��2=2mol��Ҫʹ�����缫������ͬ��������壬��ת�Ƶ�����ȣ���������ֻ��ֻ������������������������
���������ϵ缫��ӦʽΪ��2H++2e-=H2���������ϵ缫��ӦʽΪ��2Cl--2e-=Cl2����
�����൱�ڵ���Ȼ�����Һ������2NaCl+2H2O?���?.?2NaOH+H2��+Cl2��֪�������������Ƶ����ʵ���Ũ��=11.2L22.4L/mol��20.5L=2 mol/L��
������������Ӧʽ����������Һ��NaOH�����ʵ���Ũ�ȷֱ�Ϊ2H++2e-=H2����2Cl--2e-=Cl2����2mol/L��
���������
�����Ѷȣ�һ��
3��ѡ���� �ҹ������ؾ������Ƚ�ˮƽ���Ҿ�DZͧ��װ�����������������ء����������ص�ij��������Ͻ�LaNi5H6��LaNi5H6�и�Ԫ�صĻ��ϼ۾���Ϊ0�ۣ�����ط�ӦΪ
LaNi5H6 +6NiO(OH) 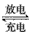 LaNi5+ 6Ni(OH)2������˵����ȷ����
LaNi5+ 6Ni(OH)2������˵����ȷ����
[? ]
A���ŵ�ʱ����Ͻ�������
B���ŵ�ʱ������ӦΪLaNi5H6 - 6e - ==LaNi5+6H+
C�����ʱ������Χc(OH -)��С
D�����ʱ����Ͻ�������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ��25��ʱ���ò��缫���һ������Na2SO4������Һ��һ��ʱ�����������amol���壬ͬʱ��Һ������bg Na2SO4��10H2O���������һ�������¶Ȳ��䣬���ʱNa2SO4��Һ�����ʵ���������Ϊ��?��
A����71/161����100�G
B����71b/161(18a+b)����100�G
C����b/(18a+b)����100�G
D����71b/161(36a+b)����100�G
�ο��𰸣�B
�����������
�����Ѷȣ���
5������� �ס��ҡ����������졢��Ϊԭ��������������Ķ���������Ԫ�ء��ס�������ͬһ���壬���������촦��ͬһ���ڣ���Ԫ������ϼ�����ͼ۵Ĵ�����Ϊ0�����������������������ˮ����֮�䶼�ܷ�����Ӧ���û�ѧ����ش��������⣺
��1���������ӵĽṹʾ��ͼΪ ���õ���ʽ��ʾ�������γɻ�����Ĺ��� ��
��2����������������Ӱ뾶�ɴ�С��˳��Ϊ ���ҡ��졢�����⻯��Ļ�ԭ���������� ��
��3��д���ɼ�����Ԫ���γɵĻ������У��Ⱥ��м��Լ��ֺ��зǼ��Լ�������Է���������С�����ʵĽṹʽ ������������������������¿ɹ���ȼ�ϵ�أ��õ�طŵ�ʱ�������ķ�ӦʽΪ ��
��4��������������������ˮ����֮�䷢����Ӧ�����ӷ���ʽΪ ���ɼס������졢���в���Ԫ���γɵ����ֻ������ˮ��Һ֮����Է�����Ӧ���û�ѧ����ʽΪ�� ��
��5������ͼ�����ͼ��γɻ�����ı�����Һ����װ�ÿ����ڼ�ͥ��ˮ��������д���õ����з�����Ӧ���ܷ�Ӧ����ʽ�� ��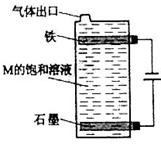
�ο��𰸣���1�� 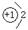 ��1�֣�
��1�֣� 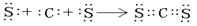 ��2�֣�
��2�֣�
��2��S2-��Na+��Al3+ ��2�֣� HCl��2�֣�
��3��H-C��C-H ��1�֣� C2H2 + 4H2O ? 10e���� 2CO2+10H+��2�֣�
��4��Al(OH)3��OH�� ��AlO2�� ��2H2O ��2�֣��� NaHS+HCl�� NaCl+H2S �� Na2S + H 2S ��2 NaHS��2�֣�
��5��NaCl��H2O NaClO��H2�� ��2�֣�
NaClO��H2�� ��2�֣�
������������ݱ��������촦��ͬһ���ڣ��ұ��������������������ˮ����֮�䶼�ܷ�����Ӧ����֪��ΪAl��������Ԫ�ش��ڵ������ڣ����������ܹ���ǿ���ǿ�ᷴӦ��������⣬ԭ��������������Ķ���������Ԫ�أ��Ƴ���ΪNa����ΪS����ΪCl��������Ԫ������ϼ�����ͼ۵Ĵ�����Ϊ0����ΪCԪ�أ��ס�������ͬһ���壬��ΪHԪ�ء���1������������������2�����ӣ�̼����֮���Թ��ۼ��γ�CS2����2�����ݵ��Ӳ���Խ��뾶Խ���Ӳ��Ų���ͬ�����ӣ����Ӱ뾶��С��˵������С�ɷ��ȣ���S2-��Na+��Al3+ ���⻯��Ļ�ԭ����ǽ����Գɷ��������ǽ�����Խǿ�����⻯��Ļ�ԭ��Խ�����仹ԭ��˳��H2S��CH4��HCl����3���ס�����Ԫ���γɵĻ������������࣬���м��Լ��ֺ��зǼ��Լ�������Է���������С�����ʣ���2��̼����H�������٣��ۺ��ж�Ϊ��Ȳ���ṹ��ʽΪ��H-C��C-H ����Ȳȼ�ϵ�أ���������Ȳʧȥ���ӷ���������Ӧ�����������µ缫��ӦʽΪ�� C2H2 + 4H2O ? 10e���� 2CO2+10H+����4����������������������Ӧ���ӷ���ʽΪAl(OH)3��OH�� ��AlO2�� ��2H2O ��H��Na��S��Cl�γɵĻ����Ӧ�������H2S��NaHS��Na2S�����Ȼ��HCl��NaCl���������ܷ�����Ӧ����NaHS+HCl�� NaCl+H2S��Na2S + H 2S ��2 NaHS����5����ⱥ���Ȼ�����Һ��������װ�õ��²���������Ӧ���ɵ�������������Ĺ������������������������Ʒ�Ӧ���ɴ������ƣ����������ã��ܵ�ⷴӦΪNaCl��H2O NaClO��H2����
NaClO��H2����
���㣺Ԫ�������ɡ����ӷ���ʽ��д�����ط�Ӧԭ��֪ʶ��
�����Ѷȣ�����