微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列过程中发生化学变化的是
A.用四氯化碳萃取溴水中的溴
B.用蒸馏的方法制取蒸馏水
C.用过滤的方法除食盐水中的泥沙
D.用加热的方法除碳酸钠中碳酸氢钠
参考答案:D
本题解析:考查物质的分离
ABC均为物理分离方法,而用加热的方法除碳酸钠中碳酸氢钠是通过化学方法:2NaHCO3=Na2CO3+H2O+CO2↑,不但除去碳酸氢钠,还生成了碳酸钠,答案为D
本题难度:一般
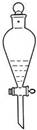
2、选择题 下列实验能达到目的的是
| 
| 
| 
|
用酒精萃取溴水中的溴
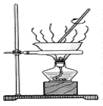
| 将硫酸铜溶液直接蒸干得到胆矾
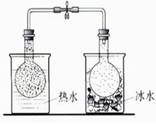
| 说明2NO2(g)  N2O4(g)?△H<0 N2O4(g)?△H<0
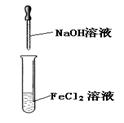
| 实验室制备Fe(OH)2
|
A
| B
| C
| D
|
?
参考答案:C
本题解析:A、酒精与水互溶,不能萃取溴水中的溴,错误;B、胆矾是硫酸铜的结晶水合物,将硫酸铜溶液蒸干得不到胆矾,错误;C、热水中的烧瓶的颜色深,说明温度升高平衡逆向移动,所以正向是放热反应,正确;D、氢氧化亚铁不稳定,极易被氧气氧化,所以如图上操作得不到氢氧化亚铁,错误,答案选C。
本题难度:一般
3、简答题 下图为某套实验装置示意图,其中加热装置和部分药品等均已经省略(装置①和装置②为气体发生装置)。
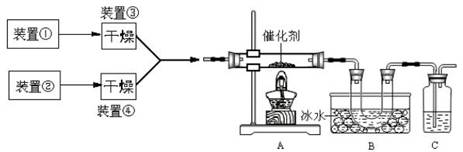
(1)甲同学用此装置(在A、B间增加一盛有浓硫酸的洗气瓶)制备NO2并验
证其性质。装置①用于实验室制备NH3,用装置②制备过量O2。装置①中发生
反应的化学方程式是?。B处冰水冷却的U型管中有红棕色气
体生成且越接近U型管底部颜色越浅,请解释原因?。
(2)乙同学用此套装置合成SO3,B处冰水冷却的U型管中有固体出现。C中
若盛放酸性K2Cr2O7溶液,则在C中发生的氧化还原反应的离子方程式是?(生成物中Cr以Cr3+形式存在);现欲制得纯净干燥的SO3,若C中盛放NaOH溶液,则此装置中存在明显不足,应如何改进?(从下面给出的实验装置中选择字母标号补充或替换,并用简要文字说明补充和替换的位置)。
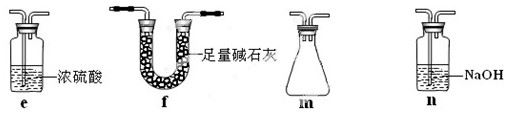
(3)丙同学拟验证NO能被氨气还原并测算其转化率(装置①、装置②分别制
NO和NH3),将上述装置A、B、C分别换成下列⑤、⑥、⑦。

请回答:装置⑦的作用可能是?;若进入装置⑤的NO共22.4L(已折算为标准状况,下同),氨气过量,最后收集到标准状况下11.2LN2,则NO的转化率是?。
参考答案:(1)实验室制取氨气的反应是,2NH4Cl+Ca(OH)2 CaCl2+NH3+2H2O 因为氨气催化氧化生成NO,2NO+O2=2NO2,2NO2(红棕)
CaCl2+NH3+2H2O 因为氨气催化氧化生成NO,2NO+O2=2NO2,2NO2(红棕) N2O4(无色),正反应是放热,U型管底部的温度降低,上述平衡向右移动,NO2的浓度降低,颜色变浅。
N2O4(无色),正反应是放热,U型管底部的温度降低,上述平衡向右移动,NO2的浓度降低,颜色变浅。
(2)Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O
将e、m依次连接在B、C之间或将C装置换成f
(3)吸收未反应的NO? 60%
本题解析:(1))实验室制取氨气的反应是,2NH4Cl+Ca(OH)2 CaCl2+NH3+2H2O 因为氨气催化氧化生成NO,2NO+O2=2NO2,2NO2(红棕)
CaCl2+NH3+2H2O 因为氨气催化氧化生成NO,2NO+O2=2NO2,2NO2(红棕) N2O4(无色),正反应是放热,U型管底部的温度降低,上述平衡向右移动,NO2的浓度降低,颜色变浅。
N2O4(无色),正反应是放热,U型管底部的温度降低,上述平衡向右移动,NO2的浓度降低,颜色变浅。
(2)酸性K2Cr2O7溶液氧化未反应的二氧化硫,
Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O,此装置中存在明显不足是易发生倒吸且空气的水蒸气进入B中,得不到纯净干燥的三氧化硫,需在B、C之间依次加装置e、m,e装置防止空气的水蒸气进入B,m是安全瓶的起防止倒吸,或将C装置换成f装置,既可以吸收二氧化硫,还可防倒吸现象,防止水蒸气进入B中。
(3)装置⑥的作用是吸收未反应的的氨气,则⑦的作用是吸收未反应的NO;根据反应方程式有6NO―5N2,生成标准状况下11.2LN2,消耗NO的物质的量为0.6mol,原有NO的物质的量是22.4L/22.4L/mol=1mol,则NO转化率是60%。
本题难度:一般
4、填空题 为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A?,B?,C?。
(2)加过量A的原因是?
有关反应的化学方程式为:??
(3)加过量B的原因是:? ??
??
有关反应的化学方程式为:??
参考答案:(1)写出三种试剂的化学式:A :Ba(OH)2,? B :K2CO3,? C :HCl?。
(2)加过量A的原因是:为了除尽Mg2+和SO42-?,
有关反应的化学方程式为:MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓?
MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓?
(3)加过量B的原因是:为了除尽过量的Ba2+?,
有关反应的化学方程式为:Ba(OH)2+K2CO3=BaCO3↓+2KOH
本题解析:略
本题难度:简单
5、选择题 下列五组物质分离所涉及的实例、性质差异和分离方法的组合正确的是( )
| 实例 | 物质性质差异 | 分离方法
①除去氯化钠溶液中的泥沙
a在水中溶解度的差异
甲 蒸馏
②用四氯化碳提取溴水中的溴单质
b在不同溶剂中溶解度的差异
乙 萃取
③分离乙酸(沸点118°C)与乙酸乙酯(沸点77.1°C)
c沸点的差异
丙 分液
④分离汽油和水
d互不相溶
丁 过滤
⑤从含少量氯化钠的硝酸钾溶液中提取硝酸钾
e溶解度随温度变化的差异
戊 结晶
|
A.①a和③c丙
B.②b乙和⑤e戊
C.④d丁和⑤e戊
D.①a和④d丁
参考答案:A、氯化钠溶液中的泥沙是不溶于水的固体,实现固体和溶液的分离采用过滤的方法,即①a丁,乙酸(沸点118°C)与乙酸乙酯(沸点77.1°C)是互溶但是沸点不同的液体,可以采用蒸馏法分离,即③c甲,故A错误;
B、溴在四氯化碳中的溶解度大于在水中的溶解度,且水和四氯化碳互不相容,可以采用萃取法来分离,即②b乙,氯化钠的溶解度随温度升高变化不大,但是硝酸钾的溶解度随温度升高而增大,随温度降低而减小,可以采用结晶法来分离二者,即⑤e戊,故B正确;
C、汽油和水是互不相溶的液体,可以采用分液的方法来分离,即④d丙,氯化钠的溶解度随温度升高变化不大,但是硝酸钾的溶解度随温度升高而增大,随温度降低而减小,可以采用结晶法来分离二者,即⑤e戊,故C错误;
D、氯化钠溶液中的泥沙是不溶于水的固体,实现固体和溶液的分离采用过滤的方法,即①a丁,汽油和水是互不相溶的液体,可以采用分液的方法来分离,即④d丙,故D错误.
故选B.
本题解析:
本题难度:一般