��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ����
A��ԭ��ط�Ӧ���Է���������ԭ��Ӧ�����ŵ�������ƽ����������ɣ� �γɱպϻ�·
B��Ϊ��ֹ�ִ�������ʴ���������ִ���Ǻ��Ͻ���п��������������������������
C������ͭʱ����ͭ����������ͭ��������CuSO4�ǵ������Һ�����ǰ����ҺŨ�Ȳ���
D�����������ĵ�⣬���ǰ���������ٵ��������������ӵ��������
�ο��𰸣�A
���������B��Ϊ��ֹ�ִ�������ʴ���������ִ���Ǻ��Ͻ���п��п���ã���������������������������B����C������ͭʱ����ͭ����������ͭ��������CuSO4�ǵ������Һ�����ǰ��CuSO4��ҺŨ�ȼ�С����ͭ�ŵ�ʱ������ͭ���õĽ������ȷŵ磬����Һ�е�ͭ���ӷŵ磬���Ե��ǰ����ҺŨ�ȼ�С��D�����������ĵ�⣬���������ϱ����ŵ磬���Ե��ǰ���������ٵ��������������ӵ�������ȣ�D������ѡAS��
�������������յ������֪ʶ�������ǵ��غ͵�Ƴأ��������Һ�ı仯����ǰ�߱�С������������
�����Ѷȣ���
2��ѡ���� �ò��缫���100mL?HNO3��?AgNO3?�Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24L���壨��״��������ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ��������
A��1mol?L-1
B��2?mol?L-1
C��2.5?mol?L-1
D��3?mol?L-1
�ο��𰸣����缫Ϊ���Ե缫�����HNO3��AgNO3?�Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24L���壨��״������
n�����壩=2.24L22.4L/mol=0.1mol��
����������4OH--4e-=2H2O+O2����֪������0.1molO2ת��0.4mol���ӣ�
���ݵ����غ��֪������ת��0.4mol���ӣ���
2H++2e-=H2��
?0.2mol 0.1mol
? 2Ag++2e-=2Ag
0.2mol 0.2mol
��n��Ag+��=0.2mol��
��ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ0.2mol0.1L=2mol/L��
��ѡB��
���������
�����Ѷȣ�һ��
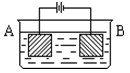
3�������� ��ͼ��װ�ý��е��ʵ�飺A����ͭп�Ͻ�B��Ϊ��ͭ��������к���������ͭ���ӡ�ͨ��һ��ʱ�����A��ǡ��ȫ���ܽ⣬��ʱB����������7.68g����Һ��������0.03g����A�Ͻ���Cu��Znԭ�Ӹ�����Ϊ
A��3�U1
B��4�U1
C��2�U1
D�������
�ο��𰸣�A
���������B����������7.68g����Һ��������0.03g�����ԺϽ��������7.71g����Ӧ��ת�Ƶ���Ϊ ����Ͻ���Cu��Zn�����ʵ����ֱ�Ϊx��y����64x��65y��7.71��2x��2y��0.24�����x��0.09mol��y��0.03mol������Cu��Znԭ�Ӹ�����Ϊ3�U1��
����Ͻ���Cu��Zn�����ʵ����ֱ�Ϊx��y����64x��65y��7.71��2x��2y��0.24�����x��0.09mol��y��0.03mol������Cu��Znԭ�Ӹ�����Ϊ3�U1��
�����Ѷȣ���
4��ѡ���� ��һ���¶��£��ò��缫��ⱥ��Na2SO4��Һ���Ե������Һ�ж���ȷ����
A�������������
B��Ũ�ȱ��
C��Ũ�ȱ�С
D��pH����
�ο��𰸣�D
������������Na2SO4��Һ��ʵ���ǵ��ˮ����ˮ�����٣�����Na2SO4��ҺҪ�������壬�������DZ�����Һ������Ũ�Ȳ��䡣
�����Ѷȣ���
5��ѡ���� �ö��Ե缫���100mLCuSO4��Һһ��ʱ�����ͨ������0.1molCu(OH)2����Һ������Ũ����ȫ��ԭ������ʱ��·��ͨ���ĵ���Ϊ (? )?
A��0.1mol
B��0.2mol
C��0.4mol
D��0.8mol 1
�ο��𰸣�C
�����������������֪��ͨ������0.1molCu(OH)2����Һ������Ũ����ȫ��ԭ����֪���ʱCu2+�ŵ���ȫ���ҵ����һ����ˮ����0.1molCu(OH)2��֪�����ʱ����������0.1molCu��0.1molH2����ϵ缫��Ӧʽ֪��ͨ���ĵ���Ϊ0.4mol��ѡC��
�����Ѷȣ�һ��