|
高考化学试题《燃烧热》考点强化练习(2017年押题版)(二)
2017-08-10 00:50:37
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (6分)(1)某学生进行中和热测定,取用50 mL 0.50 mol・L-1的HCl和50 mL 0.55 mol・L-1的NaOH溶液(密度都是1 g・cm-3)。实验后得到以下数据:
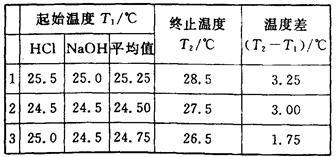
(中和后生成的溶液的比热容为4.18J・g-1・℃-1)请替该同学计算出中和热的平均值: .
(2)该学生测得的数据比理论值 (填“高”或“低”).
(3)从下列分析中选出该学生产生实验误差的原因可能是(填写字母) .
A.溶液混合后未及时盖好量热计杯盖
B.倾倒溶液太快,有少量溅出烧杯
C.溶液混合后搅拌不够
D.未等温度升到最高值就记录温度计示数
| E.用量筒量取盐酸体积时仰视读数
F.烧杯和玻璃棒吸收了一部分热量
参考答案:(1)52.25kJ・mol-1?(2)低? (3)ABCDF
本题解析:(1)根据实验数据可知,实验3中数据是无效的,所以温度差的平均值是3.125℃,所以根据△H=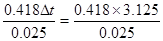 =52.25kJ・mol-1。 =52.25kJ・mol-1。
(2)中和热是57.3kJ・mol-1,所以实验值比理论值低。
(3)数值偏低,说明反应中有热量损失,或者是酸、碱有损失。E中读数偏大,结果应该是是偏高,所以正确的答案选ABCDF。
本题难度:一般
2、选择题 能使电离平衡H2O H++OH-向右移动,且使溶液呈酸性的是( ) H++OH-向右移动,且使溶液呈酸性的是( )
A.向水中加入少量硫酸氢钠固体
B.向水中加入少量硫酸铝固体
C.向水中加入少量碳酸钠固体
D.将水加热到100℃,使水的pH=6
参考答案:B
本题解析:硫酸氢钠能电离出氢离子,抑制水的电离,A不正确。硫酸铝溶于水铝离子水解,促进水的电离,溶液显酸性,B正确;碳酸钠是强碱弱酸盐,CO32-水解,溶液显碱性,C不正确;加热促进水的电离,但纯水仍然是显中性的,D不正确,答案选B。
点评:该题是基础性试题的考查,主要是考查学生对水的电离平衡的掌握情况,以及外界条件对水的电离平衡的影响程度,有利于培养学生的逻辑推理能力,提升学生的学科素养。
本题难度:一般
3、选择题 25℃时,某溶液中由水电离产生的C(H+)和C(OH-)的乘积为1×10-20,下列说法正确的是
A.该溶液的pH一定是10
B.该溶液不可能pH="4"
C.该溶液的pH不可能是7
D.不会有这样的溶
参考答案:C
本题解析:由题意可知由水电离的C(H+)=C(OH-)=1×10-10mol/L<1×10-7mol/L,说明水的电离受抑制,可能是酸溶液也可能是碱溶液
当是酸溶液时,溶液中的OH-全部来自于水的电离,溶液中的C(H+)=1×10-4mol/L,pH=4
当是碱溶液时,溶液中的H+全部来自于水的电离,溶液中的C(H+)=1×10-10mol/L,pH=10
故答案为C
本题难度:一般
4、选择题 下列关于电解质溶液中离子关系的说法正确的是
A.0.1 mol・L-1NaHCO3溶液中离子浓度关系:
c(Na+)=2c(CO)+c(HCO)+c(H2CO3)
B.0.1 mol/L NH4Cl和0.1 mol・L-1 NH3・H2O等体积混合后离子浓度关系:
c(Cl-)>c(NH)>c(H+)>c(OH-)
C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:
c(Na+)=c(CH3COO-)
D.常温下,在pH=1的溶液中,Fe2+、NO、ClO-、Na+能大量共存
参考答案:C
本题解析:
正确答案:C
A.不正确,物料守恒应为:
c(Na+)=c(CO)+c(HCO)+c(H2CO3)
B.不正确:c(NH)>c(Cl-)>c(OH-) >c(H+)
C.正确,由电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)得,
c(Na+)=c(CH3COO-)
D.不正确, 3Fe2++NO+4H+ =3Fe3++NO+2H2O、ClO-与Fe2+ 也不能大量共存
本题难度:简单
5、计算题 氘在化学、医药学及生物学等领域有广泛使用,也是制造氢弹和中子弹最重要的原料,1967年6月17日我国爆炸的第一颗氢弹用的炸药就是氘化锂。其实海洋是一个能源库,已知每1 L海水中大约有0.03 g氘,氘在海水中以重水(D2O)的形式存在。
(1)1 000 g氘化锂(6Li2H相对分子质量为8)的爆炸力相当于5万吨烈性TNT炸药。则生产90 g氘化锂至少需处理海水多少升?
(2)从海水中提取重水可用电解法获得氘气(D2),那么将1 L海水中所含重水的氘气全部电解出来用于制取氘时,理论上至少消耗多少电能?(已知断开1 mol化学键所吸收的能量或形成1 mol化学所放出的能量称为键能。又已知氧氘键的键能是463 kJ・mol-1,氘氘键的键能是436 kJ・mol-1,氧氧键的键能是493 kJ・mol-1)。
参考答案:(1)750 L? (2)1.83 kJ
本题解析:(1)先求出90 g氘化锂中含氘的质量,根据其摩尔质量之间的关系有:90 g× 2/8 ="22.5" g,需处理海水:22.5 g÷0.03 g・L-1="750" L。
(2)每个D2O中含两个D―O键,根据方程式:2D2O====2D2↑+O2↑,每电解2 mol重水需吸收的总能量为:4 mol×463 kJ・mol-1-2 mol×436 kJ・mol-1-1 mol×493 kJ・mol-1 ="487" kJ,即电解生成2 mol氘气即8 g氘,需487 kJ能量。所以每电解制得0.03 g氘吸收能量为:487 kJ×0.03 g/8 g="1.83" kJ。
本题难度:简单
|