微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
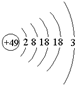
1、选择题 张青莲是我国著名的化学家。1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值。这是原子量表中首次采用我国测定的相对原子质量值。已知In的原子结构如图所示,则下列关于In的说法不正确的是(?)
A.In为长周期元素
B.In为过渡元素
C.In容易导电导热
D.In在反应中容易失电子
参考答案:B
本题解析:根据原子结构图可知,最外层电子数是3个,所以属于第ⅢA主族,B不正确。其余都是正确的,答案选B。
本题难度:一般
2、选择题 下列关于元素周期表的说法正确的是(?)
A.能生成碱的金属元素都在ⅠA族
B.原子序数为14的元素位于元素周期表的第3周期ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.最外层电子数是次外层电子数的2倍的原子容易失去电子成为阳离子
参考答案:B
本题解析:A、因ⅡA族的金属元素也能生成碱,如氢氧化镁,故A错误;
B、原子序数为14的原子为硅,有三个电子层,每一层的电子数分别为2、8、4,所以位于元素周期表的第3周期ⅣA族,故B正确;
C、因氦原子的最外层电子数为2,故C错误;
D、最外层电子数是次外层电子数的2倍的原子,比如碳,很稳定,故D错误;
故选:B。
点评:本题考查长式元素周期表的结构,要求学生对元素周期表的组成特点要熟悉,周期表中周期与周期之间,族与族之间含有较多规律,在学习中要善于抓住这些规律会起到事半功倍的效果。
本题难度:简单
3、选择题 下列各组物质的性质比较中,正确的是
A.热稳定性:H2O>HF>H2S
B.沸点:HF>HCl>HBr
C.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl
D.氧化性:Fe3+>Cu2+>H+
参考答案:D
本题解析:A项中氢化物的稳定性与元素的非金属性相关,非金属性越强气态氢化物越稳定,故错误,正确的为HF>H2O>H2S;B正确的顺序为HF>HBr>HCl;C中没有说明外界情况,无法判断,错误;D正确;
本题难度:一般
4、选择题 下列各组物质中,互为同位素的是
A.红磷与白磷
B.正丁烷与异丁烷
C.11H与21H
D.金刚石与C60
参考答案:C
本题解析:A、D 互为同素异形体
B 互为同分异构体
C 互为同位素
故选C
本题难度:一般
5、填空题 A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,能生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为?,B为?,C为?,D为?。(填元素符号)
(2)D的最高价氧化物的水化物的化学式是?,E的电子式是?。
(3)写出由A、B组成的化合物与E反应的化学方程式:?。
(4)请用电子式表示出C和D形成的化合物F的形成过程:?。
参考答案:(1)C?、O?、Na 、S?
(2)H2SO4?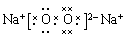 ?
?
(3)2CO2 + 2Na2O2 = 2Na2CO3 + O2?
(4)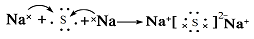
本题解析:(1)A原子的最外层上有4个电子,则A核外电子排布为2、4.所以A是C元素;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,能生成一种淡黄色的固体E;则B是O元素;C是Na元素,形成的淡黄色的固体E是Na2O2。D的L层电子数等于K、M两个电子层上的电子数之和。则D是S元素。(2)S最外层有6个电子,所以其的最高价氧化物的水化物的化学式是H2SO4。Na2O2是含有非碱性共价键的离子化合物。其电子式为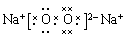 。(3)由C、O组成的化合物CO2与Na2O2反应的化学方程式:2CO2 + 2Na2O2 = 2Na2CO3 + O2。(4)Na和S形成的化合物Na2S的形成过程的电子式表示为:
。(3)由C、O组成的化合物CO2与Na2O2反应的化学方程式:2CO2 + 2Na2O2 = 2Na2CO3 + O2。(4)Na和S形成的化合物Na2S的形成过程的电子式表示为: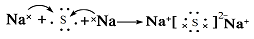 。
。
本题难度:一般