微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是(NA表示阿伏加德罗常数的值)
A.常温常压下,18g?NH4+所含的电子数为10NA
B.标准状态下,22.4L氧气所含的氧原子数为2?NA
C.56g金属铁与氯气反应时得到的电子数为2NA
D.1?mol由Na2O2和Na2O组成的混合物,其中的钠离子数为4?NA
参考答案:AB
本题解析:分析:A、质量换算物质的量结合离子结构计算电子数,铵根离子是10电子微粒;
B、依据气体摩尔体积计算物质的量,结合分子式计算原子数;
C、质量换算物质的量,结合铁和氯气反应生成的是氯化铁计算;
D、1molNa2O2和Na2O中都含有相同钠离子,均为2mol钠离子.
解答:A、18g NH4+物质的量为1mol,铵根离子是10电子微粒,所含的电子数为10NA,故A正确;
B、标准状态下,22.4L氧气物质的量为1mol,所含的氧原子数为2 NA,故B正确;
C、56g金属铁物质的量为1mol,完全与氯气反应时,氯气得到的电子数为3NA,故C错误;
D、Na2O2和Na2O中钠离子相同,1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为2NA,故D错误;
故选AB.
点评:本题考查了阿伏伽德罗常数的分析计算,主要考查气体摩尔体积的计算应用,质量换算物质的量计算微粒数,题目较简单.
本题难度:困难
2、选择题 用NA代表阿伏加德罗常数,下列说法正确的是( )
A.0.5mol?Al?与足量盐酸反应失去电子数为NA
B.0.2mol?H2O所含的H原子数为0.2NA
C.0.1mol?NH3所含的电子数为NA
D.46g NO2和N2O4的混合物含有的分子数为NA
参考答案:A.铝原子最外层为3个电子,发生化学反应易失去最外层3个电子,所以0.5mol?Al?与足量盐酸反应失去电子数为1.5NA个电子,故A错误;
B.根据水分子的分子式知,1个H2O分子中有2个氢原子,所以0.2mol?H2O所含的H原子数为0.4NA,故B错误;C.1个氮原子含有7个电子,一个氢原子含有1个电子,1个NH3所含的电子数为10个,所以0.1mol?NH3所含的电子数为NA,故C正确;
D.NO2的摩尔质量为46 g/mol,46g NO2的物质的量为1mol,N2O4的摩尔质量为92 g/mol,46g N2O4的物质的量为0.5mol,所以46 g NO2和N2O4的混合物含有的分子数只能在1 NA和0.5 NA之间,故D错误;
故选C.
本题解析:
本题难度:简单
3、选择题 以NA表示阿伏加德罗常数,下列说法中不正确的是
A.在常温常压下,14 g氮气所含原子数为NA
B.在标准状况下,2.24 L三氧化硫所含分子数为0.1 NA
C.在常温常压下,28 g的一氧化碳和乙烯混合气体,所含分子数为NA
D.常温常压下,1 mol甲基(-CH3)所含的电子数为9 NA
参考答案:B
本题解析:
本题难度:困难
4、选择题 设 表示阿伏加德罗常数,下列叙述中正确的是
表示阿伏加德罗常数,下列叙述中正确的是
①.31g白磷含有的P―P键数为 ②. 1mol
②. 1mol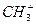 (碳正离子)中含有电子数为10
(碳正离子)中含有电子数为10 ③. 1mol铜与足量硫蒸气反应,转移电子数为2
③. 1mol铜与足量硫蒸气反应,转移电子数为2 ④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2
④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2 个电子 ⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA ⑥.0.84 g
个电子 ⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA ⑥.0.84 g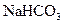 晶体中阳离子和阴离子总数为0.03
晶体中阳离子和阴离子总数为0.03 ⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑧.标准状况下,3.2g铜与足量的浓硝酸反
⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑧.标准状况下,3.2g铜与足量的浓硝酸反 应生成的气体含有的分子数是0.1NA ⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023 ⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
应生成的气体含有的分子数是0.1NA ⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023 ⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A ②④⑦⑧ B ③④⑥⑦⑧ C ④⑦ D④⑥⑨⑩
参考答案:C
本题解析:略
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
A.4gCH4中含有2.5NA个电子
B.1molO2作为氧化剂得到的电子数为2NA
C.通常状况下,NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
参考答案:A、4g CH4 物质的量为0.25mol,甲烷分子中含有10个电子,所以含有2.5NA个电子,故A正确;
B、1 mol O2作为氧化剂得到的电子数为2NA,氧气做氧化剂可以变为-2价,也可以变为-1价;故B错误;
C、气体摩尔体积的条件是标准状况,通常状况下,NA个CO2分子占有的体积不是22.4 L,故C错误;
D、物质的量浓度为0.5 mol/L的MgCl2溶液中,体积不知,无法计算微粒物质的量,故D错误;
故选A.
本题解析:
本题难度:简单