|
高中化学必备知识点《物质的量》考点巩固(2017年最新版)(六)
2017-08-10 01:12:27
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A.16g
B.32g
C.64g /mol
D.32g /mol
|
参考答案:D
本题解析:1.505×1023个X气体分子的物质的量是1.505×1023/6.02×1023mol-1=0.25mol,根据M=m/n得X气体的摩尔质量M=8g/0.25mol=32g/mol,答案选D。
考点:考查摩尔质量的计算
本题难度:一般
2、选择题 下列叙述正确的是
[? ]
A.H2O的摩尔质量为18g
B.16克CH4含有的分子数为6.02×1023?
C.常温、常压下1molNH3的体积约为22.4L
D.1L1mol/LNa2SO4溶液中含Na+为1mol
参考答案:B
本题解析:
本题难度:简单
3、选择题 下列关于物质的量和摩尔质量的叙述,正确的是
[? ]
A.水的摩尔质量是18g
B.0. 012kg 12C中约含6. 02×1023个C原子
C.1mol水中含有2mol氢和1mol氧
D.1mol任何物质都含有6.02×1023个分子
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列说法或表示方法正确的是( )
A.反应物的总能量低于生成物的总能量时,该反应一定不能发生
B.在10lkPa、25℃时,1gH2完全燃烧生成气态水,放出120.9kJ的热量,则氢气的燃烧热为241.8kJ/mol
C.已知:2SO2(g)+O2(g)

2SO3(g);△H=-98.3kJ/mol.将1molSO2和0.5molO2充入一密闭容器中反应,放出49.15kJ的热量
D.由石墨比金刚石稳定可知:C(金刚石,s)=C(石墨,s);△H<0
参考答案:A、依据能量守恒,反应物的总能量低于生成物的总能量时,该反应为吸热反应,故A错误;
B、燃烧热是指1mol可燃物质完全燃烧生成稳定氧化时放出的热量,根据1gH2完全燃烧生成气态水放热计算不符合概念要求,故B错误;
C、2SO2(g)+O2(g)

2SO3(g);△H=-98.3kJ/mol.将1molSO2和0.5molO2充入一密闭容器中反应,由于反应是可逆反应,所以放出的热量<49.15kJ,故C错误;
D、由石墨比金刚石稳定可知石墨的能量低,所以,金刚石能量高转化为石墨是放热反应,C(金刚石,s)=C(石墨,s);△H<0,故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 设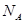 表示阿伏加德罗常数,下列叙述中正确的是? 表示阿伏加德罗常数,下列叙述中正确的是?
①.31g白磷含有的P―P键数为NA?
②. 1mol CH3+(碳正离子)中含有电子数为10NA?
③. 1mol铜与足量硫蒸气反应,转移电子数为2NA?
④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2NA个电子?
⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA?
⑥.0.84 g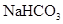 晶体中阳离子和阴离子总数为0.03NA? 晶体中阳离子和阴离子总数为0.03NA?
⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA?
⑧.标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA?
⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023?
⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A ②④⑦⑧? B ③④⑥⑦⑧? C ④⑦? D④⑥⑨⑩
参考答案:C
本题解析:①在一个白磷P4分子中含有6个P―P共价键,所以.31g白磷含有的P―P键数为31g ÷(31×4)g/mol×NA=1.5NA.错误. ②. 1molCH3+(碳正离子)中含有电子数为9NA .错误. ③由于S的氧化性弱,在与Cu反应时1个S只能得到1个电子,所以 1mol铜与足量硫蒸气反应,转移电子数为NA。错误。④Mg是+2价的金属,因此1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2NA个电子。正确。⑤.用惰性电极电解CuCl2溶液,实质就是电解CuCl2本身。若阴极析出16g铜时,n(Cu)=16g÷64g/mol=0.25mol,Cu是+2价的金属,所以线路中通过的电子是0. 5mol,即电子数为0. 5NA。错误。⑥电离方程式为NaHCO3=Na++HCO3-,0.84 g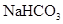 的物质的量0.01mol,所以在晶体中阳离子和阴离子总数为0.02NA.错误。⑦3.9gNa2O2的物质的量为0.05mol,每有1mol的Na2O2吸收足量的CO2时转移电子1mol,所以0.05mol的Na2O2反应转移的电子数是0.05NA。正确。⑧反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O.若有1mold Cu反应,产生NO21mol。n(Cu)=3.2g÷64g/mol=0.05mol,所以在标准状况下,3.2g铜Cu与足量的浓硝酸反应生成的气体含有的分子数是0.05NA.错误。⑨C16O相对分子质量是28,28 g C16O的物质的量为1mol,含有质子数是14×6.02×1023?;C18O相对分子质量是30,28 g C18O中含有的质子的物质的量小于1mol,因此含有的质子数小于14×6.02×1023。错误。⑩.标准状况下,22.4 L氯气的物质的量为1mol,反应方程式为 Cl2+2NaOH=NaCl+NaClO+H2O。所以1mol的氯气与足量氢氧化钠溶液反应转移的电子数为1×6.02×1023 .错误。因此正确的说法是④⑦,选项为C。 的物质的量0.01mol,所以在晶体中阳离子和阴离子总数为0.02NA.错误。⑦3.9gNa2O2的物质的量为0.05mol,每有1mol的Na2O2吸收足量的CO2时转移电子1mol,所以0.05mol的Na2O2反应转移的电子数是0.05NA。正确。⑧反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O.若有1mold Cu反应,产生NO21mol。n(Cu)=3.2g÷64g/mol=0.05mol,所以在标准状况下,3.2g铜Cu与足量的浓硝酸反应生成的气体含有的分子数是0.05NA.错误。⑨C16O相对分子质量是28,28 g C16O的物质的量为1mol,含有质子数是14×6.02×1023?;C18O相对分子质量是30,28 g C18O中含有的质子的物质的量小于1mol,因此含有的质子数小于14×6.02×1023。错误。⑩.标准状况下,22.4 L氯气的物质的量为1mol,反应方程式为 Cl2+2NaOH=NaCl+NaClO+H2O。所以1mol的氯气与足量氢氧化钠溶液反应转移的电子数为1×6.02×1023 .错误。因此正确的说法是④⑦,选项为C。
本题难度:一般
|