|
���л�ѧ֪ʶ����ɡ������йص����ӷ���ʽ����д������ǿ����ϰ��2017��Ѻ��棩(��)
2017-08-10 01:16:48
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����?��?��
A��Ư����Һ��ͨ�����������̼��
Ca2++2ClO-+H2O+CO2=CaCO3��+2HClO
B��NaOH��Һ�е��˱���FeCl3��Һ��
Fe3++3H2O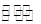 3H++3Fe��OH��3�����壩 3H++3Fe��OH��3�����壩
C������������ˮ������ˮ��Cl2+H2O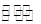 H++Cl-+HClO H++Cl-+HClO
D���������ữ��KMnO4��Һ��H2O2��Ӧ��
| 2MnO4-+10H++3H2O2=2Mn2++3O2��+8H2O
�ο��𰸣�C
���������
��ȷ�𰸣�C
A�����ӷ���ʽ��ClO-+H2O+CO2=HCO3�D��HClO
B�����ӷ���ʽ��Fe3++3H2O 3H++3Fe��OH��3�����壩 3H++3Fe��OH��3�����壩
D�����ӷ���ʽ��2MnO4-+6H++5H2O2=2Mn2++8H2O
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ��ȷ����
A������ϡ���ᷴӦ��2Fe �� 6H�� �� 2Fe3�� ��3H2��
B��Al(OH) 3�����еμ�����Al(OH)3 �� H�� �� Al3����H2O
C��̼��������Һ�м���ϡ���HCO3�� ��H+�� CO2 �� ��H2O
D��̼�����ϡ���ᷴӦ��CO32�� �� 2H���� CO2�� �� H2O
�ο��𰸣�C
���������
A������ϡ���ᷴӦ��2Fe �� 6H�� �� 2Fe3�� ��3H2��?��������ʵ��ֻ�����ɶ���������
B��Al(OH) 3�����еμ�����?Al(OH)3 �� H�� �� Al3����H2O?��ɲ��غ㣻
C��̼��������Һ�м���ϡ���HCO3�� ��H+�� CO2 �� ��H2O?��ȷ��
D��̼�����ϡ���ᷴӦ��CO32�� �� 2H��?��? CO2�� �� H2O?̼�������������ܲ���ѡC��
���������ӷ���ʽ�����жϵIJ��裺
1.������ԭ��
�ſ���ʵԭ��
��2Fe + 6H+ = 2Fe3+ + 3H2��������H+���ܰ�Fe������Fe3+����ֻ��������Fe2+��ӦΪ��Fe + 2H+ ="===" Fe2+ + H2����
�������غ�ԭ��
��Na + H20 =Na+ + OH- + H2�������ڷ�Ӧǰ��Hԭ�ӵ���Ŀ���ȡ�ӦΪ��2Na + 2H2O = 2Na+ + 2OH- + H2����
�ǵ���غ�ԭ��
��Fe3+ + Cu = Fe2+ + Cu2+�������������ߵ�ɲ��غ㡣ӦΪ��2Fe3+ + Cu =2Fe2+ + Cu2+��
�ȶ����ԭ��
��ϡ������Ba(OH)2��Һ��Ӧ��H+ + SO42- + Ba2+ + OH- = BaSO4�� + H2O������SO42-��H+��Ba2+��OH-δ��ѭ1��2��һ����ɡ�ӦΪ��2H+ + SO42- + Ba2+ + 2OH- =BaSO4�� + 2H2O��
2.���������
���ܲ�ֵ�����
�ܲ�ֵ�����һ��Ϊǿ�ᣨ������HCl����ǿ�����������NaOH�����ʹ�����������Σ��Ȼ���NaCl����ǿ�����
�Ʋ��ܲ�ֵ�����
һ�������ﲻ��
���������������ﲻ��
˵������������Ӧ�Ũ�Ƚ�Сʱ�������ʽ��Ũ�Ƚϴ�ʱӦд�ɻ�ѧʽ��
����������ʲ���
�ġ������ﲻ��
�塢�������ʽ�������
ע�⣺����ǿ�����ʽ�Σ���NaHSO4����������ϡ��Һ��Ӧ��д��
H+��SO42-��ʽ����Ũ��Һ�в�����д��HSO4-;��
�������෴Ӧ����
д���ӷ�Ӧ��ǰ������ˮ��Һ�л�����״̬�½��еķ�Ӧ�����������ķ�Ӧ���������ӷ�Ӧ��ֻ��д��ѧ����ʽ����д���ӷ���ʽ��
�ߡ��ǵ���ʲ���
���ǡ��Ҵ��ȴ�����л����Ƿǵ���ʣ�����д���ӷ���ʽʱ�����ܲ�Ӧд����ʽ��
�����Ѷȣ�һ��
3������� �ס��ҡ�����������֮��������ת����ϵ��
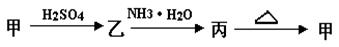
��1�������Dz�����ˮ�İ�ɫ�������ʣ�������������������������������Һ�������_____________д���� ��ת���Ļ�ѧ����ʽ :_______________________________ . ��ת���Ļ�ѧ����ʽ :_______________________________ .
��2��������Һ�м���KSCN��Һ ,��Ѫ��ɫ����,���������_________________.
д�� �� ��ת�������ӷ���ʽ___________________________________. ��ת�������ӷ���ʽ___________________________________.
�ο��𰸣���1��Al2O 3��1�֣� ��Al2��SO4��3+6NH3��H2O===2Al��OH��3 ?+3��NH4��2SO4��3�֣� 3��1�֣� ��Al2��SO4��3+6NH3��H2O===2Al��OH��3 ?+3��NH4��2SO4��3�֣�
��2��Fe2O3��1�֣� ��Fe2O3+6H+===2Fe3++3H2O��3�֣�
�����������
�����Ѷȣ���
4��ѡ���� ����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ��ѧ����ʽ���ǣ�������
A�����������缫�������������Һ��2H2O 2H2��+O2��
B����ȩ��������Ӧ��CH3CHO+2[Ag��NH3��2]++2OH-CH3COO-+NH4++2Ag��+3NH3+H2O
C����̼������Һ����������������2CO32-+2SO2+H2O=2HCO3-+SO32-
D��̼���Ⱶ��Һ�м������������������Һ��Ba2++HCO3-+OH-=BaCO3��+H2O
�ο��𰸣�A�����������缫�������������Һ����������ʧ���ӷ���������Ӧ����Ӧ������ˮ�ķ�Ӧ����A����
B����ȩ��������Һ��Ӧ�����ӷ���ʽ��д��ȷ����B��ȷ��
C����̼������Һ�������������������ӷ���ʽӦ����������������ӣ���C����
D��̼���Ⱶ��Һ�м������������������Һ����̼���Ⱶ��ȫ��Ӧ��д�����ӷ���ʽΪBa2++2HCO3-+2OH-=BaCO3��+2H2O+CO32-����D����
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ�У���ȷ����
A���ڵ��۵⻯����Һ�м���ϡ�����ữ����ͨ��ClO2���壬��Һ������
2ClO2+10I����4H2O��5I2��2Cl����8OH-
B������������Һ��ͨ������������壺2ClO-+SO2+H2O ="=" 2HClO+SO32-
C��100mL4mol/L NaOH��Һ��ȫ����6.72L����״���£�CO2��
3 CO2+4OH��= CO32-+2HCO3-+H2O
D����Ũ�ȵ�NH4Al(SO4)2��Һ��Ba(OH)2��Һ��1:2����Ȼ�ϳ��ְ�ɫ������
|