微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 密闭容器中发生下列反应:N2+3H2 2NH3 △H<0 ,下图是某一时间段中反应速率与反应进程的曲线关系图。回答下列问题:
2NH3 △H<0 ,下图是某一时间段中反应速率与反应进程的曲线关系图。回答下列问题:
(1)处于平衡状态的时间段是_________________
(2)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
t1 时刻 ___________________________ t3时刻___________________________
t4时刻____________________________
(3)下列时间段中,氨的百分含量的大小关系是:t0 - t1_______ t2 - t3 (填 “>”“<”“=”)
(4)t6时刻,若升高温度,反应速率变化情况画在下图中。

参考答案:(1)t0-t1、t2-t4、t5-t6
(2)增加生成物C;加催化剂;降低压强
(3)<
(4)“略”
本题解析:
本题难度:一般
2、选择题 NO2中存在下列平衡:2NO2?N2O4(g)(正反应是放热反应).在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
A.温度130℃,压强3.03×105?Pa
B.温度25℃,压强1.01×105?Pa
C.温度130℃,压强5.05×104?Pa
D.温度0℃,压强5.05×104?Pa
参考答案:由于存在平衡2NO2(g)?N2O4(g),N2O4的存在会影响二氧化氮的相对分子质量测定,故应采取措施使平衡向左移动,减小N2O4的含量,该反应正反应是体积减小的放热反应,减小压强平衡向逆反应移动,升高温度平衡向逆反应移动,故应采取高温低压,故选C.
本题解析:
本题难度:一般
3、选择题 一定条件下,在一体积恒定的容器中发生CO+NO2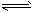 CO2+NO反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
CO2+NO反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
[? ]
A.正反应为吸热反应
B.正反应为放热反应
C.降温后CO的浓度增大
D.降温后各物质的浓度不变
参考答案:B
本题解析:
本题难度:一般
4、选择题 一定温度时于密封容器中发生反应:mA(g)+nB(g) pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是
pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是
[? ]
A.平衡向正反应方向移动
B.C气体的质量分数增大
C.气体A的转化率降低
D.m+n>p
参考答案:C
本题解析:
本题难度:一般
5、简答题 无水氯化铝是一种重要的化工原料,利用明矾石[K2SO4?Al2(SO4)3?2Al2O3?6H2O]制备无水氯化铝的流程如下:
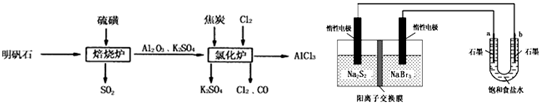
(1)焙烧炉中产生的SO2直接排放到空气中会形成酸雨,若某地酸雨的pH为4.6,在空气中放置一段时间后,pH变为4.0,其原因为______;(用必要的文字简述).
(2)氯化炉中发生的主要反应为:2Al2O3(s)+6Cl2(g)?4AlCl3(g)+3O2(g)△H>0.反应达平衡时,加焦炭能使平衡向正反应方向移动,理由是______.
(3)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染.试设计简单实验检验二者是否恰好完全反应.(简要描述实验步骤、现象和结论)______.
仪器自选,可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液?②氯化亚铁溶液?③硫氰化钾溶液?④品红溶液
(4)工业上利用如下装置制备氯气:已知左侧原电池的工作原理为:2Na2S2+NaBr3
Na2S4+3NaBr
①用惰性电极电解饱和食盐水的化学方程式为______.
②如图所示原电池放电时,电池中的Na+向______(填“左槽”或“右槽”)移动.左槽中发生的电极反应式为______.
③该原电池工作一段时间后,测得左槽中Na+物质的量由a?mol变为b?mol,则电解池中b电极上得到的气体在标准状况下的体积为______L(不考虑气体的损失).
参考答案:(1)酸雨中的弱酸亚硫酸被氧化为强酸硫酸,使溶液中的c(H+)增大,pH减小,
故答案为:酸雨中的弱酸亚硫酸被氧化为强酸硫酸,使溶液中的c(H+)增大,pH减小;
(2)焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动,
故答案为:焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动;
(3)取少量溶液,向其中加入品红溶液,若品红溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应,
故答案为:取少量溶液,向其中加入品红溶液,若品红溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应;
(4)①惰性电极电解饱和氯化钠溶液,生成氢气、氯气、氢氧化钠,电解总反应式为:2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑;
②原电池左侧发生氧化反应,为负极,右侧为正极,电解质溶液钠离子向正极移动,即向右槽移动;
由反应2Na2S2+NaBr3?放电?.?Na2S4+3NaBr可知,左侧S22-放电生成S42-,电极反应式为:2S22--2e-=S42-,
故答案为:右槽;2S22--2e-=S42-;
③该原电池工作一段时间后,测得左槽中Na+物质的量由a?mol变为b?mol,则转移电子的物质的量为(a-b)mol,电解池中b电极连接电源的正极,为阳极,得到的气体为氯气,根据电子转移守恒可知氯气的物质的量为你(a-b)mol2,故生成氯气的体积=(a-b)mol2×22.4L/mol=11.2(a-b)L,
故答案为:11.2(a-b).
本题解析:
本题难度:一般