微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 配制一定物质的量浓度溶液时,能使所配溶液的浓度偏高的原因是( )
A.没有用水冲洗烧杯2-3次
B.溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切
C.定容时俯视液面使与刻度线相切
D.定容时仰视液面使与刻度线相切
参考答案:C
本题解析:
本题难度:一般
2、填空题 用Na2CO3?10H2O晶体,配制0.2mol/L的Na2CO3溶液480mL.
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少?,?;
(2)应用托盘天平称取Na2CO3?10H2O的晶体的质量为?g;
(3)配制溶液时有以下几个操作:
①溶解 ?②摇匀 ?③洗涤 ?④冷却 ?⑤称量 ?⑥转移溶液?⑦定容
正确的操作顺序是?(填序号).
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空.
①碳酸钠失去了部分结晶水 ?②用“左码右物”的称量方法称量晶体③碳酸钠晶体不纯,其中混有氯化钠?④称量碳酸钠晶体时所用砝码生锈⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有?,无影响的有?.(填序号)
参考答案:
本题解析:
本题难度:一般
3、简答题 三大强酸的性质均与浓度有关.回答下列问题:
(1)某学习小组用15mol/L浓硝酸配制100mL 3mol/L稀硝酸.
①他们需要用量筒量取15mol/L浓硝酸______mL;
②如图所示仪器,在配制过程中不需用的是______(填序号).
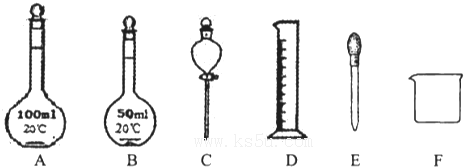
除图中已有的仪器外,配制上述溶液还需用到的玻璃仪器是______;
③下列实验操作中,不正确的是______(填写标号).
A.使用容量瓶前,检查它是否漏水.
B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出.
C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容.
D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀.
④用量筒量取浓硝酸,读数时,俯视量筒,所配制溶液的浓度______(填“偏高、偏低、无影响”).
(2)①铜与浓硫酸在加热条件下反应,浓硫酸表现出来的性质是______.
②MnO2与浓盐酸在加热条件下反应,离子方程式为______.
③分别用浓硝酸和稀硝酸制取相同质量Cu(NO3)2晶体,消耗浓硝酸和稀硝酸的物质的量之比是______.
参考答案:(1)①设需要浓硝酸的体积为V,则0.1L×3mol/L=15mol/L×V,V=0.02L=20.0mL,
故答案为:20.0mL;
②配制100mL 3mol/L稀硝酸需要量筒、烧杯、玻璃棒、胶头滴管以及容量瓶等仪器,则不需要的仪器为50mL容量瓶、分液漏斗,还缺少玻璃棒,
故答案为:BC;玻璃棒;
③A.容量瓶有瓶塞,配制过程中需要摇匀,所以使用容量瓶前,检查它是否漏水,故A正确;
B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故B错误;
C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容;容量瓶只能用于配制一定浓度的溶液,不能用于稀释或者加热,故C错误;
D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀,该存在符合配制要求,故D正确;
故选BC;
④用量筒量取浓硝酸,读数时俯视量筒,导致量取的浓硝酸的体积偏小,配制的溶液中溶质的物质的量偏小,所配制溶液的浓度偏低,
故答案为:偏低;
(2)①铜与浓硫酸在加热条件下反应方程式为:Cu+2H2SO4(浓)△.CuSO4+SO2↑+2H2O,该反应中,浓硫酸将铜氧化成铜离子,浓硫酸表现了氧化性;反应产物中有硫酸铜和水生成,所以浓硫酸有表现了酸性,
故答案为:氧化性和酸性;
②二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,反应的离子方程式为MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O;
③设制取的硝酸铜的物质的量为nmol,根据反应的相关方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO2↑+4H2O可知,需要浓硝酸的物质的量为:4nmol,需要稀硝酸的物质的量为:83nmol,则消耗浓硝酸和稀硝酸的物质的量之比是:4nmol:83nmol=3:2,
故答案为:3:2.
本题解析:
本题难度:一般
4、选择题 实验室需配制?480mL?1mol/L?NaOH?溶液,下列叙述正确的是( )
A.转移液体时,玻璃棒应紧靠容量瓶口
B.用托盘天平称量19.2克NaOH固体
C.容量瓶上标有温度、浓度、容积和压强
D.定容时若俯视刻度线观察液面,会使所配制的NaOH?溶液的浓度偏高
参考答案:D
本题解析:
本题难度:一般
5、简答题 用质量分数为98%的浓硫酸配制100ml?3.0mol/L?稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积?②量取一定体积的浓硫酸?③溶解?④转移、洗涤?⑤定容?⑥摇匀
回答下列问题
(1)若所用浓硫酸密度为1.84g/cm3,则该浓硫酸的物质的量浓度为______,配制上述稀硫酸所需浓硫酸的体积是______(小数点后保留一位),量取浓硫酸所用的量筒的规格是______(从下列中选用A.10ml?B.20ml
C.50ml?D.100ml)
(2)第⑤步实验的操作是______
(3)为了保证实验的准确性,在第③和第④步操作之间还应该加多一步什么操作______,如果在配制溶液过程中出现下列情况对所配稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水______
B.所用过的烧杯、玻璃棒未洗涤______
C.定容时仰视容量瓶刻度线______.
参考答案:(1)该浓硫酸的物质的量浓度为1000×1.84×98%98mol/L=18.4mol/L,根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=100mL×3mol/L,解得:x≈16.3,故应选择20mL的量筒,
故答案为:18.4mol/L;16.3;B;
(2)定容操作为:向容量瓶内加蒸馏水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切为止,
故答案为:向容量瓶内加蒸馏水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切为止;
(3)浓硫酸稀释放出大量的热,向容量瓶内转移溶液应先冷却至室温,故答案为:冷却至室温;
A.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
B.所用过的烧杯、玻璃棒未洗涤,少量溶质硫酸沾在烧杯壁与玻璃棒上,移入容量瓶内溶质硫酸的物质的量偏小,所配溶液的浓度偏小;
C.定容时,仰视容量瓶刻度线,液面在刻度线以上,导致所配溶液体积判断,所配溶液浓度偏大;
故答案为:无影响;偏小;偏小.
本题解析:
本题难度:一般