| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《化学平衡常数》高频考点预测(2017年最新版)(八)
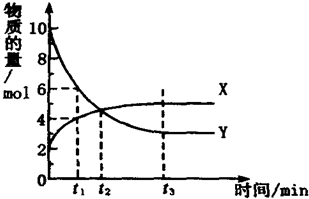 参考答案:B 本题解析: 本题难度:简单 2、选择题 化学平衡常数(K)、弱酸的电离常数(Ka)、难溶物的溶度积常数(KSP)是判断物质性质或变化的重要的平衡常数.下列关于这些常数的说法中,正确的是(? ) 参考答案:C 本题解析: 本题难度:简单 3、选择题 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( ? ) |
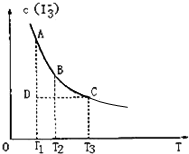
参考答案:BC
本题解析:
本题难度:简单
4、简答题 乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0
请回答:(1)该反应的化学平衡常数表达式为______.
(2)当温度T1>T2时,化学平衡常数K1______K2(填“>”、“<”或“=”).
(3)在工业生产中,可使H2的转化率和化学反应速率同时提高的措施有______(写出一条合理措施即可).
(4)工业上,常以乙醇为原料生产乙醛.根据如图所示信息,该反应是______反应(填“放热”或“吸热”),判断依据是______.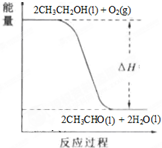
参考答案:(1)可逆反应2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)的平衡常数k=c(CH3CH2OH)?c3(H2O)c2(CO2)?c6(H2),
故答案为:c(CH3CH2OH)?c3(H2O)c2(CO2)?c6(H2);
(2)该反应正反应是放热反应,升高温度平衡向逆反应移动,平衡常数减小,即温度越高,平衡常数越小,温度T1>T2,故K1<K2,故答案为:<;
(3)改变条件加快反应速率,同时平衡向正反应移动,可以增大CO2浓度或增大压强,反应速率加快,平衡向正反应移动氢气的转化率增大,故答案为:增大CO2浓度或增大压强;
(4)由图象可知,反应物的总能量大于生成物的总能量,故该反应物为放热反应,
故答案为:放热,反应物的总能量大于生成物的总能量.
本题解析:
本题难度:一般
5、选择题 一氧化氮与一氧化碳都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳。对此反应,下列叙述中正确的是
[? ]
A.使用催化剂能改变平衡常数
B.使用催化剂能改变反应速率
C.改变压强对反应速率没有影响
D.降低压强能加大反应速率
参考答案:B
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学必备知识点《无机综合与.. | |