��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��1 L�ܱ������У�����һ������A������Ӧ��A(g) 2B(g)(����ӦΪ���ȷ�Ӧ)������Ӧ�ﵽƽ��ı�Ӱ��ƽ���һ����������Ӧ�ﵽ�µ�ƽ�⡣��ͼ�������߷ֱ��ʾ������Ӧ�������������ʵ�Ũ�ȱ仯��ϵ������˵����ȷ���ǣ�?��
2B(g)(����ӦΪ���ȷ�Ӧ)������Ӧ�ﵽƽ��ı�Ӱ��ƽ���һ����������Ӧ�ﵽ�µ�ƽ�⡣��ͼ�������߷ֱ��ʾ������Ӧ�������������ʵ�Ũ�ȱ仯��ϵ������˵����ȷ���ǣ�?��
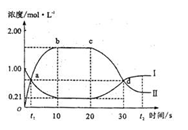
A��a���d��ֱ��ʾ������ͬ��ƽ��״̬
B����a�㣬B�����ʵ���Ũ��Ϊ0.67 mol��L
C��20s��t2s����ʾ�����¶�ʹƽ���ƶ��Ĺ���
D��0s��10s�䣬��B��ʾ�ķ�Ӧ����Ϊ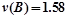 mol/(L��s)
mol/(L��s)
�ο��𰸣�B
������������⿼����ǻ�ѧƽ����й����ݡ�
A��a���d�㷴Ӧ������Ũ�Ȼ��ڷ����仯������ƽ��״̬����A����
B��a��ʱ��A��B��Ũ����ȣ�A����ʼŨ��Ϊ1mol/L����a��B��Ũ��Ϊc�����ݷ���ʽA��g��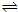 2B��g����֪A��Ũ�ȱ仯Ϊ0.5c������1mol/L-0.5c=c�����c=0.67mol/L����B��ȷ��
2B��g����֪A��Ũ�ȱ仯Ϊ0.5c������1mol/L-0.5c=c�����c=0.67mol/L����B��ȷ��
C����ͼ��֪20s��t2s��B��Ũ�ȼ�С��A��Ũ�������������¶�ʹƽ���ƶ�����ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ�ƶ���B��Ũ��Ӧ������A��Ũ��Ӧ���ʲ������ǽ����¶ȣ�ӦΪ�����¶ȣ���C����
D����ͼ��֪0s��10s��A��Ũ�ȱ仯Ϊ1mol/L-0.21mol/L=0.79mol/L������v��A��=
0.79mol/L
10s
0.079mol/��L?mol��������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��B��=2v��A��=2��0.079mol/��L?mol��=0.158mol/��L?mol������D����
�ʱ���ѡ��B��
�����Ѷȣ�һ��
2��ѡ���� t��ʱ����һ�ܱ������г���2mol A��3mol B���������»�ѧ��Ӧ��aA+B C+B����Ӧ������Ϊ���壩ƽ����֪������Ũ�������¹�ϵ����c��A����a��c��B����c��C����c��D��Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬����ʱB��ת������
C+B����Ӧ������Ϊ���壩ƽ����֪������Ũ�������¹�ϵ����c��A����a��c��B����c��C����c��D��Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬����ʱB��ת������
A��60%?B��40%?C��50%? D����ȷ��
�ο��𰸣�B
���������ƽ����֪������Ũ�������¹�ϵ����c��A����a��c��B����c��C����c��D���������ƽ�ⳣ������ʽK�� ��֪��K��1�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��˵��ƽ�ⲻ�䣬��˷�Ӧǰ��������䣬��a��1������
��֪��K��1�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��˵��ƽ�ⲻ�䣬��˷�Ӧǰ��������䣬��a��1������
A? +? B C? +? B
C? +? B
��ʼ����mol�� 2? 3? 0? 0
ת������mol��x? x? x? x
ƽ������mol��2��x? 3��x? x? x
���ڷ�Ӧǰ��������䣬���Կ��������ʵ�������Ũ�Ƚ���ƽ�ⳣ������
��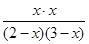 ��1
��1
���x��1.2
����B��ת���ʣ� ��100%��40%����ѡB��
��100%��40%����ѡB��
�����Ѷȣ�һ��
3��ѡ���� ��֪2SO2(g)+O2(g)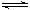 2SO3(g)?��H=��197kJ/mol����25��ʱ�����ѹ�ܱ�������ͨ��2 mol SO2��1 mol O2���ﵽƽ��ʱ�ų�����a1����25��ʱ�ڴ˺�ѹ�ܱ�������ֻͨ��1 mol SO2��0.5 mol O2���ﵽƽ��ʱ�ų�����a2�������й�ϵ��ȷ����
2SO3(g)?��H=��197kJ/mol����25��ʱ�����ѹ�ܱ�������ͨ��2 mol SO2��1 mol O2���ﵽƽ��ʱ�ų�����a1����25��ʱ�ڴ˺�ѹ�ܱ�������ֻͨ��1 mol SO2��0.5 mol O2���ﵽƽ��ʱ�ų�����a2�������й�ϵ��ȷ����
A��2a2=a1="197" kJ
B��197 kJ> a1=2a2
C��a2>a1>197 kJ
D��2a2<a1<197 kJ
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
4������� ú�����г����о���ͬ�¶��µ�ƽ�ⳣ����Ͷ�ϱȼ����ʵ����⡣��֪��
CO��g����H2O��g��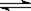 ?CO2��g����H2��g����ƽ�ⳣ�����¶ȵı仯���±���
?CO2��g����H2��g����ƽ�ⳣ�����¶ȵı仯���±���
�¶�/��
| 400
| 500
| 830
| 1000
|
ƽ�ⳣ��K
| 10
| 9
| 1
| 0.6
|
�Իش��������⣺��1��������Ӧ������Ӧ��?��Ӧ������ȡ������ȡ�����
��2��ij�¶��£�������Ӧ�ﵽƽ���������������������¶ȣ�����Ӧ����?
�����������С�����䡱���������ڻ�������ѹǿ?�����������С�����䡱����
��3��830�棬�ں��ݷ�Ӧ���з�������еķ�Ӧ�������е����ʵ���Ͷ�뷴Ӧ��������������Ӧ������е���?��ѡ��A��B��C��D����
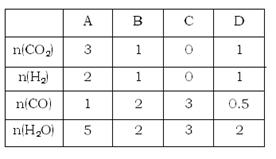
��4��830��ʱ����2L���ܱ������м���4molCO(g)��6molH2O(g)�ﵽƽ��ʱ��CO��ת������?��
�ο��𰸣���ÿ��2�֣���10�֣���1�����ȣ�2�֣�?��2������2�֣�������2�֣�
��3��B��C��2�֣�ѡһ������ȷ��1�֣��д�ѡ�����֣�?��4��60%��2�֣�
�����������1�����ݱ������ݿ�֪�������¶ȵ����ߣ�ƽ�ⳣ����С����˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ����������Ӧ�Ƿ��ȷ�Ӧ��
��2����������������������¶ȣ�����Ӧ���������淴Ӧ��������ij̶ȸ�������ƽ�����淴Ӧ�����ƶ���������������ʵ����Dz���ģ����¶����ߣ����������������ѹǿ����
��3�����ݱ������ݿ�֪��ѡ��C������û����������Է�Ӧһ����������Ӧ������еġ���ѡ��A��B��D�д�ʱ���ӻ��ֱ���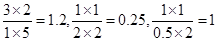 ������830����ƽ�ⳣ����1������ѡ��A�����淴Ӧ������еģ�B��������Ӧ������еģ���Dǡ����ƽ��״̬����ѡBC��
������830����ƽ�ⳣ����1������ѡ��A�����淴Ӧ������еģ�B��������Ӧ������еģ���Dǡ����ƽ��״̬����ѡBC��
��4����ﵽƽ��ʱ��CO��ת������x��������CO��ˮ��������4x��������CO2����������4x�����Ը���ƽ�ⳣ������ʽ��֪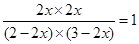 �����x��60����
�����x��60����
�����Ѷȣ�һ��
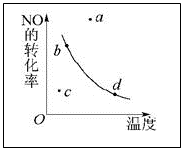
5��ѡ���� ͼ�е������DZ�ʾ��������һ��ʱ��2NO��O2 2NO2�SH<0��Ӧ��NO��ת�������¶ȵĹ�ϵ���ߣ�
2NO2�SH<0��Ӧ��NO��ת�������¶ȵĹ�ϵ���ߣ�
ͼ�б���a��b��c��d�ĵ㣬���б�ʾδ�ﵽƽ��״̬����v(��)��v(��)�ĵ���(����).
A��a��
B��b��
C��c��
D��d��
�ο��𰸣�C
�����������ͼ��֪�������ϵĵ�b��d��ʾ��Ӧ�ﵽƽ��״̬��c���NOת����С��ƽ��ʱ��NOת���ʣ�����ʱ��Ӧδ�ﵽƽ�⣬v(��)��v(��)��a���NOת���ʴ���ƽ��ʱ��NOת���ʣ���Ӧ�����淴Ӧ������У�v(��) < v(��)����ѡC��
��������ѧƽ��ͼ���ǻ�ѧƽ���һ����Ҫ֪ʶ�㣬����߿��������飬�����ڱ���������Ӧѧ�����ͼ��
�����Ѷȣ�һ��