微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于处于化学平衡状态的反应CO(g)+H2O(g)?CO2(g)+H2(g)?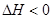 ,若要提高CO的转化率,下列措施中可行的是?(?)
,若要提高CO的转化率,下列措施中可行的是?(?)
A.升温
B.增大H2O(g)的浓度
C.增大压强
D.使用合适的催化剂
参考答案:B
本题解析:A错,该反应的正反应方向为放热反应,升温,平衡向逆反应方向移动,CO的转化率减小;B正确;C错,该反应为等体积反应,改变压强,平衡不移动;D错,催化剂不能影响平衡的移动;
本题难度:一般
2、选择题 在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )。
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )。
A.x的值为2
B.A的转化率为40%
C.B的平衡浓度为0.8 mol/L
D.D的体积分数为20%
参考答案:B
本题解析:略
本题难度:简单
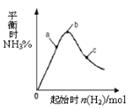
3、选择题 在300℃时,改变起始反应物中n(H2)对反应N2(g) + 3H2(g)  2NH3(g)+Q(Q>0)的影响如右图所示。下列说法正确的是
2NH3(g)+Q(Q>0)的影响如右图所示。下列说法正确的是
A.反应在b点达到平衡
B.b点H2的转化率最高
C.c点N2的转化率最高
D.a、b、c三点的平衡常数Kb > Ka > Kc
参考答案:C
本题解析:增大氢气的浓度,平衡向正反应方向移动,但氢气的转化率是降低的,氮气的转化率是提高的,所以图像中氮气转化率最高的应该是氢气的量最大时的点为C点。由于温度不变故平衡常数是相同的。
本题难度:一般
4、计算题 (18分)(1)1 mol O2与足量氢气反应产生水蒸气放热483.6 kJ,若1 g水蒸气转化成液态水放热2.444 kJ,请写出表示氢气燃烧热的热化学方程式:__________________________________。
(2)由汽油裂解得到乙烯、丙烯是重要的化工原料,请写出下列转化的方程式,并注明反应类型。
丙烯? → 聚丙烯
___________________________________________________?
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N2 2mol 、H21.5mol、NH32mol。则用氮气浓度的减少来表示该反应速率为__________ 。
(4)在500ml密闭容器中,将2mol A和1molB混合加热到500℃,达到平衡
2 A(g) +B (g) 3C(g)?K = 16求A转化为C的转化率为__________。
3C(g)?K = 16求A转化为C的转化率为__________。
(5) 在密闭容器中发生下列反应:aA(g)  cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a? _______ c+d(填“>”、“=”或“<”)。
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a? _______ c+d(填“>”、“=”或“<”)。
(6) 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,反应的化学方程式为______________________________________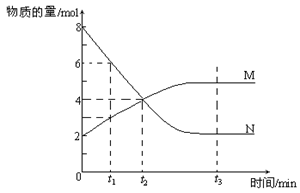
参考答案:H2(g)+1/2O2(g)===H2O(l)?ΔH=-285.8 kJ・mol-1
0.125mol/(L.S)? 57.1%? <? 2N M
M
本题解析:(1)燃烧热是指再一定条件下,1mol可燃物完全燃烧,生成稳定的氧化物时所放出的热量,根据题意可知,1mol氢气完全燃烧生成水蒸气时放出的热量是483.6 kJ÷2=241.8 kJ。又因为1 g水蒸气转化成液态水放热2.444 kJ,所以18g水蒸气转化为液态水放出的热量是2.444 kJ×18=44kJ,所以氢气的燃烧热是(241.8+44)kJ/mol,则相应的热化学方程式为H2(g)+1/2O2(g)===H2O(l)?ΔH=-285.8 kJ・mol-1。
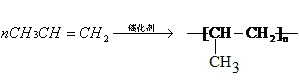
(2)丙烯中含有碳碳双键,能发生加聚反应,方程式为 。
。
(3)生成氨气是2mol,则消耗氮气是1mol,所以氮气的反应速率是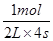 =0.125mol/(L.S)。
=0.125mol/(L.S)。
(4)? 2 A(g) +B (g) 3C(g)?
3C(g)?
起始浓度(mol/L)? 4? 2? 0
转化浓度(mol/L)? 2x? x? 3x
平衡浓度(mol/L)? 4-2x? 2-x? 3x
所以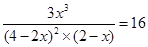
解得x=1.142
因此转化率是1.142÷4×100%=57.1%。
(5)将气体体积压缩到原来的一半的瞬间,A的浓度为原平衡的2倍,但平衡时A的浓度为原平衡的2.1倍,说明增大压强平衡向逆反应方向移动,所以a小于 c+d。
(6)根据图像可知,反应进行到t1时,N减少了2mol,M增加1mol,所以根据变化量之比是相应的化学计量数之比可知,方程式为2N M。
M。
本题难度:一般
5、选择题 汽车尾气的无害化处理已成为当今汽车工业的一项重要课题,其基本原理是实现2NO(g)+2CO(g) ?N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是(?)
?N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是(?)
A.只要使用合理的催化剂及载体,就可完全清除NO和CO
B.该反应达到平衡时v(NO)正=v(CO)逆
C.假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO)
D.使用性能好的催化剂可使反应的平衡常数增大
参考答案:B
本题解析:催化剂只能改变反应速率,但不能改变平衡状态,A不正确;平衡时正逆反应速率相等,但各种物质的浓度不一定是相等的,B正确,C不正确;平衡常数只与温度和化学计量数有关系,而与是否使用催化剂无关,D不正确,答案选B。
点评:关于催化剂需要注意的是,催化剂能够降低反应的活化能,增大单位体积内活化分子的百分数,从而加快反应速率。但不能影响平衡状态,同时也不能影响反应热和平衡常数。
本题难度:一般