|
�߿���ѧ���⡶���ʽṹ��Ԫ�������ɡ�����ǿ����ϰ��2017�����°棩(��)
2017-08-10 01:55:30
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ͼ��a��b��c��d��e��f��ʾԪ�����ڱ��в��ֶ�����Ԫ�أ�����������ȷ���ǣ�������
A��a��b��c�ļ������У�c�����Ӱ뾶���
B��c��d��f����������Ӧ��ˮ��������֮����ɷ�����Ӧ
C��e���⻯���f���⻯����ȶ��Ը�
D��a��e���γ�һ���������ǽ�������--���½ṹ�մ�
| 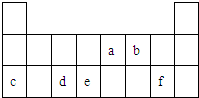
�ο��𰸣�a��b��c��d��e��f�Ƕ�����Ԫ�أ��ɸ�Ԫ����Ԫ�����ڱ���λ�ÿ�֪��aΪ��Ԫ�ء�bΪ��Ԫ�ء�c��Ԫ�ء�dΪ��Ԫ�ء�eΪ��Ԫ�ء�fΪ��Ԫ�أ�
A��aΪ��Ԫ�ء�bΪ��Ԫ�ء�c��Ԫ�أ�ԭ���γɵ����ӵ��Ӳ�ṹ��ͬ�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС������a��b��c�ļ������У�c�����Ӱ뾶��С����A����
B��c��Ԫ�ء�dΪ��Ԫ�ء�fΪ��Ԫ�أ�����������Ӧ��ˮ����Ϊ�������ơ����������������ᣬ��������������������������������ơ���������Һ����������������ᷢ���кͷ�Ӧ����B��ȷ��
C��eΪ��Ԫ�ء�fΪ��Ԫ�أ��ǽ�����Si��Cl���ǽ�����Խǿ���⻯��Խ�ȶ�������f���⻯����ȶ��Ըߣ���C����
D��aΪ��Ԫ�ء�eΪ��Ԫ�أ���������һ���������ǽ�������--���½ṹ�մɣ���D��ȷ��
��ѡBD��
���������
�����Ѷȣ�һ��
2������� ijԪ��ԭ�ӵļ۵��ӹ���Ϊ3d54s1�������ڵ������ڣ�d��Ԫ�أ���������ϼ�Ϊ_________��Ԫ�ط���
��_________��
�ο��𰸣�+6��Cr
���������
�����Ѷȣ�һ��
3��ѡ���� ���и����е����ʱȽϣ���ȷ����
A.����HClO4>HBrO4>HIO4
B.����NaOH>Mg(OH)2>Ca(OH)2
C.�ȶ��ԣ�HI>H2S> HCl
D.�����ԣ�Na+>Mg2+>Al3+
�ο��𰸣�A
���������ͬ�������϶��½���������ǿ���ǽ�����������ͬ�����������ң��������������ǽ���������ǿ��������Խǿ������������ˮ����ļ���Խǿ����Ӧ�����ӵ�������Խ��������BD����ȷ���ǽ�����Խǿ������������ˮ���������Խǿ����Ӧ�⻯����ȶ���Խǿ������A��ȷ��C����ȷ����ѡA��
�����Ѷȣ�����
4������� ����������߿���ÿһ�С�ÿһ���൱�����ڱ���ÿһ���ÿһ���ڣ�����������������������Ԫ�����ڱ���������������߿�����ʵ�������ڱ���һ���������ڵ�������������������ǽ����ķֽ��ߣ�
��X��Y��Z��M��NΪ�����ڵ���������Ԫ�أ�����X��Zͬ���壬Y��Zͬ���ڣ�M��X��Y�Ȳ�ͬ�壬Ҳ��ͬ���ڣ�Xԭ�������������Ǻ�����Ӳ�����������Y������ϼ�������ͻ��ϼ۵Ĵ����͵���6��N�Ƕ���������Ԫ����ԭ�Ӱ뾶���ķǽ���Ԫ�أ�
��1����д������Ԫ�ص�Ԫ�ط��ţ�X______��Y______��M______��
��2����д�����з�Ӧ�����ӷ���ʽ��N������NaOH��Һ��Ӧ��______��
��3��Y��Z��ȣ��ǽ����Խ�ǿ��Ԫ����______������֤���ý��۵�ʵ���ǣ������ӷ���ʽ��ʾ��______��
�ο��𰸣�����Ԫ�����ڱ��Ľṹ�Լ�Ԫ�صķֲ������������Ϊ��

��1�����������ƶ�XΪ��Ԫ�أ�ZΪSԪ�أ�X�ڵڶ����ڣ�Y��Zͬ���ڣ�Y�ڵ������ڣ���Mֻ��ΪHԪ�أ�Y������ϼ�����ͻ��ϼ۴�����Ϊ6��������ϼ�Ϊa����������ϼ�Ϊa-8����a+��a-8��=6������a=7����YΪClԪ�أ�NΪ�������ڰ뾶���ķǽ���Ԫ�أ���NΪSi���ʴ�Ϊ��O��Cl��H��
��2�����ܺ��������Ʒ�Ӧ���ɹ����ƺ�������ʵ���ǣ�Si+2OH-+H2O�TSiO32-+2H2�����ʴ�Ϊ��Si+2OH-+H2O�TSiO32-+2H2����
��3��ͬ����Ԫ�ص�ԭ�ӣ������ң�Ԫ�صķǽ���������ǿ������S��Cl�Ƚϣ��ǽ����Խ�ǿ��Ԫ��Cl�������ܽ������û�������Cl2+S2-�T2Cl-+S�����ʴ�Ϊ��Cl2+S2-�T2Cl-+S����
���������
�����Ѷȣ�һ��
5��ѡ���� �������Ӱ뾶֮��С��1����
A.r (Na+)/ r (Na)
B.r (Cl-)/ r (Cl)
C.r (Na)/ r (Mg)
D.r (Ca)/ r (Mg)
�ο��𰸣�A
���������ͬ��Ԫ�ص������Ӱ뾶С��ԭ�Ӱ뾶������A��ȷ��ͬ��Ԫ�ص������Ӱ뾶����ԭ�Ӱ뾶��B����ȷ��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶������CD���Dz���ȷ�ģ���ѡA��
�����Ѷȣ���
| 