��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и������ʣ���������ԭ��Ӧ��ͨ��ֻ����Ϊ������ʹ�õ��ǣ�������
A��SO2
B��H2SO4
C��Cl2
D��FeCl2
�ο��𰸣�C
���������A��SO2��SԪ��Ϊ+4�ۣ������м��̬���ڷ�Ӧ�мȿ����������ֿ�����ԭ������A��ѡ��
B��H2SO4��SԪ��Ϊ+6�ۣ�������ۣ�����������ԭ��Ӧ��ͨ��ֻ����Ϊ����������B��ѡ��
C��Fe��HԪ��Ϊ0�ۣ��ڷ�Ӧ���ϼ����߱�����ֻ����ԭ������ѡC��
D��FeCl2��FeԪ��Ϊ+2�ۣ������м��̬���ڷ�Ӧ�мȿ����������ֿ�����ԭ������D��ѡ��
��ѡC��
�����Ѷȣ���
2������� ���з�Ӧ�У�HCl����ԭ�����ǣ�������
A��NaOH+HCl�TNaCl+H2O
B��Zn+2HCl�TZnCl2+H2��
C��MnO2+4HCl��Ũ��
MnCl2+2H2O+Cl2��
D��CuO+2HCl�TCuCl2+H2O
�ο��𰸣�A��NaOH+HCl�TNaCl+H2O��Ӧ�У���Ԫ�ػ��ϼ۲��䣬����HCl���ǻ�ԭ������A����
B��Zn+2HCl�TZnCl2+H2����Ӧ�У���Ԫ�صĻ��ϼ۲��䣬��Ԫ�صĻ��ϼ۽��ͣ�����HCl������������B����
C��MnO2+4HCl��Ũ��?��?.?MnCl2+2H2O+Cl2����Ӧ�У���Ԫ�صĻ��ϼ����ߣ���Ԫ�صĻ��ϼ۲��䣬����HCl�ǻ�ԭ������C��ȷ��
D��CuO+2HCl�TCuCl2+H2O��Ӧ�У���Ԫ�صĻ��ϼ۲��䣬��Ԫ�صĻ��ϼ۲��䣬����HCl���ǻ�ԭ������D����
��ѡC��
���������
�����Ѷȣ�һ��
3������� ������������ȷ���ǣ�������
A����X��ΪX2-�ķ�Ӧ��������Ӧ
B�����е��ʲ���Ļ�ѧ��Ӧ��һ����������ԭ��Ӧ
C���������ܷ���������Ӧ������������
D����Ӧ��ijԪ�ص�ԭ�ӱ�Ϊ�����ӣ����Ԫ�صĵ����ڷ�Ӧ��һ���ǻ�ԭ��
�ο��𰸣�A��X��ΪX2-��Ԫ�صĻ��ϼ۽��ͣ�X����ԭ����A����
B���е��ʲ���Ļ�ѧ��Ӧ����һ����������ԭ��Ӧ����ͬ��������֮���ת������B����
C���������ܵ����H+�����������ԣ���C��ȷ��
D��ijԪ�ص�ԭ�ӱ�Ϊ�����ӣ�Ԫ�صĻ��ϼ����ߣ��ڷ�Ӧ����ԭ�������ã���D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
4��ѡ���� ����������ԭ��Ӧ��Fe2O3+2Al�TAl2O3+2Fe������˵����ȷ���ǣ�������
A��Fe2O3������
B��Al2O3��������
C��Fe����������
D��Al���л�ԭ��
�ο��𰸣�A����Ӧ����Ԫ�صĻ��ϼ۽��ͣ���Fe2O3����ԭ����A����
B����Ӧ����Ԫ�صĻ��ϼ����ߣ�Al����ԭ����Al2O3�����������B����
C����Ӧ����Ԫ�صĻ��ϼ۽��ͣ���Fe2O3����������Fe�ǻ�ԭ�����C����
D����Ӧ����Ԫ�صĻ��ϼ����ߣ�Al����ԭ������Al���л�ԭ�ԣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ���
5��ѡ���� ���е���˫���ŵı�ʾ��������ȷ���ǣ�������
A��

B��
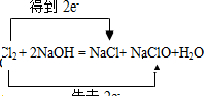
C��

D��
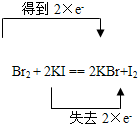
�ο��𰸣�A����Ԫ�صĻ��ϼ����ߣ���Ԫ�صĻ��ϼ۽��ͣ�����ʧȥ���ӣ�ת�Ƶĵ�����Ϊ2e-����A��ȷ��
B���÷�Ӧ��ClԪ�صĻ��ϼۼ������ֽ��ͣ�ת�Ƶĵ�����Ϊe-����ȷ�ı�ʾΪ
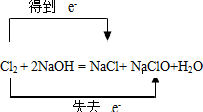
����B����
C���÷�Ӧ����ʧȥ���ӣ���õ����ӣ�ת�Ƶĵ�����Ϊ2e-����C��ȷ��
D���÷�Ӧ�е�ʧȥ���ӣ���õ����ӣ�ת�Ƶĵ�����Ϊ2e-����D��ȷ��
��ѡB��
���������
�����Ѷȣ���