微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X元素的阳离子与Y元素的阴离子具有与氩原子相同的电子层结构.下列各项的大小比较中,正确的是( )
A.X、Y的原子序数:X<Y
B.X、Y的原子最外层电子数:X>Y
C.X、Y的原子半径:X>Y
D.X的阳离子与Y的阴离子半径:X>Y
参考答案:X元素的阳离子与Y元素的阴离子具有与氩原子相同的电子层结构,则X为第四周期的金属元素,Y为第三周期的非金属元素,
A.第四周期元素的原子序数大,则原子序数为X>Y,故A错误;
B.非金属元素的最外层电子数大于4,金属元素的最外层电子数小于4,则原子最外层电子数为X<Y,故B错误;
C.电子层越多,原子半径越大,则X、Y的原子半径为X>Y,故C正确;
D.具有相同电子排布的离子,原子序数大的离子半径小,则X的阳离子与Y的阴离子半径为X<Y,故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
A.X的原子序数比Y的小
B.X原子的最外层电子数比Y的大
C.X的原子半径比Y的大
D.X元素的最高正价比Y的小
参考答案:CD
本题解析:
本题难度:简单
3、填空题 某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是
________________。
参考答案: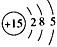
本题解析:
本题难度:一般
4、填空题 A、B、C、D、E、F六种短周期元素,原子序数依次增大,A、E同主族,D、F同主族,A元素的原子半径是所有原子中最小的,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)F元素在周期表中的位置______,在以上元素最高价氧化物的水化物中,碱性最强的化合物的电子式是:______.
(2)D、F的气态氢化物,沸点较高的是______(填分子式).
(3)A单质与C单质在一定条件下可化合为Z,常温下,向pH=a的Z的水溶液中加入等体积pH=b的X的水溶液,且a+b=14,充分作用后,溶液pH______7(填“>”“<”或“=”),原因是______.
参考答案:A元素的原子半径是所有原子中最小的,则A为氢元素;B元素原子的最外层电子数是内层电子数的2倍,则B为碳元素;C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,Y为硝酸铵,则C为氮元素;A、B、C、D、E、F六种短周期元素,原子序数依次增大,A、E同主族,则E为钠元素;D、F同主族,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物,则D为氧元素,F为硫元素;
(1)硫原子有3个电子层,最外层电子数为6,则在周期表中第三周期第ⅥA族,只有钠为金属,则氢氧化钠的碱性最强,其电子式为
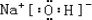
,
故答案为:第三周期第ⅥA族;
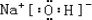
;
(2)因D、F的气态氢化物分别为H2O、H2S,水分子之间含有氢键,则沸点高,故答案为:H2O;
(3)A单质与C单质在一定条件下可化合为Z,则Z为氨气,pH=a的氨水溶液中加入等体积pH=b的硝酸的水溶液,且a+b=14,则反应后为氨水和硝酸铵的混合溶液,溶液pH>7,弱电解质的电离大于盐类的水解,故答案为:>;弱碱与盐的混合溶液真弱碱的电离大于盐中弱碱阳离子的水解.
本题解析:
本题难度:一般
5、填空题 在周期表主族元素中,甲元素与乙、丙、丁三元素上下或左右紧密相邻.甲、乙两元素的原子序数之和等于丙元素的原子序数.这四种元素原子的最外层电子数之和为20.据此可以判断:元素甲为______,元素丙为______,元素乙和丁所形成化合物的分子式为______.
参考答案:甲、乙两元素的原子序数之和等于丙元素的原子序数.若甲、丙同周期,其原子序数之差为1,乙只能是氢元素,由甲与乙、丙、丁在元素周期表中的位置关系可知,乙为氢元素,不符合四元素原子最外层电子数之和为20.所以甲,丙必同主族,故原子序之差为2或8,四种元素不可能为氢和氦,则排除原子序数之差为2,甲、丙原子序之差为8,乙元素原子序数应为8,乙为氧元素,甲为氮元素,丙为磷元素,丁为碳元素.
元素乙和丁所形成化合物的分子式为CO、CO2.
故答案为:N;P;CO、CO2.
本题解析:
本题难度:简单