微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后,再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。下列说法中错误的是
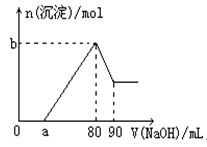
A.盐酸的体积为80mL
B.a的取值范围为0<a<50
C.n(Mg2+)<0.025mol
D.当a值为30时,b值为0.01
参考答案:D
本题解析:根据图像可知,加入氢氧化钠后并没有立即产生沉淀,说明盐酸是过量的,加入的氢氧化钠首先是中和过量的盐酸,当盐酸被中和之后,继续加入氢氧化钠,开始产生氢氧化镁和氢氧化铝沉淀。当沉淀不再发生变化时,继续加入氢氧化钠,此时氢氧化铝开始溶解,直至沉淀不再变化为止。根据图像可知,当沉淀达到最大值时,溶液恰好是氯化钠溶液,根据原子守恒可知氯化钠的物质的量就是加入的氢氧化钠的物质的量,即1mol/L×0.08L=0.08mol,所以盐酸的体积是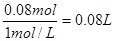 。根据图像可知,溶解氢氧化铝消耗的氢氧化钠是10mol,所以根据方程式得到,氢氧化铝的物质的量是1mol/L×0.01L=0.01mol。而产生0.01mol氢氧化钠需要消耗的氢氧化钠溶液的体积是30ml,因为还有氢氧化镁生成,所以80ml-a>30ml,则a<50ml。若a=0时,说明在80ml的氢氧化钠溶液中有50ml是来产生氢氧化镁的,所以氢氧化镁的物质的量最多不能超过
。根据图像可知,溶解氢氧化铝消耗的氢氧化钠是10mol,所以根据方程式得到,氢氧化铝的物质的量是1mol/L×0.01L=0.01mol。而产生0.01mol氢氧化钠需要消耗的氢氧化钠溶液的体积是30ml,因为还有氢氧化镁生成,所以80ml-a>30ml,则a<50ml。若a=0时,说明在80ml的氢氧化钠溶液中有50ml是来产生氢氧化镁的,所以氢氧化镁的物质的量最多不能超过
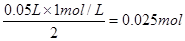 。若a=30,则产生氢氧化镁的氢氧化钠溶液的体积是80ml-30ml-30ml=20ml,所以氢氧化镁的物质的量是
。若a=30,则产生氢氧化镁的氢氧化钠溶液的体积是80ml-30ml-30ml=20ml,所以氢氧化镁的物质的量是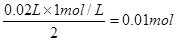 ,所以此时沉淀的物质的量是0.01mol+0.01mol=0.02mol,因此错误的选项是D,答案选D。
,所以此时沉淀的物质的量是0.01mol+0.01mol=0.02mol,因此错误的选项是D,答案选D。
本题难度:一般
2、选择题 1.6g Cu与50mL 8mol・L―1的HNO3溶液充分反应,HNO3的还原产物有NO和NO2,反应后测得溶液中H+浓度为a mol・L―1(生成水的体积忽略不计),则此时溶液中所含NO3-的物质的量为
A.(a+1)mol
B.(0.4+0.05a)mol
C.(a+0.05)mol
D.0.05(a+1)mol
参考答案:D
本题解析:略
本题难度:一般
3、选择题 标准状况下VL氨气溶解在1L水中(水的密度近似为1g・mL-1),所得溶液的密度为ρg・mL-1,质量分数为ω,物质的量浓度为cmol・L-1,则下列关系中不正确的是
[? ]
A.ρ=(17V+22400)/(22.4+22.4V)
B.ω=17c/1000ρ
C.ω=17V/(17V+22400)
D.c=1000Vρ/(17V+22400)
参考答案:A
本题解析:
本题难度:一般
4、选择题 在一定条件下,使CO和O2的混合气体26 g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14 g,则原混合气体中O2和CO的质量比可能是(?)?
A.9∶4
B.1∶1
C.7∶6
D.6∶7
参考答案:D
本题解析:由反应2Na2O2+2CO2=2Na2CO3+O2,可知混合物在常温下跟足量的Na2O2固体反应生成固体为Na2CO3,1molNa2O2生成1molNa2CO3,质量增加28g,恰好为CO的质量,固体增重14g,说明混合气体中CO为14g,则O2为26g-14g=12g,所以原混合气体中O2和CO的质量比为
12g:14g=6:7,,故本题的答案选择D。
点评:本题考查了混合物的相关计算,该题需要一定的观察能力,本题难度中等。
本题难度:简单
5、选择题 在标况下,0.56g某气体的体积为448 mL,则该气体的相对分子质量为(?)
A.2
B.56
C.0.028
D.28
参考答案:D
本题解析:标准状况下,448ml气体的物质的量是0.448L÷22.4L/mol=0.02mol。则根据m=M・n可知,M=0.56g÷0.02mol=28g/mol,所以该气体的相对分子质量为为28,答案选D。
点评:该题是基础性试题的考查,试题注重基础,侧重能力的培养。该类试题学生需要明确的是在进行物质的量的有关计算时,关键是熟练应用几个关系式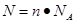 、n=m/M、
、n=m/M、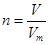 、
、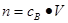 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
本题难度:一般