��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����¶ȣ��������ݲ�һ���������?
A����ѧ��Ӧ����v
B��ˮ�����ӻ�����Kw
C����ѧƽ�ⳣ��K
D������ĵ���ƽ�ⳣ��Ka
�ο��𰸣�C
������������ڷ�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ����ȷ�������������¶Ȼ�ѧƽ�ⳣ����һ��������ģ��������¶ȷ�Ӧ����һ�������������ȵģ���������¶�ˮ�����ӻ������͵���ƽ�ⳣ������һ������ģ���ѡC��
�����������Ǹ߿��еij������ͣ����������ǿ��ע�ؿ���ѧ�������Ӧ����������������������ѧ���ķ�ɢ˼ά���������ѧ���Ĵ���Ч�ʡ�
�����Ѷȣ���
2��ѡ���� һ�������£����淴ӦN2+3H2?2NH3 ��H=-92.4KJ/mol���йظ÷�Ӧ��������ȷ���ǣ�������
A���������ܼӿ�����Ӧ����v������Ӱ��v�棬���������˷�Ӧ��ƽ�������ʱ��
B����lmolN2��3molH2��ַ�Ӧ�ﵽƽ��ʱ���ų�����������92.4kJ
C����c��N2����c��H2����c��NH3��=1��3��2ʱ����Ӧ�ʹﵽƽ��״̬
D��ƽ��ʱ��������Ũ�ȣ�����ƽ��ʱN2ת���ʼ�С��H2ת��������
�ο��𰸣�A����������ͬ�ȳ̶ȵ��������淴Ӧ���ʣ����̷�Ӧ����ƽ���ʱ�䣬��A����
B���÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ����ȫת��Ϊ��������Էų�������С����92.4kJ����B����
C������Ӧ�ﵽƽ��״̬ʱ�������ʵ�Ũ�Ȳ��䣬����c��N2����c��H2����c��NH3��=1��3��2ʱ����Ӧ��һ���ﵽƽ��״̬�����뷴Ӧ��ij�ʼŨ�Ⱥ�ת�����йأ���C����
D��ƽ��ʱ����������Ũ�ȣ�ƽ��������Ӧ�����ƶ������������������ת���ʣ���������ת���ʼ�С����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� һ���¶��£������Ϊ?VL?���ܱ������м���1molX��1molY�������·�Ӧ��X��g��+Y��g?���T2Z��g?��+W��s������H��0�ﵽƽ�⣬�����ж���ȷ���ǣ�������
A����ƽ�������м�������W�������淴Ӧ���ʾ�����
B��ƽ������X��������Ӧ�ġ�H����
C���¶Ȳ��䣬�������������Ϊ2VL��Z��ƽ��Ũ�ȱ�Ϊԭ����
D���������л�������ѹǿ����ʱ������֤���˷�Ӧ�Ѵﵽƽ��״̬
�ο��𰸣�A�����ӹ������ٹ�������������Ũ�Ȳ��䣬��Ӧ���ʲ��䣬��A����
B�����Ȼ�ѧ����ʽ�У���Ӧ��Ϊ��ֵ���뷴Ӧ��Ķ����أ���B����
C�����巴Ӧ��Ļ�ѧ��������������������Ļ�ѧ���������ı�Խǿ��ƽ�ⲻ�ƶ������Խ������������Ϊ2VL��Z��ƽ��Ũ�ȱ�Ϊԭ����12����C��ȷ��
D�����巴Ӧ��Ļ�ѧ��������������������Ļ�ѧ��������Խǿ��Ӱ��ƽ���ƶ��������۷�Ӧ�Ƿ�ﵽƽ��״̬�������л�������ѹǿ�����䣬��D����
��ѡC��
���������
�����Ѷȣ�һ��
4������� ��6�֣���ע������������NO����N���ϣ��Ļ�����壬�������·�Ӧ(��ͼ2��13��ʾ)

ͼ2��13
2NO�����磩 �Σ���4��g)
����4��g)
(1)������Ѹ��������ʱ���������ɫ�ȱ�_________�����_________�����պ������ȣ�_________���
(2)������Ѹ��������ʱ���������ɫ�ȱ�_________�����_________�����պ������ȣ�_________���
�ο��𰸣�(1)dz?��?���? (2)��?dz?����
���������������˼ά����(1)Ѹ����������˲�䣬ƽ����δ�����ƶ�����ʱ��λ����ڵ�NO2������Ŀ��С������������ɫ��dz���ݻ���������ѹǿ��С��ƽ�����淴Ӧ����(����NO2�ķ���)�ƶ�����λ����ڵ�NO2���������࣬������ɫ�����ʱ������NO2����������࣬��Ũ�Ȳ�����ʼʱ����ɫ������ʼʱ�
(2)Ѹ�������Ƶ�˲�䣬ƽ����δ�����ƶ�����ʱ����λ����ڵ�NO��������Ŀ���࣬������ɫ����ݻ���С������ѹǿ����ƽ��������Ӧ����(����N����4�ķ���)�ƶ���NO2������Ŀ���٣�������ɫ��dz�����ȳ�ʼʱҪ�
�����Ѷȣ���
5������� �Ѵ����е�����̬�ĵ�ת��Ϊ���Ļ�����Ĺ��̳�Ϊ�̵�������̵��ʹ����̵�������ʱN2ת��ΪNO��������Ȼ�̵�����Զ���������������Ҫ����ҵ�̵����ϳɰ�����Ŀǰ�˹��̵�����Ҫ�������йش����̵���ҵ�̵���ƽ�ⳣ��Kֵ�ֱ����±�һ�ͱ�����
��һ��N2+ O2?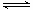 ?2NO?
?2NO?
�¶�
| 27��
| 2000��
|
Kֵ
| 3��84��10��31
| 0��1
|
?
������N2+ 3H2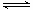 2NH3?
2NH3?
�¶�
| 25��
| 350��
| 400��
| 450��
|
Kֵ
| 5��108
| 1��847
| 0��507
| 0��152
|
��1�������ϱ��е����ݷ���������˵����ȷ����_________��
A��N2+ O2?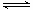 ?2NO�����ȷ�Ӧ
?2NO�����ȷ�Ӧ
B��������ģģ������̵���û�������
C���ڳ����£����ӹ�ҵ�̵���������ѹǿ��Kֵ�ᷢ���ı�
D����ҵ�̵��Ƿ��ȷ�Ӧ
��2����ij�ܱ������м���4 mol NH3��1��2 mol H2��һ������N2�������壬һ�������·�����Ӧ�������ʵ�Ũ����ʱ��仯���ͼ��ʾ[��֪0��t1�α��ֺ��¡����ݣ���c(N2)δ����]����ͼΪt2ʱ�̺�ı䷴Ӧ��������Ӧ������ʱ��ı仯�������֪��t2��t3��t4��t5ʱ�̸��ı�һ�ֲ�ͬ��������
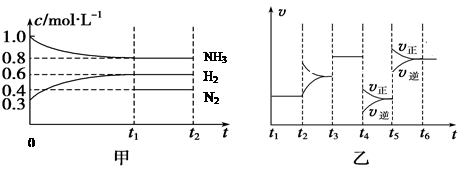
����t1="15" s����t0��t1�εķ�Ӧ����Ϊv(H2)=������
��N2����ʼ���ʵ���Ϊ����������
�۷�Ӧ�ﵽƽ��״̬������˵�����ܱ����Ѵﵽƽ��״̬����?
A����λʱ��������a molN2��ͬʱ����3a mol H2?B����������ѹǿ���ٱ仯
C�����������ܶȲ��ٱ仯? D������H��H �����ѵ�ͬʱ������H��N������
��t4ʱ�̸ı������Ϊ����?��������t5ʱ�̸ı������Ϊ��������?��
����֪t0��t1�θ÷�Ӧ�ų������յ�����ΪQ kJ(QΪ��ֵ)����д���÷�Ӧ���Ȼ�ѧ����ʽ��____________________________________________________________________
�ο��𰸣���1��ABD��2�֣�
��2����0��02mol/(L��s)?��1��2mol ����1�֣�?��BD��2�֣�?�ܼ�Сѹǿ?����?�¶ȣ���1�֣� ��2NH3(g)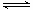 N2 (g)+ 3H2(g)?��H=+2��5QkJ/mol��2�֣�
N2 (g)+ 3H2(g)?��H=+2��5QkJ/mol��2�֣�
�����������1��A���ӱ�һ���Կ����������¶ȵ����ߣ�Kֵ���������������ȵķ�����ȷ��B���ӱ�һ���ݻ����Կ�������ʹ�����ߵ�2000�� ����������������һ��������ƽ�ⳣ��Ҳֻ�ﵽ0��1�����Ƕ����˹��ϳɰ���˵��������25�� ����ƽ�ⳣ��Ҳ�ﵽ��5��108������������ģģ������̵���û������ģ�����˵����ȷ��C��Kֵֻ���¶ȵĸı���ı䣬����ѹǿ�ĸı���ı䣬����D���ӱ������Կ������¶�Խ�ߣ�ƽ�ⳣ��ԽС������������һ�����ȵķ�����ȷ��
��2����Ӧ������ָ��λʱ����Ũ�ȵĸı�������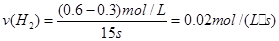
�ڴ�ͼ�п��Լ���������������Ϊ��4L��
��Ϊ��ѧ��Ӧ���ʵıȵȻ�ѧ������֮�ȣ���ˣ�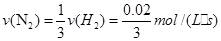
��ôN2����ʼ���ʵ���Ϊ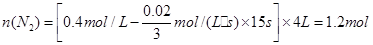 ?
?
��A����λʱ��������a molN2��ͬʱ����3a mol H2�����ֹ�ϵ����ƽ�����һֱ���ڣ�������Ϊ�ﵽƽ��ı�־������B�������ֽ����ɵ�������������һ���������ķ�Ӧ��������������ѹǿ���ٱ仯ʱ����ζ�ŷ�Ӧ�ĸ����ʵ����Ѳ�����ʱ��ĸı���ı䣬���ﵽƽ��״̬����ȷ��C����B�͵���һ������ȷ��D������H��H �����ѵ�ͬʱ������H��N�����ѣ����ֹ�ϵ��ʼ�մ��ڵģ�����ƽ�����
��t4ʱ�����淴Ӧ���ʶ���С�����淴Ӧ���ʼ�С�ij̶ȴ���ƽ�������ƶ��������������Ⱥ��������ķ������ֻ���Ǽ�Сѹǿ��t5ʱ�����淴Ӧ���ʶ����ڣ�������Ӧ��������ij̶ȴ���ƽ�������ƶ��������������Ⱥ��������ķ������ֻ���������¶ȡ�
��2NH3(g)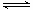 N2 (g)+ 3H2(g)?��H=+2��5QkJ/mol��2�֣���
N2 (g)+ 3H2(g)?��H=+2��5QkJ/mol��2�֣���
�����Ѷȣ�һ��