��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��֪Cl-��Ag+��Ӧ����AgCl��ÿ�������ɵ�AgCl������10%����ֽ�ɵ������������������ֿ���ˮ��Һ��᪻���HClO3��Ϊǿ�ᣩ��HCl�����������ɵ�Cl-����ʣ���Ag+�������ɳ��������ѭ��������ֱ�����ա����к�1.1molNaCl����Һ�������м�������AgNO3�������������ɶ��ٿ������AgCl��Ag�����������Һ���Ϊ1L������Һ��H+���ʵ���Ũ���Ƕ��٣�
�ο��𰸣�167.94g? 0.12mol/L
��������������漰��������Ӧ��Ag++Cl-=AgCl��,2AgCl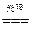 2Ag+Cl2��3Cl2+3H2O=6H++ClO3��+5Cl-��
2Ag+Cl2��3Cl2+3H2O=6H++ClO3��+5Cl-��
���Т�60Ag++60Cl-=60AgCl����Ӧ�Т�6AgCl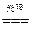 6Ag+3Cl2����3Cl2+3H2O=ClO3��+5Cl��+6H+����ȥѭ�������������ܷ�Ӧʽ��⣬��+��+�۵ã�60Ag++55Cl-+3H2O=54AgCl��+6Ag��+ClO3-+6H+��
6Ag+3Cl2����3Cl2+3H2O=ClO3��+5Cl��+6H+����ȥѭ�������������ܷ�Ӧʽ��⣬��+��+�۵ã�60Ag++55Cl-+3H2O=54AgCl��+6Ag��+ClO3-+6H+��
�ݴ��ã�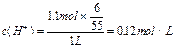 ��
��
������AgCl��Ag��������
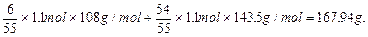
�����Ѷȣ�һ��
2��ʵ���� ��ͼ��һ����ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�á�

��l��A����������װ�ã�д�����еĻ�ѧ��Ӧ����ʽ?��
��2��a����������Ϊ??��
��3��ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�����K����������������װ�ã��ٵ�ȼD���ƾ��ƣ�������Eװ�á�Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ���Ӧ����ΪCO2��HC1��д��D�з�Ӧ�Ļ�ѧ����ʽ??��װ��C��������??��
��4����E������©����������л���ɫ������ɫʯ����Һ����ɫ�仯Ϊ??��
��5������E���ձ�����Һ��Ϊ����ʯ��ˮ����Ӧ����������Ϊ???������ţ���
���а�ɫ�������ɣ����ް�ɫ�������ɣ��������ɰ�ɫ�����������ɫ������ʧ��
��6��D����Ӧ��Ϻرջ���K����ȥ�ƾ��ƣ��������ȵ����ã�A������Cl2
��������װ��B�е�������??��������װ��B�и��������ԣ����ܵ�
ԭ����??������ԭ��ʱ���÷���ˮ��ʪ��ĵ⻯�ص�����ֽ�ȣ�����պ
��Ũ��ˮ�IJ��������ʱ�۲쵽�а��̲�����д����������ԭ��Ӧ�Ļ�ѧ����
ʽ???��
�ο��𰸣���1��MnO2+4HCl��Ũ�� MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��2��Բ����ƿ
��3��2Cl2+2H2O������+C  4HCl+CO2?����Cl2�е�HCl���壬�ṩD������ˮ����
4HCl+CO2?����Cl2�е�HCl���壬�ṩD������ˮ����
��4������ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ
��5����
��6��װ��B��ƿ��Һ���½�������©����Һ��������? A��Bװ��©��
3Cl2+8NH3�T6NH4Cl+N2
�����������l������װ�÷�����֪ʵ�����Ʊ��������ö������̺�Ũ������ȷ�Ӧ���ɣ���2�����������������жϣ�
��3��������ǿ�����ԣ�̼�л�ԭ�ԣ��ڼ���������������ˮ��̼����������ԭ��Ӧ���Ȼ������弫������ˮ����ˮ���ṩˮ�������ݴ˷�����
��4����ɫʯ����Һ�����죬����������Ư���ԣ��ݴ˷�����
��5���Ȼ��⡢������ͳ���ʯ��ˮ��Ӧ�����ɿ����Ե��κ�ˮ��
��6������Bװ���������ѹǿ�仯����Һ��仯��������װ��B�и��������ԣ�������A��Bװ��©���������Ͱ�����������Ũ��İ��̲��������ڱ����ᣬͬʱ����һ�ֳ��������嵥�ʣ�����Ϊ�Ȼ�李�����Ϊ������
�����Ѷȣ���
3��ʵ���� ij�о�С���Ʊ�����Һ����Ҫ�ɷ�ΪNaClO�������A��B����װ�á������ĵ��������ϣ����ڼ�������£�±�غͼ�Һ�������·�Ӧ��3X2+6OH-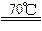 X-+
X-+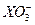 +3H2O����
+3H2O����
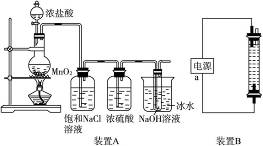
������������⣺
��1��װ��A�Ĵ��Թ��ڷ�����Ӧ�����ӷ���ʽΪ��____________________________��
��2��װ��A���ܷ�ʡȥʢ����NaCl��Һ��ϴ��ƿ�������ǣ�________________________��
��3��װ��A���ܷ�ʡȥʢŨ�����ϴ��ƿ�������ǣ�____________________________��
��4��װ��A���ܷ�ʡȥʢ��ˮ���ձ��������ǣ�____________________________��
��5��װ��B���Ʊ�ʱ�����ĵ�ⷴӦ�Ļ�ѧ����ʽΪ___________________��
��6��װ��B��a��Ӧ�ӵ�Դ�ļ��������ǣ�____________________________��
�ο��𰸣���1��Cl2+2OH-====Cl-+ClO-+H2O
��2�����ܣ������л��е�HCl���������Թ���Ҳ�������������Һ��Ӧ������NaClO�IJ����ʹ���
��3���ܣ�����ˮ���������Թ��в�Ӱ�췴Ӧ
��4�����ܣ�������ˮ�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ�¶�����ʱ����������Ӧ������NaClO3
��5��2NaCl+2H2O====H2��+Cl2��+2NaOH
��6����?������Cl2�ܳ�ֺ�����������Һ�Ӵ���������Ӧ
���������װ��A�����巢��װ�����Ʊ�Cl2�ģ���ӦΪMnO2+4HCl��Ũ��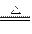 MnCl2+Cl2��+2H2O������ͨ������NaCl��Һ��Ϊ�˳�ȥCl2�е���������HCl��ͨ��ŨH2SO4��Ϊ�˸���Cl2��ͨ����ȴ��NaOH��Һ�������Ʊ�����ҺNaClO����ӦΪCl2+2NaOHNaCl+NaClO+H2O��
MnCl2+Cl2��+2H2O������ͨ������NaCl��Һ��Ϊ�˳�ȥCl2�е���������HCl��ͨ��ŨH2SO4��Ϊ�˸���Cl2��ͨ����ȴ��NaOH��Һ�������Ʊ�����ҺNaClO����ӦΪCl2+2NaOHNaCl+NaClO+H2O��
װ��B�����õ�ⱥ��ʳ��ˮ�����Ʊ�NaClO����ӦΪ2NaCl+2H2O 2NaOH+Cl2��+H2��,Cl2+2NaOH====NaCl+NaClO+H2O����a�������¶˵缫�ϲ���Cl2��Ϊ��������a�缫�ض�Ϊ������
2NaOH+Cl2��+H2��,Cl2+2NaOH====NaCl+NaClO+H2O����a�������¶˵缫�ϲ���Cl2��Ϊ��������a�缫�ض�Ϊ������
�����Ѷȣ���
4������� ��1���ڱ�״���£����������ʢ�4gH2����33.6LCH4�� ��1molH2O����3.01��1023��O2����
�к������������ǣ�����ţ���ͬ�� �� ��?�������������� ��?�������С���� ��?���ܶ��ɴ�С��˳��Ϊ����������������������
��2��ʵ���ҴӺ��壨����Ԫ�أ��Ե����ӵ���ʽ���ڣ�����ȡ����������£�

��֪2KI��Cl2��2KCl��I2������ܵ�Ŀ���ǴӺ�����л���Һ�з�������ʵ�ͻ����л���Һ��
I����ȡ��Ĺ������йص�ʵ��������ƣ����� ��?��
II��������ʵ��������A���ձ�? B��������? C��������? D����Һ©��? E���ƾ���
������б����õ����У�����ţ��� ��?����ȱ�ٵIJ����������� ��?��
III����ȡ��Ĺ����У�ѡ�õ���ȡ���������� ��?��
A�����Ȼ�̼?��?��B������?����? C���ƾ�? D������?
��3��д��ʵ������ȡ�����Ļ�ѧ����ʽ?��?��
�ο��𰸣���1���١��� ���� ���ۢܢڢ�
��2��I����ȡ����II��A B����©������III��A B��
��3��MnO2 + 4HCl(Ũ)  MnCl2 + Cl2��+2H2O
MnCl2 + Cl2��+2H2O
�����������
�����Ѷȣ���
5��ѡ���� ����˵������ȷ����(? )
A������̿��SO2��Na2O2����ʹƷ����Һ��ɫ����ԭ����ͬ
B��ͬ��ͬѹ�£�������ͬ���������ۣ��ֱ���������ϡ�����ϡ���ᷴӦ�������������������
C����SO2����ͨ��BaCl2��Һ�������ͣ�δ���������ɣ�����ͨ��NO2���г�������
D��������Cl2ͨ��NaBr��NaI�Ļ����Һ�У���Ӧ����Һ���ɲ�������գ�ʣ��Ĺ������ʳɷ�ΪNaCl
�ο��𰸣�B
�������������̿��SO2��Na2O2��ʹƷ����Һ��ɫ��ԭ��ֱ����������á�����Ư������Ư�ף�A��ȷ�����ݷ�ӦFe+H2SO4=FeSO4+H2���ɵã�����������ϡ���ᷴӦʱ��1 mol Fe��ȫ��Ӧ����1 mol H2�����ݷ�ӦFe+4HNO3=Fe(NO3)3+NO��+2H2O�ɵã�1 mol Fe��ȫ��Ӧ����1 mol NO�����߲�������������ȣ�B����Cѡ�NO2��ˮ��Ӧ����HNO3��HNO3�ܽ�SO2����ΪH2SO4��H2SO4��BaCl2��Ӧ����BaSO4������C��ȷ��Cl2ͨ��NaBr��NaI�Ļ����Һ������NaCl��Br2��I2�����ɲ��������ʱ��Br2�ӷ���I2������ʣ��NaCl��D��ȷ
�����Ѷȣ�һ��