| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《物质的量》高频试题预测(2017年最新版)(六)
参考答案:B 本题解析:A、摩尔质量表示单位物质的量的物质具有的质量,摩尔质量的常用单位是g/mol,A正确;B.气体摩尔体积表示单位物质的量的物质具有的体积,气体摩尔体积单位是L/mol,B错误;C.物质的量浓度表示单位体积的溶液中所含溶质的物质的量,单位为mol/L,C正确;D、物质的量表示微粒数目的集合体,常用单位为mol,D正确;选B。 本题难度:一般 2、选择题 配制物质的量浓度为0.1mol?L-1的Na2CO3溶液100 mL时,下列操作正确的是? 参考答案:B 本题解析:A、托盘天平的精确度为0.1g,不能用托盘天平称取1.06 g 无水碳酸钠,错误;B、在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水,正确;C、定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分,会使浓度偏低,错误;D、定容时,若仰视读数,则所配溶液的体积偏大,浓度将偏低,错误。 本题难度:一般 3、选择题 用NA?表示阿伏加德罗常数的值,下列说法正确的是 参考答案:B 本题解析:氮气与氢气的反应是可逆反应,所以不可能生成0.2NA个NH3,A错; 本题难度:一般 4、选择题 300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol/L Ba(OH)2溶液300 mL,反应后溶液中SO的物质的量浓度为( ) |
参考答案:D
本题解析:铝离子的物质的量是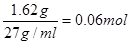 ,所以SO42-的物质的量是0.09mol。氢氧化钡的物质的量是0.03mol,因此反应后剩余SO42-的物质的量是0.06mol,其浓度是
,所以SO42-的物质的量是0.09mol。氢氧化钡的物质的量是0.03mol,因此反应后剩余SO42-的物质的量是0.06mol,其浓度是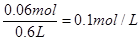 ,答案选D。
,答案选D。
本题难度:一般
5、选择题 向100 mL BaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的总物质的量和加入混合溶液B的体积关系如图所示: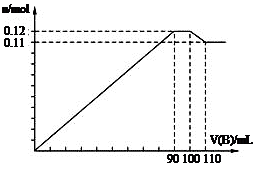
(1)当加入B溶液110 mL时,溶液中的沉淀是?。(填化学式)
(2)从90 mL至100 mL之间加入10 mLB溶液时,由图像纵坐标不变可知此段发生反应的离子方程式是:①?;②?;并由此可以分析出溶液B中Na2SO4与NaOH物质的量浓度之比为?。?
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为?mol/L;
A溶液中FeCl3物质的量浓度为?mol/L。
参考答案:(1)BaSO4、Fe(OH) 3(2分)
(2)①Ba2++SO42-== BaSO4↓(2分)?
②Al(OH) 3+ OH-== AlO2-+2H2O (2分)? 1:1(2分)
(3)c(NaOH)= " 1" mol/L(2分); c(FeCl3)=" 0.1" mol/L(2分)
本题解析:(1)当加入B溶液110 mL时,有图可知道刚开始生的沉淀分别为)BaSO4、Fe(OH) 3、Al(OH) 3,由于Al(OH) 3是两性物质,其可以溶解与过量的氢氧化钠溶液,所以溶液中的沉淀是BaSO4、Fe(OH) 3;(2)从90 mL至100 mL之间加入10 mLB溶液时,由图像纵坐标不变可知此段发生反应的离子方程式是:①Ba2++SO42-== BaSO4↓②Al(OH) 3+ OH-== AlO2-+2H2O,有图可以看出溶液B中Na2SO4与NaOH物质的量浓度之比为1:1;(3)由图可以知道铝离子的物质的量为0.02mol(10mL刚好消耗0.01mol的沉淀),钡离子的物质的量为0.1mol(10mL刚好生成0.01mol的沉淀,从开始到100mL),铁离子的物质的量为0.01mol,所以B溶液中NaOH物质的量浓度为1 mol/L,而A溶液中FeCl3物质的量浓度为 0.1 mol/L。
点评:本题考查了金属及其化合物,该考点是高考考查的重点和难点,本题要求学生要有一定的分析能力,该题有一定的难度。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《与量有关的离子方.. | |