微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C、D均为中学化学中的常见物质,请根据题中信息回答问题。
(1)已知它们存在如下反应转化关系:A +B→C +D(未配平,反应条件略去)。
①该转化关系中所涉及的反应为置换反应。若A是金属单质,D是非金属单质,且A 原子的质子数是D原子的2倍,则反应的方程式是?。
②该转化关系中所涉及的反应为非置换反应。若A、D分子的核外电子总数都为10个,B与C能发生反应,则反应的方程式是?。
(2)已知它们存在如下反应转化关系:A +B→C +D+H2O(未配平,反应条件略去)。
①该转化关系中所涉及的反应为氧化还原反应。若C、D两种气体均能使澄清石灰水变浑浊,当A的摩尔质量小于B时,物质B的名称为?,鉴别C、D两种气体不能选用的试剂是?。
a.Ba(OH)2溶液
b.酸性KMnO4溶液
c.紫色石蕊试液
d.H2O2与BaCl2混合液
e.酸化的Ba(NO3)2溶液
②该转化关系中所涉及的反应为非氧化还原反应。若A是造成温室效应的主要气体之一,C、D均为钠盐,D与B反应能转化为C。当参加反应的A、B物质的量之比为3∶4时,则C与D物质的量之比为?。
参考答案:(1)①2Mg + CO2 2MgO + C(2分)
2MgO + C(2分)
②4NH3+5O2 4NO+6H2O(2分)
4NO+6H2O(2分)
(2)①浓硫酸(写成硫酸不得分)(2分)? ac(2分)
②1∶2(2分)
本题解析:(1)①只有金属镁质子数为碳原子质子数的一倍,应为镁与二氧化碳反应;②10电子微粒间的反应,氨气与氧气反应生成一氧化氮和水或甲烷与氧气不完全燃烧生成一氧化碳和水等;(2)CD为二氧化硫和二氧化碳,反应物为碳和浓硫酸;两种气体均为酸性氧化物与Ba(OH)2溶液反应生成沉淀,能使石蕊指示剂反应呈红色;但二氧化硫具有还原性能被氧化剂氧化如酸性KMnO4溶液、H2O2、酸化的Ba(NO3)2溶液(硝酸)生成硫酸根离子从而得到鉴别;
②该反应为CO2+NaOH――Na2CO3+ NaHCO3+H2O,设Na2CO3和NaHCO3物质的量分别为x、y,根据钠原子守恒得2x+y=4?根据碳原子守恒得x+y=3,解得x=1,y=2。
本题难度:一般
2、填空题 (19分)
有关元素X、Y、Z、W的信息如下
元素
| 有关信息
|
X
| 所在主族序数与所在周期序数之差为4
|
Y
| 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子
|
Z
| 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏
|
W
| 地壳中含量最高的金属元素
|
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为?。
铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
_______________________________________________。
(2)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为_____________________,相关反应的离子方程式为_______________________________。
(3)以上述所得WX3溶液为原料制取无水WX3,先制得WX3・6H2O晶体,主要操作包括__________________________,在_____________________条件下加热WX3・6H2O晶体,能进(4)一步制取无水WX3,其原因是(结合离子方程式简要说明)_______________________________。
参考答案:
(1)2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑?(3分)
(2)2Fe3+ + 2e- 2Fe2+? (或Fe3+ + e-
2Fe2+? (或Fe3+ + e-  ?Fe2+)?(3分)
?Fe2+)?(3分)
(3)(2分)溶液变为蓝色?(2分)? 2Fe3+ + 2I- = 2Fe2+ + I2?(3分)
(4)加热浓缩、冷却结晶、过滤?(3分)?干燥的HCl气流(2分)
Al3+ + 3H2O  Al(OH)3 + 3H+,在干燥的HCl气流中,抑制AlCl3的水解,且
Al(OH)3 + 3H+,在干燥的HCl气流中,抑制AlCl3的水解,且
带走AlCl36H2O晶体受热产生的水气,故能得到AlCl3。?(3分)
本题解析:略
本题难度:一般
3、简答题 如图是几种中学化学常见物质的转化关系图,其中气体D、E为单质,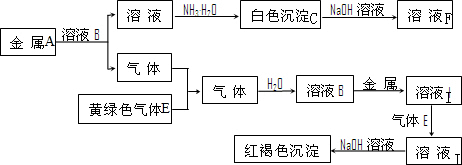
请按要求回答下列问题.
(1)C的化学式是______
(2)写出反应“C→F”的离子方程式______;
(3)写出反应“I→J”的离子方程式______;
(4)写出金属A与NaOH溶液反应的离子方程式______.
参考答案:由溶液加一水合氨生成白色沉淀,白色沉淀溶于NaOH溶液,则沉淀C为Al(OH)3,由元素守恒可知,金属A为Al,气体为H2,黄绿色气体E为Cl2,溶液B为HCl,由最后的红褐色沉淀,I为FeCl2,J为FeCl3,
(1)由上述分析可知,C为Al(OH)3,故答案为:Al(OH)3;
(2)反应“C→F”的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)反应“I→J”的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)金属A与NaOH溶液反应的离子方程式为2Al+2H2O+2OH-=AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=AlO2-+3H2↑.
本题解析:
本题难度:简单
4、填空题 非金属单质A,经如下图所示的过程转化为含氧酸D,已知D为常见强酸
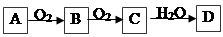
请回答下列问题:
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体
①D的化学式是??
②在工业生产中B气体的大量排放被雨水吸收后形成了?而污染了环境
(2)若A在常温下为气体,C是红棕色气体。①A和C的化学式分别是:A?;C?
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式?
参考答案:(1)①H2SO4?②酸雨?
(2)①N2? NO2?②Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2
本题解析:根据元素化合物知识分析,非金属单质可以实现上述转化的分别有C、S、N2, D为强酸,则不会是碳单质的转化;(1)①B是能使品红溶液褪色的被有刺激性气味的无色气体,B为SO2.所以据此推断C为SO3、D为H2SO4;②SO2被雨水吸收后生成H2SO3和H2SO4,即形成酸雨;(2)①A在常温下为气体,C是红棕色气体为NO2,A为N2;②据①可知D为硝酸,浓硝酸与铜反应生成NO2,答案为:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑.
本题难度:一般
5、推断题 A、B、C、D、E、F六种物质在一定条件下的相互转化关系如图所示(所有反应物和生成物均已给出)。

(1)若反应①、②、③均为水溶液中的置换反应,且A、D、E为卤素单质,则A、D、E的氧化性由强到弱的顺序为___________________,其中A的化学式是___________。
(2)若B是一种能使湿润的红色石蕊试纸变蓝的气体,C是一种溶于强碱而不溶于B的水溶液的白色沉淀,图中B与E反应生成D。则气体B的空间构型为___________,反应①的离子方程式为_________________。
(3)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应②的化学方程式为
__________________
(4)若B是一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D和E的循环,则化合物B的电子式为__________,用电子式表示物质A的形成过程___________,F的饱和溶液与足量E反应的离子方程式为__________________。
参考答案:
(1)E>A>D;Br2
(2)三角锥形;3NH3・H2O+Al3+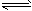 3NH4++Al(OH)3↓
3NH4++Al(OH)3↓
(3)Fe3O4+4CO 4CO2+3Fe
4CO2+3Fe
(4)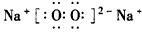 ;
;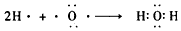 ;CO2+2Na++CO32-+H2O=2NaHCO3↓
;CO2+2Na++CO32-+H2O=2NaHCO3↓
本题解析:
本题难度:一般