��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (12)�±���Ԫ�����ڱ���һ����, ��Ա��еĢ١�����Ԫ��,��д���пհ�:
?����
����
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| 0��
|
2
| ?
| ?
| ?
| ��
| ��
| ��
| ?
| ?
|
3
| ��
| ?
| ��
| ?
| ?
| ��
| ��
| ��
|
4
| ��
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
(1) ����ЩԪ����,��ѧ��������õ���:??(��Ԫ�ط���)��
(2) ������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��_______���ܺ͢������������ˮ�������ǿ���ıȽ�:_____________������Ӧ��ѧʽ����
(3) ��������������������Ԫ����_____ ____(��Ԫ�ط���)��д���������������������Ʒ�Ӧ�����ӷ���ʽ_____ _________ _________ _________ _________ ____��
(4)��ʾ�ٺ͢����ɵĻ�����ĵ���ʽ??��
�ο��𰸣�(1)Ar?��2��HClO4? KOH>NaOH?
��3��Al? Al2O3��2NaOH ��2NaAlO2��H2O?��4����
�����������1��ϡ������Ԫ�ص������������Ѿ��ﵽ�ȶ��ṹ������ѡ������õģ������Ar��
��2���ǽ�����Խǿ������������ˮ���������Խǿ��������HClO4��������Խǿ������������ˮ����ļ���Խǿ���ƵĽ���������K�ģ����Լ�����KOH>NaOH��
��3��������������������������������������Ʒ�Ӧ�ķ���ʽΪAl2O3��2NaOH ��2NaAlO2��H2O��
��4���ٺ͢����ɵĻ����������Ȼ�̼�����м��Լ��Ĺ��ۻ��������ʽΪ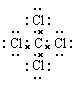 ��
��
�����Ѷȣ���
2������� A��B��C��D��EΪ���ֳ����Ķ�����Ԫ�أ������£�A��B���γ�B2A2��B2A����Һ̬�����B��D����ɷ���X��Xˮ��Һ�ʼ��ԣ�CԪ�ص���ɫ��Ӧ�ʻ�ɫ��E��Cͬ���ڣ���E�ļ����Ӱ뾶��ͬ����Ԫ���γɵļ������а뾶��С�ġ��Իش�
��1��DԪ�������ڱ��е�λ��Ϊ?��
��2��B2 A��X�ķ��ӽ�����ӵ�������ͬ��ֻ��һ�����ӷ���ʽ����֤����д�������ӷ�Ӧ����ʽ?��
��3��A��D��E����Ԫ���γɵ��Σ���ѧʽA9D3E����ˮ��Һ�����ԣ������ӷ���ʽ������ԭ��?��
��4��W��Q����A��B��C��D����Ԫ��������������ɵIJ�ͬ���͵�ǿ����ʣ�������0.1mol��L��1W��ˮ��Һ��pHΪ13��Q��ˮ��Һ���������ܺ�W��Ӧ�ų����壬���ʵ���Ũ����ͬ�� W��Q��Һ��ˮ�ĵ���̶���ǰ��С�ں��ߡ���WΪ?��QΪ?���ѧʽ����
��5��B��E�γɵĻ�����E2B6�����л��ϳ�����ǿ��ԭ���������ɽ�������̼���»�ԭ�ɼ��飬д���÷�Ӧ����ʽ?��
��6����֪��ҵ�ϳ�X�ķ�Ӧ����ʽ��D2 (g)+3B2 (g) 2X(g)����H ="-92.4" kJ��mol��1�����ʵ��Ĵ����ͺ��º�ѹ�����·�Ӧ������˵����ȷ����?��
2X(g)����H ="-92.4" kJ��mol��1�����ʵ��Ĵ����ͺ��º�ѹ�����·�Ӧ������˵����ȷ����?��
A���ﵽ��ѧƽ��ʱ�����淴Ӧ�������
B����Ӧ�����в��Ϸ����X��ʹƽ�ⳣ��K��С��ƽ�������ƶ������ںϳ�X
C���ﵽƽ��������¶ȣ�ƽ�ⳣ��K����B2��ת���ʽ���
D���ﵽ��ѧƽ��Ĺ����У�����ƽ����Է���������С
�ο��𰸣�
��1���ڶ����ڢ�A��?
��2��H3O++NH3=NH4++H2O
��3��Al3++3H2O Al(OH)3+3H+?
Al(OH)3+3H+?
��4��W? NaOH?��Q? NH4NO3 ?
��5��3CO2+2Al2H6=3CH4+2Al2O3?
��6��A
�����������������ó�A��B��C��D��EԪ�طֱ�ΪO��H��Na��N��Al����2��������ӣ�H+����������ͬ������ͨ��һ�����ʰ���һ�������н�ϵ����Ӷ���������֤������3��A��D��E����Ԫ���γɵ���ΪAl(NO3)3��������ˮ����Һ�����ԣ���4��������0.1mol��L��1W��ˮ��Һ��pHΪ13��������������Ũ��Ϊ0.1mol��L��1��ȷ��ΪһԪǿ����Һ����ΪAΪNaOH��Q��ˮ��Һ���������ܺ�W��Ӧ�ų����壬ȷ��ΪNH4NO3;��6��A��ƽ��״̬�ı�־�����淴Ӧ������ȣ���ȷ��B���¶Ȳ��䣬ƽ�ⳣ�����䣬����C����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ����С����Ӧ��ת���ʽ��ͣ�����D���ڴﵽƽ��Ĺ����У��淴Ӧ������������ʵ������٣������������䣬Ħ�����������
�����Ѷȣ�����
3��ѡ���� �������ڱ��е�7���ڵڢ�A��Ԫ�أ����й����ص����������в���ȷ����?
A���ڻ������г�+2��
B���رȸƵĽ�����ǿ
C���������������
D��̼����������ˮ
�ο��𰸣�C
����������ڢ�A��Ԫ�أ�������Be��Mg��Ca��Sr��Ba��Ra��ͬ����Ԫ�ؼ��������ԣ����еݱ��ԣ����=������������A��ȷ��ͬ���壬���ϵ��£�ԭ�ӵ�ʧ������������ǿ����Ԫ�صĽ���������ǿ����B��ȷ��ͬ���壬���ϵ��£�ԭ�ӵ�ʧ������������ǿ��������������Ӧˮ����ļ�������ǿ��Ca(OH)2��Ba(OH)2��Ϊǿ���Ra(OH)2Ϊ��ǿ���C����D���ͬ��Ԫ�ص������ԣ�̼��ơ�̼�ᱵΪ�������̼����ҲΪ�������G��ȷ
�����Ѷȣ���
4��ѡ���� ����Ԫ�������ɷ���������ƶϣ����д������
A����(At)Ϊ��ɫ���壬HAt���ȶ�
B����(T1)������ͬ��Ԫ�أ�ԭ�Ӻ�����6�����Ӳ㣬�Ʋ�T1(OH)3��������������
C����֪��Sr��þͬ����ԭ�Ӱ뾶���ڸƣ�������(SrSO4)��������ˮ�İ�ɫ����
D��������(H2Se)�������ȶ��Բ�
�ο��𰸣�B
���������A��ȷ��±�ص��ʴ��ϵ��£���ɫ��������⻯����ȶ�����Ԫ�صķǽ������йأ��ǽ�����Խǿ�⻯��Խ�ȶ���
B������Ϊ��IIIA��Ԫ�أ�ͬ����Ԫ�ش��ϵ���Ԫ�صĽ�������ǿ��T1(OH)3�������������������
C��ȷ�����ڵ�IIA��Ԫ�ص���������˵��������þ����ˮ�����������ˮ�����ᱵ������ˮ�����Ʋ�������(SrSO4)��������ˮ�İ�ɫ���壻
D��ȷ��������Ϊͬ����Ԫ�أ�����λ������·����ǽ����Ա��������⻯����ȶ��Ա�������
�����Ѷȣ�һ��
5������� W��M��N��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯����ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��M��Neԭ�ӵĺ�����������1��N��X���ڣ�X�ĵ�����һ�ֳ����İ뵼����ϣ�Y�������������������ڲ��������3����Z�ķǽ�������ͬ��������Ԫ�������

��1��Ԫ��X�����ڱ��е�λ����_______________��Ԫ��Y�����ӽṹʾ��ͼΪ____________
��2�������й��������ʵıȽ��У���ȷ����________________
A��M��X��Z�γɵĵ����۷е� M��X��Z
B���⻯������ȶ��ԣ�W��X
C��X�ֱ���W��Z�γɵĻ������л�ѧ�����ͣ��������;���ͬ
D��ZԪ�غ����������һ��ǿ��YԪ�صĺ�����