微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关叙述中不正确的是( )
A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B.在离原子核越近的区域运动的电子,能量越低
C.1869年俄国化学家门捷列夫经研究提出了元素周期律,并列出了第一张元素周期表
D.金刚石晶体中每个碳原子与相邻的三个碳原子以共价键结合,形成空间网状结构
2、推断题 已知:A、B、C、D、E、F五种元素核电荷数依次增大,属周期表中前四周期的元素。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序为___________。(用元素符号表示)
⑵B的氯化物的熔点比D的氯化物的熔点__________(填高或低),理由是___________。
⑶E的最高价氧化物分子的空间构型是___________。
⑷F的核外电子排布式是___________,F的高价离子与A的简单氢化物形成的配离子的化学式为___________。
⑸A、F形成某种化合物的晶胞结构如图所示,则其化学式为__________;(黑色球表示F原子)?
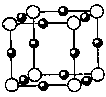
⑹A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为_____________。
3、选择题 同周期的A、B、C三元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3CO4,则下列判断错误的是
A.非金属性A>B>C
B.气态氢化物稳定性HA>H2B>CH3
C.原子半径A>B>C
D.阴离子还原性C3->B2->A-
4、推断题 D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是_______,写出该元素的任意3种含氧酸的化学式
_______;
(3)D和Y形成的化合物,其分子的空间构型为___________;
(4)D和X形成的化合物,其化学键类型属________,其晶体类型属________;
(5)金属镁和E的单质在高温下反应得到的产物是____________,此产物与水反应生成两种碱,该反应的化学方程式是____________________;
(6)试比较D和X的最高价氧化物熔点的高低并说明理由:___________________。
5、选择题 X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是
[? ]
A. 由mXa+与nYn-1,得m+a=n-b
B. X2-的还原性一定大于Y-
C. X、Y一定不是同周期元素
D. 若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY