微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于元素周期表的说法正确的是(?)
A.第ⅠA族的元素都为金属元素
B.第三周期非金属元素含氧酸的酸性从左到右依次增强
C.过渡元素全部是金属元素
D.周期表中有7个主族,7个副族,一个0族,一个VIII族,共16个族16个纵行
参考答案:C
本题解析:第ⅠA族的元素中的氢元素是非金属,A不正确;第三周期非金属元素最高价含氧酸的酸性从左到右依次增强,B不正确;过渡元素全部是金属元素,C正确;周期表中有7个主族,7个副族,一个0族,一个VIII族,共16个族18个纵行,D不正确,答案选C。
点评:该题是基础性试题的考查,也是高考中的常见考点,难度不大。主要是考查学生对元素周期表结构的熟悉了解程度,旨在培养学生的能力,提高学生的学习效率和学习积极性。
本题难度:一般
2、填空题 短周期的3种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3化合物。请回答:
⑴X元素的名称是?;Y元素的名称是?;Z元素的名称是?。
⑵XZ3化合物的分子式是?,电子式是?。
⑶分别写出X、Y的含氧酸的分子式??、?。
参考答案:(1)氮 、碳 、?氢?; (2)NH3?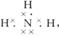 ?(3)HNO3、H2CO3
?(3)HNO3、H2CO3
本题解析:本题能力层次为C。从元素X、Y、Z之间的原子序数的关系(依次变小),它们核外电子层数的关系(之和是5),以及X、Z可形成化合物(即不是稀有元素),这就确定有两个元素在第二周期,一个元素在第一周期,即Z是氢元素。由于Y元素原子的最外电子层上的电子数是它的电子层数的2倍,即最外层有4个电子,所以Y是碳元素。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,故X元素原子最外电子层上的电子数是5,所以X是氮元素。答案:(1)氮 、碳 、?氢?; (2)NH3?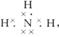 ?(3)HNO3、H2CO3
?(3)HNO3、H2CO3
学法指导:本题主要考查物质的结构与元素周期表的关系,以及运用其关系进行推理的能力。在解答这类试题时,主要是熟练掌握“位,构,性”三者之间的关系。
本题难度:简单
3、选择题 下列物质中,在相同条件下最易与氢气化合的是(?)
A.F2
B.Cl2
C.Br2
D.I2
参考答案:A
本题解析:非金属性越强,越容易合氢气化合,所以正确的答案是A。
本题难度:简单
4、选择题 X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )。
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.三种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X
参考答案:A
本题解析:X原子的最外层电子数是其电子层数的3倍,说明X是氧元素,则Y必然为硫元素,Z原子的核外电子数比Y原子少1,Z为磷。它们在周期表中的位置如图 。元素非金属性由弱到强的顺序为P<S<O,A项正确;S元素最高价氧化物对应水化物的化学式可表示为H2SO4,B项错误;非金属性越强,其氢化物的稳定性越强,因此,X的气态氢化物最稳定,C项错误;根据元素周期律,原子半径由大到小的顺序为P>S>O,D项不正确。
。元素非金属性由弱到强的顺序为P<S<O,A项正确;S元素最高价氧化物对应水化物的化学式可表示为H2SO4,B项错误;非金属性越强,其氢化物的稳定性越强,因此,X的气态氢化物最稳定,C项错误;根据元素周期律,原子半径由大到小的顺序为P>S>O,D项不正确。
本题难度:一般
5、选择题 下列判断错误的是( )
A.沸点:NH3>PH3>AsH3
B.熔点:Si3N4>NaCl>SiI4
C.酸性:HClO4>H2SO4>H3PO4
D.碱性:NaOH>Mg(OH)2>Al(OH)3
参考答案:A
本题解析:NH3、PH3、AsH3都属于分子晶体,分子晶体相对分子质量越大,熔沸点越高,故沸点:AsH3>PH3,由于NH3分子间存在氢键,故沸点:NH3>AsH3>PH3,A错;Si3N4属于原子晶体,NaCl属于离子晶体,SiI4属于分子晶体,物质的熔点:原子晶体>离子晶体>分子晶体,故B正确;非金属元素的非金属性越强,最高价氧化物的水化物的酸性越强,根据元素周期律可知非金属性Cl>S>P,故酸性HClO4>H2SO4>H3PO4,C正确;金属元素的金属性越强,最高价氧化物的水化物的碱性越强,根据元素周期律可知金属性Na>Mg>Al,故碱性NaOH>Mg(OH)2>Al(OH)3,D正确。
本题难度:一般