微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在配制一定物质的量浓度的溶液时,必须用到的仪器是
A.
B.
C.
D.
参考答案:D
本题解析:分析:根据结构判断各选项中仪器,再根据配制溶液的步骤所用仪器进行判断,配制一定物质的量浓度的溶液时需要确定所配溶液的体积,故容器为定量仪器.
解答:配制步骤为计算、称量(量取)、溶解、定容等,称量时用到天平、钥匙(量取时用到量筒),溶解时用到烧杯、玻璃棒,定容需要容量瓶、胶头滴管,
A、仪器为集气瓶,配制中不需要,故A不符合;
B、仪器为锥形瓶,配制中不需要,故B不符合;
C、仪器为圆底烧瓶,配制中不需要,故C不符合;
D、仪器为容量瓶,由于溶液配制需确定溶液的体积,必须使用,故D符合;
故选D.
点评:考查对仪器的认识、一定物质的量浓度溶液的配制,比较基础,注意基础知识的掌握.
本题难度:一般
2、选择题 所含分子数相同的一组物质是
A.1gH2和1gN2
B.1molH2O和1gH2O
C.3.2gO2和4.8gO3
D.44gCO2和16gO2
参考答案:C
本题解析:分析:物质的量相同,所含分子数目相同,根据n= 计算判断.
计算判断.
解答:A、1gH2和1gN2,二者物质的量之比与摩尔质量成反比为28:2=14:1,故二者含有分子数之比为14:1,不相等,故A错误;
B、1gH2O的物质的量为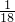 mol,二者物质的量不同,含有水分子数目不同,故B错误;
mol,二者物质的量不同,含有水分子数目不同,故B错误;
C、3.2gO2的物质的量为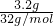 =0.1mol,4.8gO3的物质的量为
=0.1mol,4.8gO3的物质的量为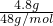 =0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;
=0.1mol,二者物质的量相同,含有相同的分子数目,故C正确;
D、44gCO2的物质的量为1mol,16gO2的物质的量为0.5mol,二者物质的量不同,含有的分子数目不同,故D错误;
故选C.
点评:本题考查物质的量的有关计算,比较基础,旨在考查学生对基础知识的理解掌握,注意对公式的理解与灵活运用.
本题难度:一般
3、选择题 现有一瓶甲、乙的混合物,已知甲、乙属同系物,甲、乙某些性质如下:
A.蒸馏
B.萃取
C.加热升华
D.分液
参考答案:A
本题解析:分析:互溶且沸点不同的液体采用蒸馏的方法分离.
解答:根据题中信息可以看出,甲和乙两物质的熔点相差不大,均易溶于水,能互溶,但是沸点相差较大,所以可以采用蒸馏的方法通过控制沸点的不同来实现二者的分离,故选A.
点评:本题考查物质的分离、提纯的基本方法选择与应用,难度不大,熟记常见物质的分离方法和原理是解题的关键所在.
本题难度:简单
4、选择题 下列说法中正确的是
A.1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L
B.从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C.配制500mL 0.5mol?L-1的CuSO4溶液,需62.5g胆矾
D.中和100mL 1mol/L的H2SO4溶液,需NaOH为4g
参考答案:C
本题解析:分析:A、水的体积不等于溶液的体积;
B、从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度不变;
C、先计算出胆矾的物质的量,再计算质量;
D、根据H++OH-=H2O计算.
解答:A、水的密度与NaCl溶液的密度不等,则配制后溶液的体积不等于1L,故A错误;
B、溶液为均一的混合物,从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度不变,故B错误;
C、胆矾的物质的量为0.5L×0.5mol/L=0.25mol,质量为0.25mol×250g/mol=62.5g,故C正确;
D、根据H++OH-=H2O,需要NaOH的物质的量为0.1L×1mol/L×2=0.2mol,质量为0.2mol×40g/mol=8g,故D错误.
故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,注意水的密度与NaCl溶液的密度不等,水的体积不等于溶液的体积.
本题难度:一般
5、选择题 根据中国民航总局规定,旅客乘坐飞机时,可以较大量随身携带的物质是
A.硫黄
B.氯酸钾
C.硝酸钾
D.碘盐
参考答案:D
本题解析:分析:根据物质的可燃性判断,易燃易爆物一旦着火或爆炸,极易造成巨大危害,上述选项中只要属于易燃易爆物,就是不准随身携带的.
解答:爆炸是指可燃物在有限的空间里急剧燃烧,放出大量的热,生成的气体急剧膨胀,发生爆炸.
硫磺、氯酸钾、硝酸钾等物质属于易燃易爆品,乘坐公共交通工具时禁止携带,碘盐不属于易燃易爆物;
故选D.
点评:本题考查易燃易爆物,难度不大,解答本题的关键是要充分理解爆炸的含义,了解常见的易燃易爆物质.
本题难度:困难