��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ҵ�������е�һ����Ҫ��Ӧ��SO2�ڡ��µĴ������� ������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
[? ]
A��ʹ�ô�����Ϊ�˼ӿ췴Ӧ����
B��SO2������100%��ת��ΪSO3
C������O2��Ũ�ȿ����SO2��ת����
D��ƽ��ʱSO2��Ũ����SO3��Ũ�����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ���л�ѧ��Ӧ����Ҫ�ӿ���ǣ�������
A��ʳ�︯��
B�������ϻ�
C������
D������ʴ
�ο��𰸣�A��Ϊ��Լ��ʳ��Ӧ��Сʳ�︯�ܵ����ʣ���A����
B��Ϊ������Դ���˷ѣ�Ӧ��С�����ϻ������ʣ���B����
C��Ϊ��߸ֵIJ��������㹤ũҵ���ɵ���Ҫ��Ӧ������ֵ����ʣ���C��ȷ��
D��Ϊ������Դ���˷ѣ�Ӧ��С����ʴ�����ʣ���D����
��ѡD��
���������
�����Ѷȣ���
3������� ����β���к���CO��NO2���ж�����,��������װβ������װ��,��ʹ�ж��������Ӧת��Ϊ�����塣����β����CO��NO2������һ�������¿��Է�����Ӧ:4CO(g)+2NO2(g) 4CO2(g)+N2(g) ��H="-1" 200 kJ��mol-1
4CO2(g)+N2(g) ��H="-1" 200 kJ��mol-1
(1)���º���������,����˵���÷�Ӧ�Ѵﵽƽ��״̬����?(����ĸ,��ͬ)��
A.�����ڻ��������ɫ���ٱ仯
B.�����ڵ�ѹǿ���ֲ���
C.2v(NO2)��=v(N2)��
D.�����ڻ�������ܶȱ��ֲ���
(2)��ʹ�÷�Ӧ�ķ�Ӧ��������,��ƽ�����淴Ӧ�����ƶ�����?��
A.��ʱ�����CO2
B.�ʵ������¶�
C.��С�������ʹ��ϵѹǿ����
D.ѡ���Ч����
(3)���ڸ÷�Ӧ,�¶Ȳ�ͬ(T2��T1)������������ͬʱ,����ͼ����ȷ����?��
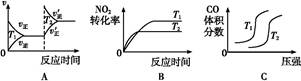
�ο��𰸣�(1)CD (2)B (3)B
���������(1)���º�����,���������ɫ���ٱ仯˵��NO2Ũ�Ȳ��ٸı�,��˵����Ӧ�Ѵ�ƽ��;���ڸ÷�Ӧ�������������С�ķ�Ӧ,�����ڵ�ѹǿ���ֲ���,��ζ����������������ٸı�,��˵����Ӧ�Ѵ�ƽ��;2v��(NO2)=v��(N2)˵����Ӧδ��ƽ��,��Ӧ��ϵ������ȫΪ����,��������������,�ں��������������ڻ�������ܶ�һֱ���ֲ���,���ܶȲ���,����˵����Ӧ�Ѵ�ƽ�⡣(2)�����CO2���·�Ӧ��Ũ�ȼ�С,��ʹ�÷�Ӧ�ķ�Ӧ���ʼ�С��ƽ��������Ӧ�����ƶ�,A��;��H��0,������ʹ��Ӧ��������,ƽ�������ƶ�,B��;�÷�Ӧ�������������,��С�������,��ϵѹǿ������ƽ�������ƶ�,C��;������Ӱ�컯ѧƽ��,D����(3)����,�����淴Ӧ����Ӧͬʱ����,A��;������ʹ��Ӧ��������,����������ӦΪ���ȷ�Ӧ,���µ���ƽ�������ƶ�,NO2ת���ʽ���,B��;�ɷ�Ӧ�ص��֪,����ѹǿƽ������,CO���������Ӧ�ü�С,�����¶�ƽ������,CO���������Ӧ������,��C����
�����Ѷȣ�һ��
4������� ��2L������3�����ʼ���з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ����Ӧ��tʱ����ƽ�⣬��ͼ��ʾ��
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��______��
�ڷ�Ӧ��ʼ��t��Y��ƽ����Ӧ������______��
�۹��ڸ÷�Ӧ��˵����ȷ����______��
A������tʱ�̸÷�Ӧ��ֹͣ��
B����tʱ��֮ǰX���������ʴ��������������ʣ�
C����tʱ��Y������Ӧ���ʵ����淴Ӧ���ʣ�
D����tʱ�̴ﵽƽ������Ϊ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ�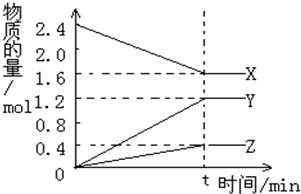
�ο��𰸣�����ͼ����Կ�������Ӧ��X�����ʵ�����С��Y��Z�����ʵ������࣬��XΪ��Ӧ�Y��ZΪ�����tʱ�̺�X�����ʵ���Ϊ��ֵ�Ҳ�Ϊ�㣬Ϊ���淴Ӧ���ҡ�n��X������n��Y������n��Z��=0.8mol��1.2mol��0.4mol=2��3��1����Ӧ�Ļ�ѧ����ʽΪ��2X?3Y+Z��
�ʴ�Ϊ��2X?3Y+Z
����tminʱ���ڣ���Y��ʾ��Ӧ��ƽ������v��Y��=��c(Y)��t=1.2mol-0mol2Ltmin=0.6t?mol/��L�qmin����
�ʴ�Ϊ��0.6t?mol/��L�qmin��
��A�����淴Ӧ�Ƕ�̬ƽ�⣬tʱ�̣��ﵽƽ��״̬�����淴Ӧ������ȣ�����Ϊ�㣬��A����
B����tʱ��֮ǰ�����淴Ӧδ�ﵽƽ�⣬��Ӧ������Ӧ������У�V����V�棬��X���������ʴ��������������ʣ���B��ȷ��
C��tʱ�̣���Ӧ�ﵽƽ��״̬�����淴Ӧ������ȣ���Y������Ӧ���ʵ����淴Ӧ���ʣ���C��ȷ��
D����Ӧ����ƽ��ı�����V��=V�棬��D����
��ѡBC
���������
�����Ѷȣ�һ��
5��ѡ���� ������ʾ���淴Ӧ2A(g)��B(g)  2C(g)(����ӦΪ���ȷ�Ӧ)����ȷͼ��Ϊ��?��
2C(g)(����ӦΪ���ȷ�Ӧ)����ȷͼ��Ϊ��?��
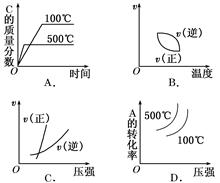
�ο��𰸣�AC
����������˷�Ӧ������Ӧ�����������С�����ȵĿ��淴Ӧ��A��¶�Խ�ߣ��ﵽƽ���ʱ��Խ�̣���ƽ�����ƣ�C�������������ͣ�A��ȷ��B���ʾ�¶���v�Ĺ�ϵ�������¶ȵ����ߣ�v(��)��v(��)����������ȴ�½�������ȷ��C�����ѹǿ������v(��)��v(��)������ƽ�����ƣ�v(��)>v(��)����ȷ��D������¶ȵ����ߣ�A��ת����Ӧ�����ͣ�����ȷ��
�����Ѷȣ�һ��