微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NA代表阿伏加德罗常数的值,下列叙述不合理的是( )
A.常温常压下,22.4?L?N2所含的分子数小于NA
B.在含有1mol?CH3COO-的醋酸钠溶液中,Na+数目略大于NA
C.8.0?g?Cu2S和CuO的混合物中含有铜原子数为0.1NA
D.0.1mol?Fe?与0.1mol?Cl2充分反应,转移的电子数为0.3?NA
参考答案:A、常温常压下,22.4?LN2物质的量不是1mol,所含的分子数小于NA,故A正确;
B、含有1mol?CH3COO-的醋酸钠溶液中,存在醋酸根离子水解后的醋酸根离子为1mol,所以醋酸钠的化学式可知,钠离子物质的量略大于1mol,故B正确;
C、若8.0?g?全是Cu2S,则其中含有的铜原子数=8.0g160g/mol×2×NA=0.1NA;若8.0?g?全是CuO,则其中含有铜原子数=8.0g80g/mol=0.1mol,所以8.0?gCu2S和CuO的混合物中含有铜原子数为0.1NA,故C正确;
D、0.1mol?Fe与0.1mol?Cl2充分反应,根据化学方程式2Fe+3Cl2=2FeCl3,0.1molFe有剩余,所以反应的电子转移由完全反应的氯气计算为0.2mol,故D错误;
故选D.
本题解析:
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
A.60gSiO2中含有NA个SiO2分子
B.标况下,22.4LSO3的分子数为NA
C.1L0.5mol?L-1CuCl2溶液中含有0.5NA个Cu2+
D.15.6g Na2O2与过量CO2反应时,转移的电子数为0.2NA
参考答案:A、二氧化硅为原子晶体,二氧化硅晶体中不存在分子,故A错误;
B、标况下,三氧化硫不是气体,题中条件无法计算三氧化硫的物质的量,故B错误;
C、1L0.5mol?L-1CuCl2溶液中含有溶质氯化铜0.5mol,由于铜离子部分水解,导致溶液中铜离子小于0.5mol,溶液中含有的铜离子小于0.5NA,故C错误;
D、15.6g Na2O2的物质的量为0.2mol,0.2mol过氧化钠过量CO2反应时生成了0.1mol氧气,转移了0.2mol导致,转移的电子数为0.2NA,故D正确;
故选D.
本题解析:
本题难度:一般
3、选择题 设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A.1molα-氨基乙酸(甘氨酸)分子中存在10NA对共用电子
B.25℃时,l?L?pH=13的Ba(OH)2?溶液中含有Ba2+的数目为0.1NA
C.在一定条件下,46g的NO2和N2O4混合气体中原子数目为3NA
D.含有非极性键的数目为NA的Na2O2与水充分反应产生标况下O2约11.2L
参考答案:A.α-氨基乙酸的结构简式为CH2NH2COOH,含有的共价键有2个C-H键,2个N-H键,1个C-N键,1个C-C键,1个C=O键,1个C-O键和1个O-H键,所以1molα-氨基乙酸(甘氨酸)分子中存在10NA对共用电子,故A正确;
B.pH=13时,c(OH-)=0.1mol/L,c(Ba2+)=0.05mol/L,lLpH=13的Ba(OH)2溶液中含有Ba2+的数目为0.05NA,故B错误;
C.NO2和N2O4混合气体中N和O原子个数都为1:2,可按NO2计算,n(NO2)=1mol,则混合气体中原子数目为3NA,故C正确;
D.1molNa2O2含有1molO-O键,为非极性键,则含有非极性键的数目为NA的Na2O2为1mol,与水反应生成0.5molO,标准状况下体积为11.2L,故D正确.
故选B.
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.4.4gCO2和N2O混合物所含原子数为0.3NA
B.一定温度下,6.72LCl2与11.2gFe粉反应转移电子数为0.3NA
C.50mL18mol/L硫酸与足量的Cu粉反应产生10.08L气体
D.标准状况下,4g氦气中所含的原子数为0.5NA
参考答案:A、CO2和N2O的摩尔质量都是44g/mol,每个分子中含有的原子数相等,所以4.4gCO2和N2O混合物所含原子数为0.3NA,故A正确;
B、温度压强不同,气体摩尔体积不同,因为,该题温度不明确,气体摩尔体积不确定,所以无法计算转移电子数,故B错误;
C、浓硫酸和铜反应,稀硫酸和铜不反应,浓硫酸和铜反应的过程中,浓度逐渐减小,达到一定浓度时和铜不反应,故C错误;
D、氦气的摩尔质量是4g/mol,所以4g氦气的物质的量是1mol,所含的原子数为NA,故D错误.
故选A.
本题解析:
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值,下列说法错误的是
A.常温常压下,22.4L氢气中含有的氢分子数为NA
B.24gMg变为Mg2+时失去的电子数为2?NA
C.32g臭氧分子中含有的氧原子数为2?NA
D.1L1mol/LCaCl2溶液中含有氯离子数为2?NA
参考答案:A
本题解析:分析:A.不是标准状况,不能使用气体摩尔体积22.4L/mol;
B.根据镁原子的结构分析判断;
C.根据臭氧的分子式计算原子数;
D.根据体积和浓度计算公式计算,结合氯化钙的化学式计算氯离子数.
解答:A.常温常压下,不是标准状况,氢气所处的状态不是标准状况,不能使用气体摩尔体积22.4L/mol,故A错误;
B.镁原子最外层电子数为2,1个镁原子失去2个电子变为Mg2+,24克金属镁物质的量为1mol,失去电子物质的量为0.2mol,即2NA,故B正确;
C.32g臭氧分子中,含有氧原子物质的量:n=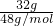 ×3=2mol,含有氧原子的个数为2NA,故C正确;
×3=2mol,含有氧原子的个数为2NA,故C正确;
D.1L1mol/LCaCl2溶液中含有为1molCaCl2,氯离子为2mol,氯离子数为2NA,故D正确;
故选A.
点评:本题主要考查了阿伏伽德罗常数的运用,注意气体摩尔体积的应用条件、原子结构的判断、相关公式的换算运用,平时须总结常见易错点.
本题难度:困难