| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《离子共存》高频试题特训(2017年最新版)(四)
参考答案:C 本题解析: 本题难度:一般 2、选择题 下列离子组能在酸性溶液中大量共存的是? 参考答案:B 本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。溶液显酸性,则A中SO32-,B中CO32-、OH-,D中HSO3-均不能与氢离子大量共存,答案选B。 本题难度:简单 3、选择题 下列说法正确的是 |
参考答案:C
本题解析:AlO2-与HCO3-反应生成Al(OH)3沉淀和CO32-,不生成气体A项错; NaAlO2溶液是碱性溶液,H+不能在其中存在,B项错;C项正确;氨水在离子方程式书写中不能拆,D项错。
本题难度:一般
4、填空题 (15分)某强酸性溶液X可能含有Ba2+、A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-、NO2-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下: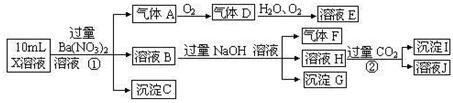
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是 ▲ ,不能确定是否含有的离子(M)是 ▲ ,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是 ▲ 。
▲ 。
(2)沉淀I的化学式为 ▲ ,气体F的电子式为 ▲ 。
(3)写出生成A的离子方程式: ▲ 。
(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4。请写出制备过程中的离子方程式 ▲ 。
(5)1.0mol/L的E溶液与2.0mol/LF溶液等体积混合完全反反应后,溶液中各离子的浓度大小关系为 ▲ 。
(6)假设测定A、F、I均为0.10mol,50mL X溶液中n(H+)=0.40mol,当沉淀C物质的量大于0.70mol时,溶液X中还一定含 ▲ 。
参考答案:(15分) (1)A13+、NH4+、Fe2+ SO42- Fe3+ Cl-
取少量X溶液于试管中,加入几滴KSCN溶液,溶液不变红色则说明无Fe3+;或取少量B溶液于试管中,加入几滴AgNO3溶液,若无白色沉淀说明无Cl- (每空各2分)
(2) Al(OH)3 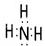 (每空各1分)
(每空各1分)
(3)3Fe2++4H++NO3-==3Fe3++NO+2H2O (2分)
(4)3ClO-+2Fe(OH)3+4OH-==3Cl-+2FeO42-+5H2O (2分)
(5)C(NH4+)> C(NO3-)> C(OH-)> C(H+) (2分)
(6)Fe3+ (1分)
本题解析:略
本题难度:一般
5、选择题 在酸性溶液中,能大量共存的是离子组是
A.Mg2+、Fe3+、NO3-、SCN-
B.Al3+、Fe2+、Cl-、SO42-
C.K+、Na+、Cl-、HCO3-
D.Na+、Ba2+、NO3-、SO42-
参考答案:B
本题解析:离子大量共存:指的是离子之间两两相互不反应。A中Fe3+与SCN-会反应生成血红色物质;B符合题意;C中由于题目说明是在酸性溶液中,故要在离子组中加入H+,HCO3-与 H+会反应生成气体,不能大量共存;D中Ba2+与SO42-会反应生成BaSO4;故选B。
点评:了解离子能大量共存的条件。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《阿伏伽德罗.. | |