微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组物质,不能只用一种试剂鉴别的是( )
A.CH4、CH2=CH2、CH3CH=CH2
B.CH3CHO、CH3COOH、CH3CH2OH
C.CuO、MnO2、C粉
D.C2H5OH、CCl4、C6H6
参考答案:A
本题解析:B项可用新制氢氧化铜悬浊液鉴别,乙醛加热出现砖红色沉淀、乙酸混合氢氧化铜变澄清、乙醇无明显现象;C项可用浓盐酸鉴别,氧化铜溶解、二氧化锰加热剧烈反应生成黄绿色气体、碳粉无明显想象;D项可用水鉴别,乙醇溶解、四氯化碳分层水在上层、苯分层水在下层。A中乙烯和丙烯都含有碳碳双键,因此只用一种试剂无法鉴别,答案选A。
本题难度:简单
2、实验题 如不用任何试剂鉴别氯化钡、硝酸银、碳酸钠、盐酸四种溶液,先将四种溶液分别编为A、B、C、D进行互滴实验,将现象列表如下:
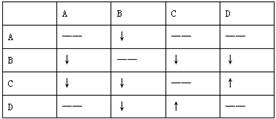
根据以上信息可以推出:A?,B?,C?,D?。
参考答案:A是氯化钡,B是硝酸银,C是碳酸钠,D是盐酸。
本题解析:在四种物质中,能跟另外三种物质反应产生沉淀的只有硝酸银,因此B是硝酸银;能跟其中两种物质反应产生沉淀而跟另一种物质反应产生气体的只有碳酸钠,因此C是碳酸钠;而能跟碳酸钠反应产生气体的物质D必是盐酸;那么A必然是氯化钡。结论为:A是氯化钡,B是硝酸银,C是碳酸钠,D是盐酸。
本题难度:简单
3、选择题 不用其他试剂无法鉴别的一组溶液是
A.氯化铁溶液和氯化铜溶液
B.硫酸钠溶液和氯化钠溶液
C.氯化铝溶液和氢氧化钠溶液
D.硫酸溶液和碳酸钠溶液
参考答案:B
本题解析:氯化铁溶液为棕黄色,氯化铜溶液为蓝色,观察颜色可鉴别;硫酸钠溶液和氯化钠溶液都为无色,二者不反应,不用其他试剂无法鉴别,故选B;把氯化铝溶液逐滴滴入到氢氧化钠溶液中,开始无现象,一定程度后出现白色沉淀,而把氢氧化钠溶液逐滴滴入到氯化铝溶液中,开始出现白色沉淀,一定程度后沉淀逐渐溶解,最后消失,可以签别;把硫酸溶液逐滴滴入到碳酸钠溶液中,开始无现象,一定程度后生成气体,而把碳酸钠溶液逐滴滴入到硫酸溶液中,开始时就生成气体,可以签别。
本题难度:一般
4、填空题 氯碱工业是最基本的化学工业之一,它的产品应用广泛。请回答下列问题:
(1)氯碱工业是利用电解食盐水生产?为基础的工业体系。
(2)电解前,为除去食盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入下列试剂的顺序合理的是?(填下列各项中序号)。
a、碳酸钠、氢氧化钠、氯化钡? b、碳酸钠、氯化钡、氢氧化钠
c、氢氧化钠、碳酸钠、氯化钡? d、氯化钡、氢氧化钠、碳酸钠
(3)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
成分
| NaCl
| Mg(OH)2
| CaCO3
| BaSO4
| 其他不溶物
|
质量分数(%)
| 15~20
| 15~20
| 5~10
| 30~40
| 10~15
|
?
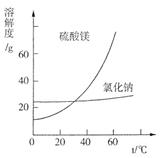
利用盐泥生产MgSO4・7H2O晶体的工艺流程如下图所示。

回答下列问题:
①酸洗过程中加入的酸为?,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是 ?。
②过滤所得滤渣的主要成分为??。
③根据图分析,蒸发结晶过滤所得晶体A主要成分为?。
④真空干燥MgSO4・7H2O晶体的原因是?。
参考答案:(12分)
(1)(2分)烧碱、氯气(氢气)
(2)(2分)d
(3)(8分)①(稀)硫酸(1分);硫酸能与碳酸钙反应,搅拌过程中产生的CO2不断逸出,碳酸钙转化为硫酸钙(1分)
②BaSO4、CaSO4等不溶于酸的物质(2分,答出BaSO4即可) ③NaCl(2分)
④防止失去结晶水(2分)
本题解析:(1)电解食盐水生成NaOH、H2、Cl2,所以氯碱工业是利用电解食盐水生产烧碱、氯气(氢气)为基础的工业体系。
(2)Na2CO3的作用除了除去Ca2+外,还有除去过量的BaCl2的作用,所以Na2CO3的顺序在BaCl2的后面,只有d项符合。
(3)①因为最终产品为MgSO4・7H2O,为避免生成杂质,应加入稀硫酸;加入硫酸后,H2SO4和CaCO3发生反应:H2SO4+CaCO3=CaSO4+CO2↑+H2O,搅拌过程中产生的CO2不断逸出,碳酸钙转化为硫酸钙。
②盐泥含有BaSO4,加入H2SO4后CaCO3转化为CaSO4,所以过滤所得滤渣的主要成分为BaSO4、CaSO4等不溶于酸的物质。
③蒸发结晶时温度较高,MgSO4溶解度大,所以析出NaCl,过滤所得滤渣的主要成分为NaCl。
④在空气中干燥即烘干MgSO4・7H2O,MgSO4・7H2O容易失去结晶水,所以真空干燥MgSO4・7H2O晶体的原因是防止失去结晶水。
本题难度:困难
5、选择题 下列物质的检验试剂选择正确的是(?)
A.I2----------淀粉
B.H+----------酚酞
C.OH--------蓝色石蕊试纸
D.Cl----------盐酸酸化的AgNO3
参考答案:A
本题解析: I2常用淀粉进行检验,A正确; H+用酚酞检验不出来,可用紫色石蕊检验,B错误; OH-用蓝色石蕊试纸检验不出来,应用酚酞检验, C错误; Cl-常用硝酸酸化的AgNO3检验, D错误。
点评:熟记常见物质的常用检验试剂
本题难度:一般