��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� I��X��W��Y��Z��Ϊ����������Ԫ�أ�ԭ��������������Xԭ�ӵ�������������W��4����X��Y�����ڱ������λ����ͼ��
��1��X�����ڱ��е�λ����______��
��2��Z������ʯ���鷴Ӧ�Ļ�ѧ����ʽΪ______��
��3��Y����̬�⻯��ͨ��FeCl3��Һ�У���Y�����������÷�Ӧ�����ӷ���ʽΪ______��
��4��W-Y���ܵ����һ�����͵�أ��������ڵ�W��Y����Ϊ����������֮��ͨ���������ʴ���W+���ӣ���ط�ӦΪ16W��l��+nY8��l��
8W2Yn��l����
�ŵ�ʱ��W+������______���ƶ��������ĵ缫��ӦʽΪ______��
�����ݻ��ɱ���ܱ������г���A��B��C�������壬������ӦxA+yB?zC�������£�ͨ��ѹ����������ı�ѹǿ���ֱ���A��ƽ��Ũ�����±���
| ʵ����� | �� | �� | ��
ѹǿ�Mpa
1��105
2��105
1��106
C��A��mol?l
0.08
0.16
0.88
|
��5�����ݢ٢����ݷ����ó���x+y______z�����������������=������
��6�����¶��£���ѹǿΪ1��106Paʱ���˷�Ӧ��ƽ�ⳣ������ʽΪ______��
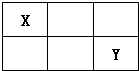
�ο��𰸣���X��W��Y��Z��Ϊ����������Ԫ�أ�ԭ��������������Xԭ�ӵ�������������W��4���������������������ܳ���8���ֶ�������Ԫ�أ���W����������ֻ��Ϊ1��X������������Ϊ4����X��Y�����ڱ������λ�ÿ�֪��XΪCԪ�ء�YΪSԪ�أ����ԭ��˳���֪��WΪNa��ZΪCl��
��1��XΪCԪ�أ������ڱ��е�λ���ǵڶ����ڵڢ�A�壬�ʴ�Ϊ���ڶ����ڵڢ�A�壻
��2��������ʯ���鷴Ӧ�����Ȼ��ơ����������ˮ����Ӧ��ѧ����ʽΪ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
��3��Y����̬�⻯��H2Sͨ��FeCl3��Һ�У�Fe3+���������������ɵ���S������Ϊ����ΪFe2+��ͬʱ����H+���÷�Ӧ�����ӷ���ʽΪH2S+2Fe3+=S��+2Fe2++2H+��
�ʴ�Ϊ��H2S+2Fe3+=S��+2Fe2++2H+��
��4��Na-S���ܵ����һ�����͵�أ��������ڵ�Na������Ϊ����������֮��ͨ���������ʴ���Na+���ӣ��ŵ�ʱ��Ϊԭ��أ�Na+�����������ƶ�������ΪS8��õ��ӵõ�Sn2-�������缫��ӦʽΪ��nS8+16e-=8Sn2-��
�ʴ�Ϊ������nS8+16e-=8Sn2-��
��5�����ݢ٢����ݿ�֪��ѹǿ����һ����A��Ũ������һ����˵������ѹǿƽ�ⲻ�ƶ�����x+y=z���ʴ�Ϊ��=��
��6���ɢڢ����ݿ�֪���۵�ѹǿ��Ϊ�ڵ�5������AŨ�ȱ�Ϊ�ڵ�5.5����˵������ѹǿƽ�����淴Ӧ�����ƶ���B���ʷ���Һ������xA��g��+yB?zC��g����ƽ�ⳣ��k=cz(C)cx(A)���ʴ�Ϊ��cz(C)cx(A)��
���������
�����Ѷȣ�һ��
2������� �����Ԫ�����ڱ���һ���֣�����������ĸ�ֱ����ijһԪ�أ�������ݱ�������Ԫ�أ��ش��������⣺
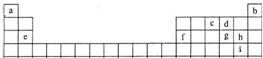
��1������ը���ۡ�ָ����200������ǰ���������������ʶ�������һ���ܶ������¶����ߵ�ԭʼ���У�����ij��ԭ���������˱�ը�����Ȳ��������ӡ����Ӻ͵��ӣ����Ͳ�����Ԫ�أ����ɴ˿�֪���Ȳ�����Ԫ����______����д������ĸ����
��2��e��f���ʼ�ef�Ͻ���Ӳ��������______����д���ƣ���
��3����д��ԭ�Ӻ�������������Ϊ���ڲ������3����Ԫ��ԭ�ӵĺ�������Ų�ʽ��______����Ԫ�صͼ���������һ��������ת��Ϊ��������ķ�ӦΪ��ҵ��Ҫ��Ӧ����д���˷�Ӧ�Ļ�ѧ����ʽ______��
��4���Ƚϱ���cdg����Ԫ�صĵ�һ�����ܵĴ�С˳��______��
��5����д������֤h��i�ǽ�����ǿ����һ����ѧ��Ӧ�����ӷ���ʽ______��
��6����������ᡢ�����������������Ҫ��Ԫ����______����д������ĸ����
�ο��𰸣���1���������ԭ��Ҳ�����������ɵ�ԭ�ӣ����ԭ������ԭ�ӣ�
�ʴ�Ϊ��a��
��2���Ͻ��Ӳ�ȴ��ںϽ�����һ������Ӳ�ȣ�����e��f���ʼ�ef�Ͻ���Ӳ��������þ���Ͻ�
�ʴ�Ϊ��þ���Ͻ�
��3�����������ǵڶ����Ӳ㣬ԭ�Ӻ�������������Ϊ���ڲ������3����Ԫ��ԭ����Oԭ�ӣ������������⣻���������ǵ������Ӳ㣬��ԭ����S���������⣻���������Ų�ʽΪ��1s22s22p63s23p4��
��Ԫ�صͼ�������Ϊ��������������������ܷ���������ԭ��Ӧ������������
��Ӧ����ʽΪ��2SO2+O2����.��2SO3��
�ʴ�Ϊ��1s22s22p63s23p4��2SO2+O2����.��2SO3��
��4��ͬһ���ڣ�Ԫ�صĵ�һ����������ԭ������������������ڢ�A��ĵ�һ�����ܴ��ڵڢ�A�壬�ڢ�A��ĵ�һ�����ܴ��ڵڢ�A��ģ�ͬһ���壬��һ����������ԭ���������������С��N��OԪ������ͬһ���ڣ�NԪ�����ڵڢ�A�壬OԪ�����ڵڢ�A�壬���Ե�Ԫ�صĵ�һ�����ܴ�����Ԫ�صģ�O��SԪ������ͬһ���壬����Ԫ�ص�ԭ������������Ԫ�صģ�������Ԫ�صĵ�һ�����ܴ�����Ԫ�صģ�����cdg����Ԫ�صĵ�һ�����ܵĴ�С˳��Ϊc��d��g����N��O��S����
�ʴ�Ϊ��c��d��g����N��O��S����
��5��h��i����ͬһ���壬Ԫ�صķǽ�����Խǿ����������Խǿ��ֻҪ�������û��嵥�ʼ���֤����Ԫ�صķǽ�����ǿ����Ԫ�صģ����ӷ�Ӧ����ʽΪ��Cl2+2Br-=2Cl-+Br2��
�ʴ�Ϊ��Cl2+2Br-=2Cl-+Br2��
��6���������б�����Ԫ�أ����б�����������������������Ӻͽ��������ӻ�笠����ӣ����б������ٻ���һ��Ԫ�أ������к��н��������ӣ��������ٺ���4��Ԫ�أ������к���笠����ӣ��������Ϊ��������ӣ��������ٺ���3��Ԫ�أ�������������ᡢ�����������������Ҫ��Ԫ�������֣���acd��
�ʴ�Ϊ��acd��
���������
�����Ѷȣ�һ��
3��ѡ���� ���и������ʵ����ʼ����ӵ����ʱ仯��ȷ���ǣ�������
A���ȶ���H2S��HCl��HBr��HI
B����ԭ��Na+��S2-��Br-��Cl-
C�����뾶Cl-��K+��S2-��S
D������HClO4��H2SO4��H2CO3��HClO
�ο��𰸣�A����Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ����ǽ����ԣ�Cl��Br��S��I�������ȶ��ԣ�HCl��HBr��H2S��HI����A����
B����ԭ�ӵ�������Խǿ�����Ӧ���ӵĻ�ԭ��Խ���������ԣ�Cl��Br��S�����Ի�ԭ�ԣ�S2-��Br-��Cl-��Na+��ԭ�ԣ���B����
C�����������Ų���ͬʱ��ԭ������ԽС���ӵİ뾶Խ���Լ�ͬһԪ�صIJ�ͬ���ӣ������ӵİ뾶����ԭ�ӵİ뾶�����Ӱ뾶��S2-��Cl-��K+��S2-��S����C����
D����Ԫ�صķǽ�����Խǿ������������ˮ���������Խǿ���ǽ����ԣ�Cl��S��C��
���ԣ�HClO4��H2SO4��H2CO3����H2CO3�����Դ���HClO���������ԣ�HClO4��H2SO4��H2CO3��HClO����D��ȷ��
��ѡ��D��
���������
�����Ѷȣ���
4��ѡ���� ��֪A��B�ֱ�Ϊͬ���ڵĢ�A��͢�A�������Ԫ�أ����ǵ�ԭ�������ֱ�Ϊm��n�������й�ϵ�����ܳ�������
[? ]
A.?n��m��16?
B.?n��m��6?
C.?n��m��30?
D.?n��m��10?
�ο��𰸣�D
���������
�����Ѷȣ���
5��ѡ���� ����ԭ����������±��Ԫ�أ�����±�����ʵĵݱ���ɣ��������仯�������������ȷ���ǣ�������
A��KAt�˼�����KBr
B�����ڳ�����Ϊ��ɫ����
C��NaAt�۵�ϸ�
D����������ˮ���������Ȼ�̼
�ο��𰸣�A��±��Ԫ�ش��ϵ��£����Ӳ������࣬�뾶������KAt�˼�����KBr����A��ȷ��
B��±��Ԫ�ش��ϵ��£����ʵ���ɫ����۷е���������������ɫ���壬��B��ȷ��
C��±��Ԫ�������γɵĻ�����Ϊ���ӻ�����۵�ߣ���C��ȷ��
D�����������ڷǼ��Է��ӣ���������ˮ�������ڷǼ��Ե��л��ܼ�����D����
��ѡD��
���������
�����Ѷȣ�һ��