| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《电解质和非电解质》试题巩固(2017年最新版)(六)
参考答案:B 本题解析:A、质子数相同,中子数不同的原子的互称为同位素,D2、H2、T2是由不同同位素构成的单质,错误;B、CO2、CCl4、NH3都是由极性键、分子构成的共价化合物,正确;C、氯气既不是 电解质也不是非电解质,错误;D、同系物的结构相似,但三者分子中的羟基所连的位置不同,前两者属于酚类,后者属于醇类,错误,答案选B。 本题难度:一般 3、选择题 下列说法中,正确的有( ) |
参考答案:C
本题解析:(1)明矾水解产生的氢氧化铝胶体能够吸附水中悬浮的固体颗粒,使之形成沉淀而除去,因此可用于水的净化;碳酸钡不溶于水,但是能够在酸中溶解,故不可用于钡餐透视,错误;(2)氮氧化物会导致形成光化学烟雾,而碳氢化合物不会,错误;(3)氨常用作制冷剂,是因为其沸点极低,很容易液化,气化时吸收大量的热,使环境的温度降低,正确;(4)硅的提纯与应用,促进了半导体元件与集成芯片的发展,可以说“硅是信息技术革命的催化剂”,正确;(5)在硫酸亚铁铵的制备实验中,为了得到硫酸亚铁铵晶体,应蒸发溶剂的方法,错误;(6)通电时,溶液中溶质粒子分别向两极移动,胶体中粒子也向两极移动,错误;(7)由于Mg活动性比Al强,所以铝粉和氧化镁粉末混合,在高温不能发生铝热反应,错误; (8)高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遭遇强碱会发生反应因此会“断路”,正确; (9)可用稀盐酸、碳酸钠溶液、硅酸钠溶液只能证明酸性HCl>H2CO3>H2SiO3,而不能证明氯、碳、硅三种元素的非金属性,错误; (10)同主族元素的简单阴离子还原性越强,则元素的非金属性就越弱,而其水解程度不一定越大,错误; (11)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝,正确;(12)在硫酸铜结晶水含量测定实验中,至少要用天平称量2次质量,错误; (13)将水蒸汽通过灼热的铁粉,粉末变黑色,说明铁在高温条件下可与水发生化学反应,错误; (14)先取少量试液于试管中,再加入氢氧化钠溶液,将润湿的红色石蕊试纸放在试管口,红色石蕊试纸不变蓝,可能是稀溶液没有产生氨气,因此不能证明溶液中是否含铵根离子,错误;(15)已知次磷酸(H3PO2)是一元中强酸,则NaH2PO2是正盐,正确。因此正确的说法是5句,选项是C。
考点:考查物质的性质、应用的正误判断的知识。
本题难度:一般
4、选择题 下列物质中,属于纯净物的是
①陶瓷,②水泥,③玻璃,④漂白粉,⑤胆矾,⑥氯水,⑦液氯
A.③⑦
B.③④⑥
C.⑤⑦
D.⑥⑦
参考答案:C
本题解析:
纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;据此结合常见物质的组成成分逐项分析即可.
解:①陶瓷是多种硅酸盐的混合物;②水泥是硅酸盐材料,是混合物;③普通玻璃是硅酸盐材料,是混合物;④漂白粉主要成分为次氯酸钙和氯化钙,是混合物;⑤胆矾是硫酸铜的结晶水合物,是化合物,属于纯净物;⑥氯水是氯气的水溶液,是混合物;⑦液氯是单质,氯气的液态形式,是纯净物;所以属于纯净物的是 ⑤⑦;答案选C。
考点:考查物质的分类
点评:本题考查了物质的分类,纯净物,混合物,难度不大。要分清氯水与液氯的区别,注意胆矾的成分。
本题难度:一般
5、选择题 按照物质的分类方法,HNO3应属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥ 一元酸 ⑦化合物
A.①②③④⑤⑥⑦
B.①④⑥⑦
C.①
D.①④⑤⑥⑦
参考答案:B
本题解析:HNO3应属于①酸,④含氧酸,⑥ 一元酸,⑦化合物。故选B。
考点:物质的简单分类 常见的氧化物、酸、碱和盐的判别
点评:本题主要考查物质的分类方法,解答时要分析物质的元素组成和物质组成,然后再根据各类物质概念的含义进行分析、判断,从而得出正确的结论。
物质的简单分类,如图所示: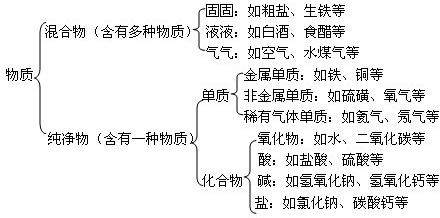 .
.
由于物质的分类原理是根据物质的组成物质或元素来进行分类的,所以物质的分类与其组成的关系是密不可分的,具体的详情如下:
1.从物质的分类(即混合物和纯净物)来看,物质的组成关系包含两层.第一层是混合物由纯净物组成(例如:空气是由氮气、氧气、稀有气体、二氧化碳、其他气体和杂质组成的,纯净的食盐水是由食盐和水组成的,黄铜(一种合金)是由铜和锌组成的,等等);第二层是纯净物由元素组成(例如:镁是由镁元素组成的,冰水混合物是由氢、氧两种元素组成的,氯酸钾是由钾、氯、氧三种元素组成的,等等).
2.至于纯净物的分类,是根据其组成元素的种类不同,将其分为单质和化合物.其中,单质是由同种元素组成的(例如:铁是由铁元素组成的,氢气是由氢元素组成的,氦气是由氦元素组成的,等等);化合物是由不同种元素组成的(例如:过氧化氢是由氢、氧两种元素组成的,高锰酸钾是由钾、锰、氧三种元素组成的,碳酸氢钠是由钠、氢、碳、氧四种元素组成的,等等).
3.单质的分类,是按照元素的分类来进行的.它可以分为金属单质(即由金属元素组成的单质,如铝、铜和锌等)、非金属单质(即由非金属元素组成的单质,如氧气、氮气和碳等)和稀有气体单质(即由稀有气体元素组成的单质,如氦气、氖气和氩气等).
4.化合物的分类,由于分类标准的不同,分成的类别也有所不同.一般情况下,是按照化合物的组成(或构成)不同,将其分为氧化物(即由两种元素组成的,并且其中一种是氧元素的化合物,如二氧化硫、五氧化二磷和氧化铜等)、酸(即由氢离子和酸根离子构成的化合物,如盐酸、硫酸和硝酸等)、碱(即由金属离子和氢氧根离子构成的化合物,如氢氧化钠、氢氧化钙和氢氧化钾等)、盐(即由金属离子和酸根离子构成的化合物,如氯化钠、碳酸钠和碳酸钙等).当然,有时也按化合物中是否含有碳元素分为:有机化合物(即含碳元素的化合物,如甲烷、乙醇和葡萄糖等;但有少数含碳元素的化合物,如一氧化碳、二氧化碳、碳酸和碳酸盐等具有无机化合物的特点,因此将其看做无机化合物)和无机化合物(即不含碳元素的化合物,如氯化钾、硫酸和氢氧化钠等).甚至,有时还按化合物的形成方式分为:离子化合物(即由阳离子和阴离子构成的化合物.一般是指组成中含有金属元素的化合物,如氯化钠、碳酸钠和硫酸铜等)和共价化合物(即以共用电子对形成分子的化合物.一般是指组成中不含金属元素的化合物,如氯化氢、水和二氧化碳等)。
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《阿伏伽德罗.. | |