微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 升高温度反应速度加快的主要原因是
A.分子运动速度加快
B.活化能增加
C.体系能量增加
D.活化分子的百分数增加
参考答案:D
本题解析:略
本题难度:简单
2、选择题 下列说法正确的是
[? ]
A.其它条件相同时,增大反应物浓度使分子获得能量,活化分子百分数提高,反应速率增大
B.判断过程的自发性能确定过程能否发生和过程发生的速率
C.体系有自发地向混乱度增加(即熵增)的方向转变的倾向,这是自然界的普遍规律
D.催化剂不影响反应活化能,从而只影响反应速率,不影响化学平衡
参考答案:C
本题解析:
本题难度:一般
3、选择题 决定某化学反应的反应速率的主要因素是( )
A.反应的温度
B.催化剂的使用
C.反应物的浓度
D.反应物的性质
参考答案:因决定化学反应速率的根本原因:反应物本身的性质.而浓度、温度、压强、催化剂是影响因素.故选:D.
本题解析:
本题难度:一般
4、选择题 下列图象表达正确的是( )

A.图①表示25℃时,用0.1mol?L-1盐酸滴定20mL0.1mol?L-1NaOH溶液
B.图②表示常温下,两份足量、等浓度的盐酸与等量锌粉反应时,其中一份滴加了少量硫酸铜溶液
C.图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液
D.图④表示向醋酸溶液中滴入氨水
参考答案:A、0.1mol?L-1NaOH溶液的pH为13,用0.1mol?L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错;
B、锌粉与硫酸铜反应生成了铜,消耗了锌粉,锌粉、铜和盐酸构成了原电池,加快了化学反应速率,但产生的氢气减少,故B错误;
C、图象表示滴入一定量Na2CO3时开始无沉淀,至HCl完全反应后才产生沉淀,与实事相符,故C正确;
D、向醋酸溶液中滴入氨水,生成了强电解质,溶液中离子浓度增大,恰好反应后继续滴加,溶液相当于稀释,溶液中离子浓度减小,故D错误;
故选:C.
本题解析:
本题难度:简单
5、简答题 下列图象在t1时所对应的反应条件改变可能为:
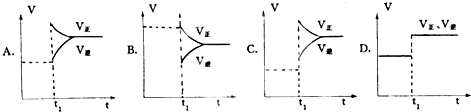
(1)升高温度______?(2)使用催化剂______?(3)增大反应物浓度______?(4)减少生成?物浓度______.
参考答案:(1)升高温度,瞬间V正、V逆都增大,若正反应为放热反应,V正增大较少、V逆增大较多,V正<V逆,平衡向逆反应移动,若正反应为吸热反应反应,V正增大较多、V逆增大较少,V正>V逆,平衡向正反应移动,图象C符合V正增大较多、V逆增大较少,V正>V逆,平衡向正反应移动,正反应为吸热反应,
故答案为:C;
(2)使用催化剂,瞬间同等程度增大V正、V逆,V正=V逆,平衡不移动,图象D符合,注意若反应前后气体的物质的量不变的反应,增大压强图象也符合,故答案为:D;
(3)增大反应物浓度,瞬间V正增大,V逆不变,V正>V逆,平衡向正反应移动,图象A符合,故答案为:A;
(4)减少反应物浓度,瞬间V正不变,V逆降低,V正>V逆,平衡向正反应移动,图象B符合,故答案为:B.
本题解析:
本题难度:一般