微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 把在空气中久置的铝片5.0 g 投入盛有500 mL 0.5 mol ・L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
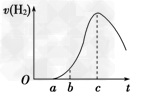
(1) 曲线由O →a段不产生氢气的原因是___________________________;有关反应的化学方程式为_________________ ;
(2) 曲线a→c段,产生氢气的速率增加较快的主要原因是____________________________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是____________________________;
(4)该反应若使用催化剂,可使H2产量增多吗?______(填“会”或“不会”)。
参考答案:(1)硫酸首先和氧化铝反应,不产生H2;Al2O3+3H2SO4===Al2(SO4)3+3H2O
(2)反应放热,温度升高是影响反应速率的主要因素,使反应速率增大
(3)硫酸的浓度逐渐减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降
(4)不会
本题解析:
本题难度:一般
2、选择题 锌粒和盐酸反应一段时间后,反应速率减慢。此时加热或加入浓盐酸,反应速率明显加快。上述实验中影响化学反应速率的因素有:
[? ]
①温度 ②固体的表面积 ③反应物的状态 ④溶液的浓度 ⑤催化剂
A.①④
B.①③
C.②④
D.①②③④⑤
参考答案:A
本题解析:
本题难度:一般
3、填空题 温度一定,在一个10L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:
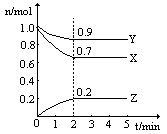
(1)从开始至2min,Z的平均反应速率为 。
(2)该反应的化学方程式为 。
(3)保持温度和体积不变,若n(X)=2mol,n(Y)="3" mol,n (Z)=1mol,该反应向 (填“正反应”或“逆反应”) 方向进行。
参考答案:(1)0.01mol/(L?min);
(2)3X(g) + Y(g)  2Z (g) ;
2Z (g) ;
(3)正反应。
本题解析:(1)0.2/2=0.1mol/(L?min);
(2)3X(g) + Y(g)  2Z (g)
2Z (g)
(3)浓度升高,压强增大,向体积减少的方向移动,所以向正反应方向移动。
考点:考查化学平衡。
本题难度:一般
4、选择题 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示,下列表述正确的是

[? ]
A.反应的化学方程式:2M = N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
参考答案:D
本题解析:
本题难度:简单
5、填空题 在T℃下,将1 mol N2和3 mol H2的混合气体通入固定体积为2L的密闭容器内,起始压强为101KPa,经过30s达到平衡,测得平衡混合气体的平均相对分子质量为10。试求:
此反应过程中N2的平均反应速率为_____________________________。
H2的转化率为_____________________。
维持一定温度和压强不变,在起始体积为2L的体积可变的容器中充入1 mol N2、3 mol H2,达平衡时N2的转化率与上述平衡相等,则该平衡时,容器的体积为_____________L。
参考答案:(1) 0.005 mol?L―1?S―1(其他合理答案也可得分)?
(2) 30%? (3) 1.7?(每空3分)
本题解析:略
本题难度:简单