��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���϶�1�š�������ʹ�õ�һ�ָ��ܵ�ء�����п���أ����صĵ缫��ӦʽΪ��
Zn+2OH--2e-=ZnO+H2O��Ag2O+H2O+2e-=2Ag+2OH-���ݴ��ж��������� (����)
A��������������
B������������ԭ
C������������ԭ
D��������������
�ο��𰸣�B
�����������������������ԭ��Ag2O-------2Ag���ϼ۽��ͱ���ԭ��Ϊ������
�����Ѷȣ�һ��
2��ѡ���� ijͬѧ�����KOH��Һ���ò����缫������CH3OH��O2�ķ�Ӧ������ԭ��ء�����˵����ȷ����(? )����������O2�õ����ӣ�������ԭ��Ӧ��ÿ����1molCH3OH���������·�ṩ6mole-�۸õ�ص��ܷ�ӦΪ��2CH3OH+3O2=2CO2+4H2O�ܵ�طŵ����Һ��pH��������
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�A
�������������CH3OH��O2�ķ�Ӧ�Ƴ�ȼ�ϵ�أ��ڵ�ط�Ӧ��O2 �����������õ��ӷ�����ԭ��Ӧ��Ӧ����������������Ԣ���ȷ���ڷ�Ӧ��ÿ����1molCH3OH��Ӧ1��5mol��O2 ������ת�Ƶ���6mol������ȷ��CH3OH��O2 ��Ӧ���ڼ��Խ����н��еģ��������ɵ�CO2 ����Ӧ����ӦʽӦ��Ϊ2CH3OH+3O2 +4KOH=2K2CO3+6H2O�����Ԣ۴������ŷ�Ӧ�Ľ��У�KOH�����ģ�������Һ��pHֵ�����½����ܴ���ֻ�Т٢���ȷ����ѡA��
�����Ѷȣ�һ��
3������� 27.��14�֣�����һ�ַdz���Ҫ��Ԫ�أ����ĵ��ʺͻ�����Ӧ�ù㷺���ڿ�ѧ����������������Ҫ��Ӧ�á��Իش��������⣺
��1��N2��H2Ϊԭ�Ϻϳɰ����ķ�ӦΪ��N2��g��+3H2��g�� 2NH3��g�� ��H<0�����д�ʩ�������H2��ת�����ǣ���ѡ����ţ� ��
2NH3��g�� ��H<0�����д�ʩ�������H2��ת�����ǣ���ѡ����ţ� ��
a��ѡ���ʵ��Ĵ��� b������ѹǿ
c����ʱ�������ɵ�NH3 d�������¶�
��2���ں��������£���N2��H2��һ��������ϵ��������һ��2L�̶��ݻ����ܱ������У�10���Ӻ�Ӧ��ƽ��ʱ��n��N2��=1.0mol��n��H2��=1.0mol��n��NH3��=0.4mol����Ӧ����v��N2��= mol/(L��min)��
��3�����ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O2��g�� 2NO2��g�� ��H>0
2NO2��g�� ��H>0
�÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ����ͼ��ʾ����t2��t4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ� ��
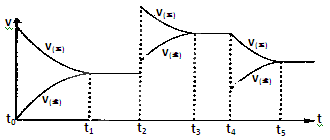
a����t1-t2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
b����t2ʱ����ȡ�Ĵ�ʩһ���������¶�
c����t3-t4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
d����t0-t5ʱ��������NO2�����������t3-t4ʱֵ�����
��4������������N2H4���ǵ������ֳ��������������Ʊ������ķ������Ա�ͪΪ�������ô��������백����Ӧ���÷�Ӧ�л�ԭ���������������ʵ���֮��Ϊ2:1��д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��5����֪��N2(g)+O2(g) = 2NO(g) ��H=+180.5kJ/mol
N2(g)+3H2(g) 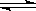 2NH3(g) ��H=��92.4kJ/mol
2NH3(g) ��H=��92.4kJ/mol
2H2(g)+O2(g) = 2H2O(g) ��H=��483.6kJ/mol
����17 g ��������������ȫ����һ�����������ˮ�������ų�������Ϊ ��
��6��ֱ�ӹ���ʽ����ȼ�ϵ�صĵ�ط�Ӧʽ��4NH3 + 3O2 = 2N2 + 6H2O���������Һһ��ʹ��KOH��Һ�����缫��Ӧʽ�� ���������Ϸ������õ�ع��������� (���Ҫ������Ҫ��)�����(KOH)��
�ο��𰸣���1�� bc
��2��0.01
��3��a d
��4��NaClO+2NH3=N2H4+NaCl+H2O
��5��226.25 kJ
��6��2NH3+6OH����6e��=N2+6H2O������Ҫ
�����������1��ѡ�����ֻ�ܼӿ췴Ӧ���ʣ�����Ӱ��ƽ����ƶ���H2��ת���ʲ��䣻����ѹǿ��ƽ���������С�ķ����ƶ�����ƽ�������ƶ���H2��ת�����������NH3��������Ũ�Ƚ��ͣ�ƽ�����ƣ�H2��ת�������������¶ȣ�ƽ�������ȵķ����ƶ����������ƶ���H2��ת���ʽ��͡�
��2�� N2��g��+3H2��g��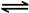 2NH3��g��
2NH3��g��
ʼ 1.2 1.6 0
ת 0.2 0.6 0.4
ƽ 1 1 0.4
V(N2)= mol/(L��S)="0.01" mol/(L��S)
mol/(L��S)="0.01" mol/(L��S)
��3��2NO��g��+O2��g��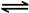 2NO2��g�� ��H>0����ӦΪ���������С�ķ��ȷ�Ӧ��a.�÷�Ӧ���������ʵ�����С�ķ�Ӧ�����º���ʱ��ѹǿ���䣬˵���ﵽƽ�⣻b.����Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����t2ʱ���������ʶ�����������Ӧ����������࣬ƽ�����ƣ��÷�Ӧ�����������С�ķ�Ӧ������ѹǿƽ�����ƣ�ת�������������±仯��c.���������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬��d.��ͼ��֪����t2ʱ���ı�����ƽ�����ƣ�t3ʱ�ﵽƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ�����ƣ�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ���
2NO2��g�� ��H>0����ӦΪ���������С�ķ��ȷ�Ӧ��a.�÷�Ӧ���������ʵ�����С�ķ�Ӧ�����º���ʱ��ѹǿ���䣬˵���ﵽƽ�⣻b.����Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����t2ʱ���������ʶ�����������Ӧ����������࣬ƽ�����ƣ��÷�Ӧ�����������С�ķ�Ӧ������ѹǿƽ�����ƣ�ת�������������±仯��c.���������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬��d.��ͼ��֪����t2ʱ���ı�����ƽ�����ƣ�t3ʱ�ﵽƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ�����ƣ�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ���
��4���Ʊ��µķ��������Դ�������������������Ӧ�л�ԭ���������������ʵ���֮��Ϊ2:1���Ƶ��µ�ϡ��Һ����ӦΪNaClO+2NH3=N2H4+NaCl+H2O
��5�����ݸ�˹���ɣ���H=�١�2-�ڡ�2+�ۡ�3=905.2kJ/mol����ô17g��1mol�������������ų�������Ϊ ��905.2kJ/mol="226.25" kJ
��905.2kJ/mol="226.25" kJ
��6��ȼ�ϵ���У�������ȼ�Ϸ���ʧ���ӵ�������Ӧ����������Ϊȼ�ϵ��ȼ��ʱ��������ʷ����ʧ���ӵĹ��̣���2NH3+6OH����6e��=N2+6H2O��������ӦΪO2+2H2O+4e-=4OH-,���ݵ����غ��������������Ӧ�����ɵ�OH-��ͬ�������Ϸ�������Ҫ����KOH��
���㣺��ѧƽ�⼰Ӱ�����ء��Ȼ�ѧ����ʽ����ѧ��Դ��
���������⿼���˸�˹���ɡ�Ӱ��ƽ�����ʵ����ء�ƽ����жϡ�ȼ�ϵ�ص����֪ʶ���Ѷ��еȣ�ע��ͼ��仯�ķ�����
�����Ѷȣ�����
4��ѡ���� ����������ȷ����
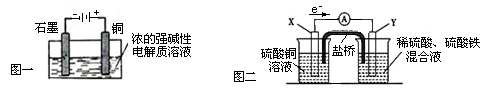
A��Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼһ��ʾ��ʯī�缫�ϲ���������ͭ�缫����������Ӧ
B��ͼһ��ʾ����0.1mol����ת��ʱ����0.1molCu2O����
C��ͼ��װ���з�����Cu��2Fe3+ = Cu2+��2Fe2+��X���Ǹ�����Y�����Ͽ�����ͭ
D����ͼ�������ŵ������Ǵ��ݵ����ά�ֵ��ƽ�⣬Fe3+�������Ž�������ձ���
�ο��𰸣�A
���������ͼһΪ����,�������ҺΪǿ������Һ��ʯī�缫���Դ��������Ϊ������������ԭ��Ӧ��2H2O + 2e- = H2��+ 2OH-��ͭ�缫���Դ��������Ϊ����������������Ӧ��2Cu �C 2e- + 2OH- = Cu2O + H2O ������ܷ�ӦΪ��2Cu+H2OCu2O+H2�����ɴ˿�֪Aѡ����ȷ�����ݵ���ܷ�Ӧ��֪������0.2mol����ת��ʱ������0.1molCu2O���ɣ� Bѡ���ȷ��ͼ��װ��Ϊԭ��أ�����ͼ�и����ĵ����������ж�X���ǵ�صĸ�����Y���ǵ�ص�����������װ���з����ķ�Ӧ��Cu��2Fe3+ = Cu2+��2Fe2+����֪X��Ϊ������ʧ���ӣ�����������Ӧ����Cu-2e- = Cu2+������X���IJ���Ӧ����ͭ������ԭ��ص��γ�������Y������Ӧ���ǻ�Ա�ͭ���Ľ�����ʯī�Ȳ��ϣ���Cѡ���ȷ�����ŵ����â����������ӵĶ���Ǩ�ƹ����˵���ͨ·���Ӷ���ͨ�ڵ�·���γɱպϻ�·�������˵���ͨ�����·�ӵ�ظ����������IJ���ת�ƣ�ʹԭ��ز��ϲ�����������ƽ���ɣ����ſ�ʹ�������ӵ����������е���Һ���ֵ����ԣ�ͬʱ������ֹ��Ӧ��ֱ�ӽӴ������ԣ�Fe3+�Dz��ܾ������Ž�������ձ��У���Dѡ���ȷ��
�����Ѷȣ���
5��ѡ���� ��ͼ��ʾ����пƬ��ͭƬ��ϡ������Һ���ɵ�ԭ����У�����������ȷ����
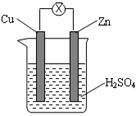
A��пƬΪ������������ԭ��Ӧ
B��������пƬ����ͭƬ
C��һ��ʱ���ͭƬ��������
D��һ��ʱ�����ҺpHֵ���