微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 俗话说, “陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程。请回答下列问题:
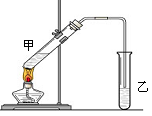
(1)在大试管中需加入浓硫酸、冰醋酸各2mL,乙醇3mL,加入试剂的正确的操作是?。
(2)浓硫酸的作用是:①?;②?。
(3)饱和碳酸钠溶液的主要作用是?。
(4)装置中通蒸气的导管只能插到饱和碳酸钠溶液的液面处,不能插入溶液中,目的 ?,长导管的作用是?。
(5)若要把制得的乙酸乙酯分离出来 91eXaM.org,应采用的实验操作是 ?。
(6)进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 ? 。
(7)试管乙中观察到的现象是____________________,由此可见,乙酸乙酯的密度比水________(填“大”或“小”),而且______。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的是(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
参考答案:(1)先在试管中加入一定量的乙醇,然后边振荡试管边慢慢加入浓硫酸和冰醋酸。
(2)催化剂,吸水剂。
(3)中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层析出。
(4)由于受热不均匀引起倒吸。将反应生成的乙酸乙酯蒸气冷凝。
(5)分液。?(6)防止大试管中液体暴沸而冲出导管。(7)上层产生油状液体,并闻到水果香味。小,易挥发。(8)②④⑤
本题解析:(1)制取乙酸乙酯加入试剂时应考虑浓硫酸的稀释问题,不能先在试管中加入浓硫酸,一般是先加入乙醇,再加入浓硫酸或冰醋酸;(2)浓硫酸的作用是做为催化剂和吸水剂;(3)饱和碳酸钠溶液的主要作用是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层析出;(4)不插入液体中是为了防止由于受热不均匀引起倒吸,长导管的作用是将反应生成的乙酸乙酯蒸气冷凝,提高收集的产率;(5)分离乙酸乙酯时先将盛有混合物的试管充分振荡,使乙酸、乙醇溶解,静置分层后取上层得乙酸乙酯,该操作是分液;(6)碎瓷片可以作为气化中心,可以防止大试管中液体暴沸而冲出导管;(7)乙中生成了乙酸乙酯,乙酸乙酯不溶于饱和碳酸钠溶液,并且具有水果香味,有机物不溶于水,一般是呈现油状,所以乙中观察到的现象是上层产生油状液体,并闻到水果香味,并且可以得出乙酸乙酯的密度比水,且易挥发;(8)CH3COOH+CH3CH2OH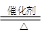 CH3COOC2H5+H2O,故对于反应的任何时候,都是单位时间里,生成1mol乙酸乙酯,同时生成1mol水,故①错误,同理③也是错误的,当该反应达到平衡时单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸,正反应的速率与逆反应的速率相等,即该混合物中各物质的浓度不再变化,所以答案为②④⑤。
CH3COOC2H5+H2O,故对于反应的任何时候,都是单位时间里,生成1mol乙酸乙酯,同时生成1mol水,故①错误,同理③也是错误的,当该反应达到平衡时单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸,正反应的速率与逆反应的速率相等,即该混合物中各物质的浓度不再变化,所以答案为②④⑤。
点评:乙酸乙酯的合成实验是高中的重要实验,是高考考查的重点,该题还综合考查了化学平衡、实验操作,有一定的综合性,难度适中,是一道不错的题目。
本题难度:一般
2、选择题 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如右图。
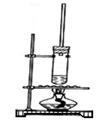
下列对实验叙述错误的是?(?)
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
参考答案:C
本题解析:略
本题难度:一般
3、选择题 下列叙述错误的是
[? ]
A.淀粉、油脂、蛋白质都能水解,但水解产物不同
B.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
C.乙烯和苯都能使溴水褪色,褪色的原因相同
D.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
参考答案:C
本题解析:
本题难度:一般
4、填空题 科学家发现某药物M能治疗心血管疾病,是因为它在人体内释放出一种“信使分子D”。并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。 ?
(1)已知M的分子量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%、18.50%,则M的分子式是____,D是双原子分子,相对分子质量为30,则D的分子式是____。 ?
(2)油脂A经下列途径可制得M
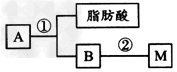
图中②的提示:CH3CH2OH+HO-NO2(硝酸)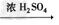 CH3CH2O-NO2(硝酸乙酯)+H2O?
CH3CH2O-NO2(硝酸乙酯)+H2O?
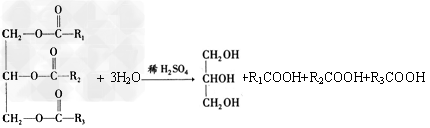
反应①的化学方程式是_________________,反应②的化学方程式是________________。 ?
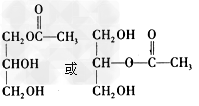
(3)C是B与乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式__________。 ?
(4)若将0.1?mol?B与足量Na反应,则需消耗_______g?Na。
参考答案:(1)C3H5N3O9;NO
(2)
(3)
(4)6.9
本题解析:
本题难度:一般
5、选择题 下列物质的类别与所含官能团都正确的是?
[? ]
A.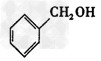 ?酚类
?酚类 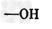
B.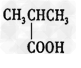 ? 羧酸?
? 羧酸? 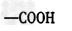
C.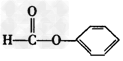 ? 醛类?
? 醛类? 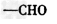
D.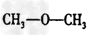 ? 醇?
? 醇? 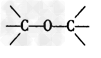
参考答案:B
本题解析:
本题难度:简单