微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验操作中错误的是
[? ]
A.蒸发操作时,不应使混合物中的水分完全蒸干后,才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:D
本题解析:
本题难度:简单
2、选择题 将3 mol・L-1的CaCl2溶液a mL稀释至b mL,稀释后溶液中Cl- 的物质的量浓度为
A.3a/b mol・L-1
B.6a/b mol・L-1
C.b/3a mol・L-1
D.a/b mol・L-1
参考答案:B
本题解析:
本题难度:一般
3、选择题 某学生设计了如下图所示的方法对A盐溶液进行鉴定:
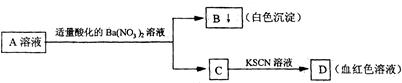
由此分析,下列结论中不正确的是? (?)
A.A中一定有Fe3+
B.C中一定有Fe3+
C.A可能为Fe2(SO4)3
D.B一定为BaSO4
参考答案:A
本题解析:A中不一定有铁离子,因为如果A只含有亚铁离子也由此现象,故A错误,为本题的答案;B正确,C中一定含有铁离子;C正确,A可以为Fe2(SO4)3,D也正确,因为硫酸钡为白色沉淀,不溶于硝酸。
点评:本题考查了离子检验的知识,该知识点是高考常常考查的,本题要理解A中不一定含有铁离子,若要检验则直接在A中滴加KSCN,看是否出现血红色,若是,则说明一定含有铁离子,若不是则说明含有的是亚铁离子,本题难度中等。
本题难度:一般
4、填空题 硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4・7H2O的流程如下:
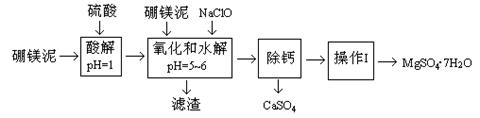
根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施__________、______________。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有?。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是?。在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为?。
(4)如何检验滤液中Fe3+是否被除尽,简述检验操作?。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃)
| 40
| 50
| 60
| 70
|
MgSO4
| 30.9
| 33.4
| 35.6
| 36.9
|
CaSO4
| 0.210
| 0.207
| 0.201
| 0.193
|
?
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤?、?。
(6)现有l.60 t硼镁泥,生产MgSO4・7H2O,若生产过程的产率为50%,则能生产出MgSO4・7H2O产品?t (计算结果保留三位有效数字)。(H:1? O:16? Mg:24? S:32)
参考答案:(1)升温、把硼镁泥粉碎、搅拌等(2分)?(2)SiO2(2分)
(3)Mn2+ + ClO- + H2O ==? MnO2↓ + 2H+ + Cl-(2分) 2Fe2+ + ClO- + 2H+ ="=" 2Fe3+ + Cl- + H2O(2分)
(4)取少量滤液于试管中,向其中几滴硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+。?(3分)
(5)蒸发浓缩(结晶),趁热过滤?(2分)?(6)1.97?(3分)
本题解析:(1)此处主要考查反应速率的影响因素,所以要想加快酸溶解速率可以从外因浓度、温度、接触面积等考虑,所以答案可以是升温、把硼镁泥粉碎、搅拌等。
(2)由于该硼镁泥的成分有MgO、CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等物质,所以酸溶后生成的阳离子有Mg2+、Ca2+、Mn2+、Fe3+、Fe2+、Al3+ ,不溶的有SiO2,加入氧化物NaClO后Fe2+ 被氧化为Fe3+,Mn2+ 被氧化为MnO2 ,所以调节pH至5―6,阳离子发生沉淀,生成的沉淀有Fe(OH)3、Al(OH)3,所以滤渣的所有成分为Fe(OH)3、Al(OH)3、MnO2、SiO2 。
(3)加入氧化剂NaClO,Mn2+、Fe2+均能够被其氧化,发生氧化还原反应,根据所给的产物形式,根据氧化还原反应缺项配平法,先把发生化合价变化的离子和物质写出,然后再根据电子得失守恒配平,再用电荷守恒和原子守恒配平所缺物质。所以离子方程式为:Mn2+ + ClO- + H2O ==? MnO2↓ + 2H+ + Cl-(2分) 2Fe2+ + ClO- + 2H+ ="=" 2Fe3+ + Cl- + H2O。
(4)检验Fe3+ 的方法是加入KSCN,利用显色反应检验,所以可以向溶液中加入硫氰化钾溶液检验溶液中是否存在三价铁离子,方法为:取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+。
(5)由温度对硫酸镁、硫酸钙的溶解度影响可看出,温度越高,硫酸钙溶解度越小,可以采用蒸发浓缩,趁热过滤方法除去硫酸钙;操作I”是将滤液继续蒸发浓缩,冷却结晶,再经过过滤,便得到了MgSO4?7H2O,故答案为:蒸发浓缩,趁热过滤;过滤(或过滤洗涤);
(6)100g硼镁泥中氧化镁的物质的量为:1.6×106g×40%×50%÷40g/mol=8×103mol,根据镁原子守恒,生成MgSO4?7H2O的物质的量为8×103mol,质量为246g/mol×8×103mol=1.968×106g≈1.97t,MgSO4?7H2O的质量为1.97t。
本题难度:困难
5、选择题 以下是分离乙酸乙酯、乙酸、乙醇的混合物的流程图,图中圆括号内填入适当的试剂,方括号内填入适当的分离方法,方框内是有关物质的名称。下列说法正确的是(?)
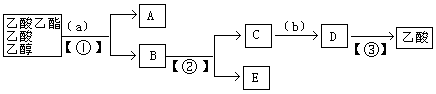
A.a为NaOH溶液,①为蒸馏
B.②、③均为蒸馏,①为分液
C.②为分液,C中含有醋酸钠
D.b可以是硫酸,也可以是盐酸
参考答案:B
本题解析:乙酸乙酯不溶于水,所以要除去乙酸和乙醇,需要加入饱和碳酸钠溶液,然后分液即得到乙酸乙酯,即A是乙酸乙酯。B中含有乙醇、碳酸钠和乙酸钠,通过蒸馏得到乙醇,即E是乙醇。C中含有碳酸钠和乙酸钠,然后加入硫酸,生成乙酸,最后再通过蒸馏得到乙酸,答案选B。
本题难度:一般