微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)下图中各仪器的名称分别是: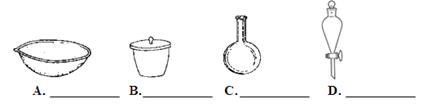
参考答案:(8分)A.蒸发皿? B.坩埚? C.圆底烧瓶? D.分液漏斗
本题解析:考查常见仪器的识别。根据仪器的结构可知,A是蒸发皿,B是坩埚,C是圆底烧瓶,D是分液漏斗。
本题难度:简单
2、选择题 下列实验中①配制 一定物质的量浓度的溶液;②pH试纸
一定物质的量浓度的溶液;②pH试纸 的使用;③过滤;④蒸发。都要用到的仪器是
的使用;③过滤;④蒸发。都要用到的仪器是
A.玻璃棒
B.烧杯
C.蒸发皿
D.酒精灯
参考答案:A
本题解析:略
本题难度:一般
3、实验题 重铬酸钠(Na2Cr2O7・2H2O)俗称红矾钠,是一种重要的无机盐产品,可作氧化剂,在印染、颜料、电镀、医药等工业方面有广泛的用途。某化学兴趣小组设计实验测定市场上的红矾钠中Na2Cr2O7的质量分数,其步骤如下:
I.称取Wg红矾钠,溶于酸配成l00mL溶液;
Ⅱ.用cmol・L-1的标准KMnO4酸性溶液滴定20.00mL一定浓度的FeSO4溶液,消耗KMnO4溶液20.00rnL;
Ⅲ。取20.00mL Na2Cr2O7溶液,用上述FeSO4溶液滴定,达到滴定终点时,消耗24.00mLFeSO4溶液;
查阅资料知:Cr2O72-在酸性条件下具有强氧化性,易被还原为Cr3+
回答下列问题:
(1)Na2Cr2O7与FeSO4的反应离子方程式为?.
(2)步骤Ⅱ中的滴定过程,滴定终点的现象为?;选用?(填“酸式”或“碱式”)滴定管。
(3)已知:MnO4-+5Fe2++8H+==Mn2++5Fe3++4H2O,此红矾钠中Na2Cr2O7的质量分数的表达式为?。
(4)判断下列操作对Na2Cr2O7的质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”):
①步骤Ⅲ中的滴定过程,滴定终点读数时俯视读数?;
②配制c mol・L-1的KMnO4标准溶液时,转移时有少量溶液洒出?。
(5)[实验探究]有同学提出FeSO4有很强的还原性,在空气中易被氧化而变质,因此对测定结果会造成影响,请你分析后指出,如果FeSO4变质,对测定结果的影响是?(填“偏高”、“偏低”或“无影响”)。
请设计一个简单实验检验FeSO4溶液是否变质?。
参考答案:(16分)
(1)Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O?(3分)
(2)溶液由浅绿色刚变浅紫色,并保持半分钟不变(2分)?酸式(1分)
(3)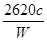 %。(2分)
%。(2分)
(4)偏低(2分)?偏高(2分)
(5)无影响(2分)取少量FeSO4溶液,向其中滴入KSCN溶液,若溶液变红,则说明FeSO4溶液已变质,反之,说明FeSO4溶液没有变质(2分)
本题解析:
(1)根据题意确定氧化还原反应中反应物、生成物并配平;
(2)由元素及化合物性质知待测液中Fe2+浅绿色,当滴定完成时MnO-4为浅紫色;盛放酸性、氧化性试剂应该选择酸式滴定管。
(3)根据题中比例关系,可知c(Na2Cr2O7)= cmol・L-1,Na2Cr2O7的质量分数为
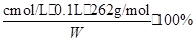 =
=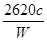 ?%。
?%。
(4)①中俯视读数会使V标(FeSO4)偏小。②中溶液洒出,会使c(FeSO4)偏大,
(5)即使FeSO4变质,用KMnO4标准溶液也可准确测出溶液中FeSO4真实浓度,故对结果无影响。
本题难度:一般
4、选择题 实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空。

(1)写出仪器名称:E?,F?
(2)下列实验操作中用到仪器G的是?(选填下列选项的编号字母)。
a.分离水和CC14的混合物?
b.分离水和酒精的混合物?
c.分离水和泥砂的混合物
(3)实验室配制100mL 0.5mol/L的盐酸溶液。
①下列关于仪器E的使用方法中,正确的是?(选填下列选项的编号字母)。
a.使用前应检查是否漏液? b.使用前必须烘干
c.不能用作物质反应或溶解的容器? d.热溶液可直接转移到容量瓶中
②需要10mol/L的浓盐酸?mL。取用该体积盐酸时,需要用到上述仪器中的A和?(选填仪器的编号字母)。
参考答案:(1)容量瓶,冷凝管(2)a?(3)① ac ?② 5(或5.0), C
本题解析:(1)根据仪器的结构特点判断仪器的名称;E为容量瓶,F为冷凝管;(2)G为分液漏斗,可用于分离互不相溶的液体混合物;选a;(3)①E为容量瓶,只能在常温下使用,且只能用来配制溶液,不能用作它途,且使用前要检查是否漏水,答案为:ac;②根据稀释定律计算所需浓盐酸的体积;0.1L×0.5mol/L=10moL/L×V,V=0.005L,即5.0mL,取用该体积盐酸时,需要用到上述仪器中的量筒和胶头滴管,其中胶头滴管用于定容,答案为:5.0;C。
本题难度:一般
5、简答题 某同学用容量瓶配制溶液,加水时不慎超过了刻度线,他把水倒出了一些,重新加水至刻度线,这种做法是否正确,如果不正确,会造成什么后果?该采取什么措置补救?
参考答案:不正确,会导致所配溶液浓度偏低,需倒掉重配
本题解析:加水时不慎超过了刻度线,他把水倒出了一些,重新加水至刻度线,这种做法是不正确的,倒出的溶液中含有一定量的溶质,相当于所配溶液中的溶质减少,而导致溶液的浓度减少;此时应重新配制;
本题难度:简单