��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��2gNaOH��������ˮ���250mL��Һ��ȡ������50mL������50mLNaOH��Һ�����ʵ���Ũ��Ϊ��������
A��0.04mol/L
B��0.2mol/L
C��1mol/L
D��2mol/L
�ο��𰸣�2gNaOH�����ʵ���Ϊ2g40g/mol=0.05mol��
������Һ��Ũ��Ϊ0.05mol0.25L=0.2mol/L��
��Һ���о�һ�ԣ���ȡ������50mL��Ũ����Ϊ0.2mol/L��
��ѡB��
���������
�����Ѷȣ���
2��ѡ���� 20��ʱ������KCl��Һ���ܶ�Ϊ1.174g/cm3�����ʵ���Ũ��Ϊ4.0mol/L��������˵���в���ȷ����
[? ]
A��25��ʱ������KCl��Һ��Ũ�ȴ���4.0mol/L
B������Һ��KCl����������Ϊ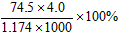
C��20��ʱ���ܶ�С��1.174g/cm3��KCl��Һ�Dz�������Һ
D��������Һ��������ˮ���ٻָ���20��ʱ����Һ�ܶ�һ������1.174g/cm3
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3������� ������500mL0.2mol/L��̼������Һ���ش��������⣺
��1��������Ҫ������______��������ƿ�ϱ��п��ߡ�______��______��
��2��ͨ�������֪��Ӧ��������ƽ��ȡ______g̼���ƣ�
��3�������IJ���˳��Ϊ������ţ�______
A������ƽ���?B���������?C����С�ձ��м���̼����?D���������ձ�?
E�������̼����벢�������Ƶ�����λ��?F��������غ�?G����¼�������
��4���������ҩƷλ�÷ŵߵ����������ʱδ���ձ�������ƽƽ��ʱ��ʵ�ʳƵ�̼���Ƶ�������______g��
��5�����в���ʹ������ҺŨ��ƫ�ߵ���______��
A����ȡ28.6gNa2CO3?10H2O��������? B������ʱ�������������
C��������ƿת����Һʱ��������Һ�彦��?D��̼�����к��в���������
E��δϴ���ܽ�̼���Ƶ��ձ�?F������ʱ�����ӿ̶���
G��С�ձ�ϴ����δ���T��������? ?H������ƿδ���T����������Һ��
�ο��𰸣���1�����������м��㡢�������ܽ⡢��Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ�������������ƽ��������ҩ��ȡҩƷ�����ձ����ܽ⣨������Ͳ��ˮ�����ò��������裬�����ܽ⣬�ָ������º�ת�Ƶ�500mL����ƿ�У����ò�����������ϴ��2-3�Σ���ϴ��Һת�Ƶ�����ƿ�У���ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�����ݵߵ�ҡ�ȣ�
����������������ƽ��500mL����ƿ���ձ�������������ͷ�ιܡ�ҩ�ȣ�
����ƿ�ϱ��п��ߡ��¶ȡ�������
�ʴ�Ϊ��������ƽ��500mL����ƿ���ձ�������������ͷ�ιܡ�ҩ�ף��¶ȣ�������
��2����̼���Ƶ����ʵ���Ϊ0.5L��0.2mol?L-1=0.1mol����̼���Ƶ�����Ϊ0.1mol��106g/mol=10.6g���ʴ�Ϊ��10.6��
��3�������IJ���˳��Ϊ��������㣬����ƽ��㣬�������ձ�����¼��������������̼����벢�������Ƶ�����λ�ã���С�ձ��м���̼���ƣ�������غУ�
�ʴ�Ϊ��BADGECF��
��4�������ҩƷλ�÷ŵߵ����������ʱδ���ձ�����ʵ�ʳƵ�̼���Ƶ�����10.0g-0.6g=9.4g���ʴ�Ϊ��9.4��
��5��A����̼���Ƶ����ʵ���Ϊ0.1mol������Na2CO3?10H2O���ƣ���ҪNa2CO3?10H2O������Ϊ0.1mol��286g/mol=28.6g����Ӱ�죬��A��ѡ��
B��������������룬�����ʵ��������������̼���Ƶ�ʵ����������������Һ��Ũ��ƫ�ߣ���Bѡ��
C��������ƿת����Һʱ��������Һ�彦������������ƿ��̼���Ƶ�ʵ��������С��������Һ��Ũ��ƫ�ͣ���C��ѡ��
D��̼�����к��в��������ʣ�������̼���Ƶ�ʵ��������С��������Һ��Ũ��ƫ�ͣ���D��ѡ��
E��δϴ���ܽ�̼���Ƶ��ձ����ձ�����մ��������̼���ƣ���������ƿ��̼���Ƶ�ʵ��������С��������Һ��Ũ��ƫ�ͣ���E��ѡ��
F������ʱ�����ӿ̶��ߣ�������Һ�����ƫ����ҺŨ��ƫ�ͣ���F��ѡ��
G��С�ձ�ϴ����δ���T����������������̼���Ƶ�ʵ��������С��������Һ��Ũ��ƫ�ͣ���G��ѡ��
H���������ˮ���ݣ�����ƿδ���T����������Һ����������ҺŨ����Ӱ�죬��H��ѡ��
��ѡB��
���������
�����Ѷȣ�һ��
4��ѡ���� ʹ��ͬ�����NaCl��MgCl2��AlCl3����Һ�е�Cl-��ȫ��������������ͬŨ��AgNO3��Һ�������Ϊ1��1��1��������������Һ�����ʵ���Ũ�ȱ��ǣ�������
A��1��2��3
B��3��2��1
C��6��3��2
D��2��3��6
�ο��𰸣���n=c?V��֪ʹ������Һ�е�Cl-��ȫ����ʱ�����ĵ�n��Ag+����ͬ������Ag++Cl-�TAgCl����֪������Һ��n��Cl-��=n��Ag+��������������Һ�������ȣ�����������Һ��c��Cl-����ȣ���c��Cl-��=c��NaCl��=12c��MgCl2��=13c��AlCl3��������c��NaCl����c��MgCl2����c��AlCl3��=6��3��2��
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ������ء���������������ɵĻ����Һ����pH=1��c(Al3+)=0.4mol/L��c(SO42-)=?0.8mol/L����c(K+)Ϊ
[? ]
A��0.15?mol/L?
B��0.2?mol/L?
C��0.3?mol/L?��?
D��0.4?mol/L
�ο��𰸣�C
���������
�����Ѷȣ���