微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于氯水说法正确的是
A.新制氯水中只含有Cl2、H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡冒出,该气体是主要是氯气
D.氯水久置后,溶液内与原来相比Cl-浓度保持不变
参考答案:B
本题解析:A、氯气和水反应生成有盐酸和次氯酸,次氯酸是弱酸,部分电离,因此新制氯水中含有Cl2、H2O和HClO分子,错误;B、氯气和水反应生成的盐酸使蓝色石蕊试纸先变红,次氯酸有漂白性,退色,正确;C、次氯酸不稳定,光照分解生成盐酸和氧气,错误;D、久置的氯水主要成分是稀盐酸,氯离子浓度增加,错误。
本题难度:一般
2、填空题 如图4-9,硬质玻璃管内,左、中、右分别放有3个湿润棉花球;a球浸有溴化钾溶液;b球浸有碘化钾浓溶液;c球中浸有KI淀粉溶液。实验时,从右端缓缓通入氯气,同时在b处微热,并逐渐向左移动酒精灯,则可以观察到:
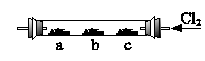 ?
?
图4-9
(1)在a处有?产生。
(2)在b处有?色产生。
(3)c处变成?色。
(4)稍冷却后,b、c之间的管壁上有?色的?。
参考答案:(1)深红棕色液体?(2)紫?气体?(3)蓝?(4)紫黑?固体
本题解析:此题巧妙地把卤素间的反应联系在一起,分析时要细心地逐一解决。涉及的反应有Cl2+2KI 2KCl+I2,Cl2+2KBr
2KCl+I2,Cl2+2KBr 2KCl+Br2,所以在b、c处有碘生成,a处有液溴生成,而碘有升华和遇淀粉变蓝的特性,所以会得上述现象。
2KCl+Br2,所以在b、c处有碘生成,a处有液溴生成,而碘有升华和遇淀粉变蓝的特性,所以会得上述现象。
本题难度:简单
3、选择题 关于水玻璃的性质和用途的叙述正确的是
A.它是一种矿物胶,既不能燃烧,也不受腐蚀
B.在建筑工业中可作黏合剂
C.木材、织物浸过水玻璃后,具有防腐性能且不易燃烧
D.水玻璃的化学性质稳定,在空气中不易变质
参考答案:AC
本题解析:水玻璃的主要成分为硅酸钠,硅酸钠是弱酸盐,易与酸性物质反应而变质。
本题难度:简单
4、填空题 Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流等等。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是 (可以多选)?
A.用pH试纸测定Na2CO3溶液的pH
B.从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
C.实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
D.配制一定物质的量浓度的氯化钠溶液
E.取某溶液做焰色反应实验,说明该溶液中含有钠元素
F.用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
G.促使过饱和的硝酸钾溶液析出晶体
Ⅱ.二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水,有刺激性气味,对人的呼吸系统有损伤,可与碱发生作用。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
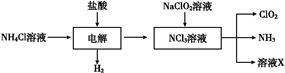
(1)写出电解时发生反应的化学方程式 ?;
(2)除去ClO2中的NH3可选用的试剂是 (填序号);
A.饱和食盐水? B.碱石灰? C.浓硫酸? D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100 mL水溶解后,再加3 mL足量硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收(假设吸收完全);将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定(I2+2S2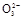
 2I-+S4
2I-+S4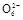 ),共用去V mL硫代硫酸钠溶液。
),共用去V mL硫代硫酸钠溶液。

①装置中玻璃液封管的作用是 ;
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式?;
③测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)。
参考答案:Ⅰ.CE
Ⅱ.(1)NH4Cl+2HCl 3H2↑+NCl3
3H2↑+NCl3
(2)C
(3)①吸收残余的二氧化氯气体,并使锥形瓶内外压强相等
②2ClO2+10I-+8H+ 4H2O+5I2+2Cl-
4H2O+5I2+2Cl-
③1.35 cV×10-2 g
本题解析:Ⅰ.A需要用玻璃棒蘸取溶液,B中需要对残留固体进行溶解、过滤、蒸发结晶,需要用玻璃棒搅拌、引流。C中用不到玻璃棒。D中配制溶液时要用玻璃棒搅拌、引流。E实验需要用铂丝,用不到玻璃棒。F用玻璃棒搅拌。G用玻璃棒摩擦烧杯壁来引发结晶。用不到玻璃棒的是C、E。
Ⅱ.(1)从流程图中可以看出电解过程中生成了H2、NCl3溶液,所以阴极上是H+得电子生成H2,阳极上是N 失去电子被氧化为NCl3,电解反应方程式:NH4Cl+2HCl
失去电子被氧化为NCl3,电解反应方程式:NH4Cl+2HCl 3H2↑+NCl3。(2)ClO2对人体有伤害作用,所以需用试剂吸收,又因ClO2及NH3都易溶于水,都能与碱作用,所以A、B、D不用选,只能用浓H2SO4吸收其中的NH3。
3H2↑+NCl3。(2)ClO2对人体有伤害作用,所以需用试剂吸收,又因ClO2及NH3都易溶于水,都能与碱作用,所以A、B、D不用选,只能用浓H2SO4吸收其中的NH3。
(3)①ClO2气体逸出会危害环境,玻璃密封管可以把逸出的少量气体吸收,同时通过水封与大气相通,保证锥形瓶内压强与大气压强相等。
②ClO2气体把还原性的I-氧化成I2。
③根据:I2+2S2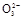
 2I-+S4
2I-+S4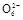 和2ClO2+10I-+8H+
和2ClO2+10I-+8H+ 4H2O+5I2+2Cl-,可以得出关系式:
4H2O+5I2+2Cl-,可以得出关系式:
2ClO2~5I2~10S2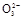 ,n(S2
,n(S2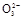 )=cV×10-3 mol,
)=cV×10-3 mol,
n(ClO2)=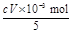 ,m(ClO2)="1.35" cV×10-2 g。
,m(ClO2)="1.35" cV×10-2 g。
本题难度:一般
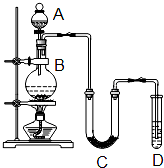
5、填空题 某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应,反应后温度将升高),A中盛浓盐酸,C中盛潮湿的消石灰,据此回答下列问题:
(1)①烧瓶B中发生反应的化学方程式______.
②在该反应中所利用的浓盐酸的性质是:______.(填符号)
a.酸性b.氧化性c.还原性d.碱性e.易挥发性
③下列有关说法正确的是______.(以下气体体积都在标状况下测定)
A.若提供0.4molHCl,MnO2不足量,则可制得氯气2.24L
B.若提供0.4molHCl,MnO2过量,则可制得氯气2.24L
C.若有0.4molHCl参加反应,可制得氯气2.24L
D.若有0.4molHCl被氧化,可制得氯气2.24L
(2)D中所盛的试剂是______,其作用是:______.
(3)漂白粉将在U型管中产生,其化学反应方程式是______.
(4)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现主要原因是在U型管C中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______.
②试判断另一个副反应是(写出此反应方程式)______.为避免此副反应发生,可采取的措施是______.
参考答案:(1)①加热条件下,二氧化锰和浓盐酸发生氧化还原反应生成氯气,反应方程式为:MnO2+4HCl(浓)△.MnCl2+2H2O+Cl2↑;
②该反应中,部分氯元素化合价升高,部分化合价不变,所以盐酸有还原性和酸性,故选ac;
③浓盐酸和二氧化锰反应生成氯气,但稀盐酸和二氧化锰不反应,且参加反应的盐酸有一半参加氧化还原反应,所以若有0.4molHCl参加反应,可制得氯气2.24L,故选C;
故答案为:MnO2+4HCl(浓)△.MnCl2+2H2O+Cl2↑;ac;C;
(2)氯气有毒不能直接排空,但氯气能和氢氧化钠反应生成无毒物质,所以D中试剂是氢氧化钠溶液,
故答案为:NaOH溶液,吸收氯气等尾气,防止污染环境;
(3)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应方程式为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,故答案为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O;
(4)①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免副反应发生,应该降低温度,所以可以采取将U型管置于冷水浴中的措施,
故答案为:将U型管置于冷水浴中;
②盐酸易挥发,加热过程中生成的氯气中含有氯化氢,氯化氢能和碱反应,所以反应方程式为:Ca(OH)2+2HCl=CaCl2+2H2O,为避免副反应发生,可以在B、C之间连接一个盛有饱和食盐水的洗气瓶,
故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;在B、C之间连接一个盛有饱和食盐水的洗气瓶.
本题解析:
本题难度:一般