微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 从含镁、钾盐湖水中蒸发最后得到产物中含光卤石(xKCl・yMgCl2・zH2O),它是制造钾肥和提取金属镁的重要原料,其组成可通过下列实验测定:
①准确称取5.550g样品溶于水,配成100.0mL溶液。
②将溶液分成二等份,在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干
燥至恒重,得到白色固体0.580g。
③在另一份溶液中加入足量的硝酸酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥
至恒重,得到白色固体4.305g。
(1)步骤②中检验白色固体已洗净的方法是:?。
(2)已知某温度下Mg(OH)2的Ksp=6.4×l0?12,当溶液中c(Mg2+)≤1.0×10?5mol・L?1可视为沉淀完全,则此温度下应保持溶液中c(OH-)≥??mol・L?1。
(3)通过计算确定样品的组成(写出计算过程)。
参考答案:
(1)取最后的洗涤液,滴加AgNO3溶液,若不产生沉淀,则已洗净(2分)。
(2)8×10―4(2分)
(3)5.550g样品中含:
n(Mg2+)=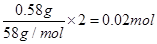 ?n(MgCl2)=0.02mol?(2分)
?n(MgCl2)=0.02mol?(2分)
n(Cl―)=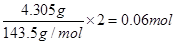 ?
?
n(KCl)=0.06mol-2×0.02mol=0.02mol?(2分)
n(H2O)=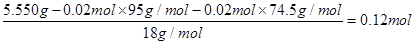
样品中n(KCl)∶n(MgCl2)∶n(H2O) =1∶1∶6
光卤石的化学式为:KCl・MgCl2・6H2O?(1分)
本题解析:(1)实验中洗涤是在过滤后在过滤器中进行,故应去最后一次的洗涤液检验:取最后的洗涤液,滴加AgNO3溶液,若不产生沉淀,则已洗净;(2)直接根据溶度积关系式计算;
(3)第一步实验计算镁离子的量
n(Mg2+)=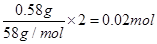 ?n(MgCl2)=0.02mol?(2分)
?n(MgCl2)=0.02mol?(2分)
第二步实验计算氯离子的量n(Cl―)= 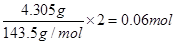 ?
?
然后根据电荷守恒计算钾离子的量,n(KCl)=0.06mol-2×0.02mol=0.02mol?
最后根据质量关系确定水的量,
n(H2O)=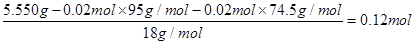
根据各物质的量的比值得出化学式。样品中n(KCl)∶n(MgCl2)∶n(H2O) =1∶1∶6
光卤石的化学式为:KCl・MgCl2・6H2O
本题难度:一般
2、选择题 下列物质中,摩尔质量最大的是 (?)
A.10 mL H2O
B.0.8 mol H2SO4
C.54 g Al
D.1g CaCO3
参考答案:D
本题解析:略
本题难度:简单
3、计算题 19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是_____________;ACl2的化学式是
_______________。
参考答案:95g/mol;MgCl2
本题解析:
本题难度:一般
4、简答题 标准状况下,22.4LHCl气体溶于50mL水后再配成250mL溶液.
(1)HCl的物质的量为______.
(2)计算所得盐酸的物质的量浓度______.
参考答案:(1)标况下,n(HCl)=22.4L22.4L/mol=1mol,故答案为:1mol;
(2)c=nV=1mol0.25L=4mol/L,故答案为:4mol/L.
本题解析:
本题难度:一般
5、选择题 配制100mL2.0mol?L-1Na0H溶液时,不需要用到的仪器是( )
A.

烧杯
B.

玻璃棒
C.

容量瓶
D.

集气瓶
参考答案:D
本题解析:
本题难度:简单