微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 在无土栽培中,配制1L内含0.25mol?NH4Cl、0.08mol?KCl、0.12molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为______、______、______.
参考答案:1L内含0.25mol?NH4Cl、0.08mol?KCl、0.12molK2SO4的某营养液中含有0.25molNH4+离子,0.32molK+离子,0.12molSO42-离子,0.33molCl-离子,
两溶液的成分不同,但含有相同的离子,
设需要KCl、NH4Cl、(NH4)2SO4的物质的量分别为x、y、z,
则有
本题解析:
本题难度:一般
2、选择题 下列物质中,摩尔质量最大的是
A.10mlH2O
B.0.8molH2SO4
C.54gAl
D.1gCaCO3
参考答案:D
本题解析:在数值上,摩尔质量等于其相对分子质量。水的摩尔质量是18g/mol,硫酸的摩尔质量是98g/mol,铝的摩尔质量是27g/mol,碳酸钙的摩尔质量是100g/mol,所以摩尔质量最大的是碳酸钙。
本题难度:简单
3、计算题 (1)(8分)恢复到室温后得到气体在标准状况下的体积
(2)(1分)恢复到室温后得到固体物质的质量(常温下水与Na2CO3会生成十水合碳酸钠)为?g
参考答案:(共10分)(1)(8分)恢复到室温后得到气体在标准状况下的体积
2NaHCO3 Na2CO3+? CO2+? H2O?(1分)
Na2CO3+? CO2+? H2O?(1分)
0.4mol? 0.2mol? 0.2mol?(1分)
2Na2O2 +2 CO2="=" Na2CO3-+O2↑?(1分)
0.2mol? 0.2mol? 0.1mol?(1分)
2Na2O2 +2H2O==4Na++4OH-+O2↑?(1分)
0.1mol? 0.1mol? 0.05mol?(1分)
n(O2)=0.1mol+0.05mol==0.15mol?(1分)
V(O2)=0.15mol×22.4L/mol=3.36L?(1分)
(2)(1分)恢复到室温后得到固体物质的质量(常温下水与Na2CO3会生成十水合碳酸钠)为?52.2?g
本题解析:恢复到室温后得到气体在标准状况下的体积
2NaHCO3 Na2CO3+? CO2+? H2O?
Na2CO3+? CO2+? H2O?
0.4mol? 0.2mol? 0.2mol?
2Na2O2 +2 CO2= Na2CO3+O2↑?
0.2mol?0.2mol? 0.1mol?
2Na2O2 +2H2O=4Na++4OH-+O2↑?
0.1mol? 0.1mol? 0.05mol?
n(O2)=0.1mol+0.05mol=0.15mol?
V(O2)=0.15mol×22.4L/mol=3.36L?
(2)恢复到室温后得到固体物质的质量(常温下水与Na2CO3会生成十水合碳酸钠)为?52.2g
本题难度:简单
4、填空题 (1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为________。
(3)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断B可能是________。
参考答案:(1)64(2)30 g/mol?(3)H2
本题解析:(1)当摩尔质量以“g/mol”为单位时,其数值与该物质的相对分子质量数值相等。在标准状况下,672mL该气体的物质的量为n="v/22.4" L/mol=0.03mol,该气体的摩尔质量为M=m/n=64g/mol,该气体的相对分子质量为64.(2)由n=m/M知,等质量的物质其物质的量与摩尔质量成反比;根据阿伏加德罗定律,同温同压下,气体的体积之比等于物质的量之比;甲烷的摩尔质量16g/mol,CH4和A气体的物质的量之比是15∶8,所以A的摩尔质量为30 g/mol;(3)标准状况下8.96L气体物质的量为8.96÷22.4=0.4molA与B物质的量比为3:1,所以A为0.3mol,B为0.1mol;设B摩尔质量为X,则A的为14X
可得:0.3×(14X)+0.1×(X)=8.6解得X=2所以A摩尔质量为28 g/mol,B摩尔质量为2 g/mol,B可能为H2。
本题难度:一般
5、选择题 物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,分别与物质的量浓度相同,体积相同的三份AgNO3溶液恰好反应,用去的三种溶液的体积比为(?)
A.1:2:3
B.6:3:2
C.3:2:1
D.1:1:1
参考答案:B
本题解析:
正确答案:B
用去的三种溶液的体积比为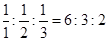
本题难度:一般