微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式正确的是( )
A.氯化亚铁溶液中通入少量氯气Fe2++Cl2=Fe3++2Cl-
B.向溴化亚铁溶液中通入过量氯气:Fe2++2Br-+2Cl2═Fe3++Br2+4Cl-
C.向碳酸氢铵溶液中加入足量的NaOH溶液:NH4++OH-=NH3?H2O
D.等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合时发生反应:HCO3-+Ba2++OH-═BaCO3↓+H2O
参考答案:A.氯化亚铁溶液中通入少量氯气的离子反应为2Fe2++Cl2=2Fe3++2Cl-,故A错误;
B.向溴化亚铁溶液中通入过量氯气的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故B错误;
C.向碳酸氢铵溶液中加入足量的NaOH溶液的离子反应为HCO3-+NH4++2OH-=NH3?H2O+CO32-,故C错误;
D.等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合时发生反应的离子反应为
HCO3-+Ba2++OH-═BaCO3↓+H2O,故D正确;
故选D.
本题解析:
本题难度:一般
2、选择题 下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是(?)
?
| (Ⅰ)
| (Ⅱ)
|
A
| 少量SO2通入Ba(OH)2溶液中
| 过量SO2通入少量Ba(OH)2溶液中
|
B
| 少量浓氨水滴入Al2(SO4)3溶液中
| 少量Al2(SO4)3溶液滴入浓氨水中
|
C
| 0.1 mol Cl2通入含0.2 mol FeBr2的溶液中
| 0.3 mol Cl2通入含0.2 mol FeBr2的溶液中
|
D
| 过量BaCl2溶液与少量Na2SO4溶液相混合
| 少量Ba(OH)2溶液与过量MgSO4溶液相混合
|
?
参考答案:B
本题解析:A项,少量SO2通入Ba(OH)2溶液中形成BaSO3沉淀;过量SO2通入少量Ba(OH)2溶液中产生酸式盐,得澄清溶液。B项,氢氧化铝不溶于氨水,所以离子方程式相同。C项,FeBr2溶液中有两种还原性的离子,所以量的不同导致离子方程式不同。D项,过量BaCl2溶液和少量Na2SO4溶液相混合产生硫酸钡沉淀,而少量Ba(OH)2溶液和过量MgSO4溶液相混合,产生硫酸钡和氢氧化镁两种白色沉淀,故离子方程式不相同。
本题难度:一般
3、选择题 下列有关离子方程式书写错误的是( )
A.将标准状况下1.12L氯气通入10mL1mol/L的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2
B.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
C.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3?H2O+H2O
D.向NaHSO3溶液中滴入适量NaClO溶液:HSO3-+ClO-=SO42-+H++Cl-
参考答案:A、标准状况下1.12L氯气n(Cl2)=1.12L22.4L/mol=0.05mol,通入10mL1mol/L的溴化亚铁溶液中n(FeBr2)=0.010L×1mol/L=0.01mol,则n(Fe2+)=0.01mol,n(Br-)=0.02mol,依据还原性顺序亚铁离子大于溴离子,2Fe2++Cl2=2Fe3++2Cl-,2Br-+Cl2=2Cl-+Br2,氧化亚铁离子需要氯气0.005mol,溴离子被氧化需要氯气0.01mol,氯气过量,亚铁离子和溴离子全部被氧化,反应的离子方程式2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2,故A正确;
B、向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液,碳酸氢钙全部反应,离子方程式中符合化学式的组成比,反应的离子方程式Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故B错误;
C、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba(OH)2和NH4HSO4按照1:1反应,反应的离子方程式Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3?H2O+H2O,故C正确;
D、向NaHSO3溶液中滴入适量NaClO溶液,次氯酸根离子具有氧化性,亚硫酸氢根离子被氧化为硫酸根离子,向NaHSO3溶液中滴入适量NaClO溶液:HSO3-+ClO-=SO42-+H++Cl-,故D正确;
故选B.
本题解析:
本题难度:一般
4、选择题 下列离子方程式书写正确的是
A.用惰性电极电解硫酸铜溶液: Cu2+ +2OH-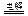 Cu↓ + H2↑+O2↑
Cu↓ + H2↑+O2↑
B.氨气通入饱和碳酸氢钠溶液中:H+ + NH3 = NH4+
C.铝溶于氢氧化钠溶液中,2Al +2OH-+2H2O=2AlO2-+3H2↑
D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br +OH-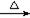 CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O
参考答案:
C
本题解析:
本题考查离子方程式的书写。用惰性电极电解硫酸铜溶液,阳极反应为:4OH--4e-=O2↑+2H2O,阴极反应为:Cu2++2e-=Cu,总反应式为:2Cu2++2H2O=2Cu+O2↑+4H+,A选项错误;氨气通入饱和碳酸氢钠溶液中发生的反应为:NH3+HCO3-=NH4++CO32-,B选项错误;溴乙烷在氢氧化钠水溶液条件下发生水解反应:C2H5Br +OH-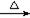 C2H5OH+Br-,D选项错误。
C2H5OH+Br-,D选项错误。
本题难度:一般
5、选择题 下列离子方程式正确的是
A.向FeCl3溶液中加入Fe粉:2Fe3++Fe=3Fe2+
B.向AlCl3溶液中滴加氨水:Al3++4OH-=AlO2-+2H2O
C.NaOH溶液中通入少量二氧化硫:SO2+2OH-=SO32-+H2O
D.用醋酸除去水垢:CaCO3 + 2H+=Ca2+ + H2O + CO2↑
参考答案:AC
本题解析:向AlCl3溶液中滴加氨水的离子反应方程式为:Al3++3NH3·H2O=AL(OH)3↓+3NH4+;
用醋酸除去水垢的离子反应方程式为:CaCO3 + 2CH3COOH=Ca2+ + 2CH3COO—+H2O + CO2↑
本题难度:一般