微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,下列叙述说明可逆反应A(g)+2B(g)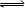
 ?2C(g) 达到平衡的(?)
?2C(g) 达到平衡的(?)
A.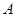 、
、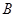 、
、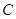 的浓度之比为1:2:2
的浓度之比为1:2:2
B.单位时间内消耗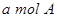 ,同时生成2a mol C
,同时生成2a mol C
C.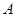 的浓度不再变化
的浓度不再变化
D.混合气体总物质的量为2a mol
参考答案:C
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,因此选项C正确。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,因此选项A不能说明。B中反应速率的方向相同,速率之比是相应的化学计量数之比,因此B中的关系始终是成立,不能说明。D中不能说明各种物质的浓度或含量不再发生变化,所以不能说明是否达到平衡状态,因此答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:简单
2、计算题 在2L的密闭容器中充入一定量的SO3,在一定温度和催化剂作用下,发生反应:2SO3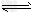 2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求:
2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求:
(1)n(SO2);
(2)氧气的生成速率v?(O2);
(3)SO3的转化率;
参考答案:(1)1.6mol
(2)v?(O2)=0.1?mol?/(L・min)
(3)20%
本题解析:
本题难度:一般
3、计算题 已知850℃时,CO(g)+H2O(g) CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
(1)当x=5.0时,判断化学反应进行的方向。
(2)若要使上述反应开始时向正反应方向进行,则x应满足的条件是什么?
(3)若x=5.0,当上述反应达到平衡后,计算H2的体积分数。
参考答案:(1)逆向进行?(2)0≥x>3?(2)0.48
本题解析:略
本题难度:一般
4、选择题 某温度下,反应N2 (g)+3H2 (g) 2NH3(g);△H <0,在密闭容器中达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(H2)/c(NH3)与原平衡相比变小了,则改变条件的可能有
2NH3(g);△H <0,在密闭容器中达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(H2)/c(NH3)与原平衡相比变小了,则改变条件的可能有
A.升高温度
B.增大N2浓度
C.减小压强
D.加入催化剂
参考答案:B
本题解析:正反应是放热反应,升高温度,平衡向逆反应方向移动,则c(H2)/c(NH3)与原平衡相比应该是变大,A不正确;增大N2浓度,平衡向正反应方向移动,则c(H2)/c(NH3)与原平衡相比应该是变小,B正确;正反应是就减小的,所以减小压强,平衡向逆反应方向移动,则c(H2)/c(NH3)与原平衡相比应该是变大,C不正确;催化剂不能改变平衡状态,比值不变,所以答案选B。
本题难度:一般
5、填空题 (18分)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:
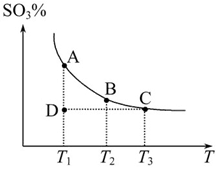
2SO2(g)+O2(g)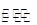 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
①2SO2(g)+O2(g)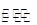 2SO3(g)的正反应为?反应(填“放热”、“吸热”);若在恒温、恒容条件下向上述平衡体系中通入氦气,平衡________移动(填“向左”、“向右”或“不”);
2SO3(g)的正反应为?反应(填“放热”、“吸热”);若在恒温、恒容条件下向上述平衡体系中通入氦气,平衡________移动(填“向左”、“向右”或“不”);
②若温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1_______K2;若反应进行到状态D时,v(正)_______v(逆)(填“>”、“<”或“=”)。
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
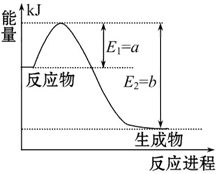
右图是一定的温度和压强下N2和H2反应生成1 mol NH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:______________。(ΔH的数值用含字母a、b的代数式表示)
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25 ℃下, 2.0×10-3 mol・L-1的NaCl溶液中逐滴加入适量的2.0×10-4? mol・L-1硝酸银溶液,?白色沉淀生成(填“有”、“没有”)。通过计算解释原因______________________________,向反应后的浊液中,继续加入2.0×10-3mol・L-1的NaI溶液,看到的现象是_____________________________,产生该现象的原因是_____________(用离子方程式表示)。(已知25 ℃时Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16)
参考答案:(1)①放热(2分)?不(2分)
②> (2分)? >(2分)
(2)N2(g)+3H2(g)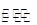 2NH3(g)?ΔH ="2(a-b)" kJ・mol-1(3分)
2NH3(g)?ΔH ="2(a-b)" kJ・mol-1(3分)
(3)有(1分)Q=c(Cl?)?c(Ag+)=1.0×10-3 ×1.0×10-4 =1.0×10-7 > Ksp,所以有沉淀生成(2分)
白色沉淀转化为黄色沉淀(2分)AgCl(s)+I-(aq)= AgI(s)+Cl-(aq)(2分)
本题解析:(1)①由图可知,温度越高,三氧化硫的含量越低,平衡向左移动,正反应放热;恒温、恒容条件下充入氦气,体积增不变,正逆反应速率不变,所以平衡不移动。
②温度越高,平衡越向左移动,平衡常数越小,故 K1>K2。状态D未达到平衡状态,要达到平衡状态,三氧化硫的含量要增大,即平衡需要向右移动,故v(正)>v(逆)。
(2)由图像可知N2和H2反应生成1 mol NH3的反应热为-(b-a) kJ・mol-1,可得热化学方程式为:N2(g)+3H2(g) 2NH3(g)? ΔH ="2(a-b)" kJ・mol-1
2NH3(g)? ΔH ="2(a-b)" kJ・mol-1
(3)通过计算比较浓度熵与Ksp的大小,Q=c(Cl?)?c(Ag+)=1.0×10-3 ×1.0×10-4 =1.0×10-7 > Ksp,所以有沉淀生成;沉淀向溶度积更小的方向转化,Ksp(AgCl)>Ksp(AgI),所以AgCl沉淀转化为更难溶的AgI,所以实验现象为白色沉淀转化为黄色沉淀;离子方程式为:AgCl(s)+I-(aq)= AgI(s)+Cl-(aq)。
本题难度:一般