��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �γ�����ЧӦ����Ҫ������
A.CO2
B.NO2
C.NO
D.SO2
�ο��𰸣�A
����������������γ�����ЧӦ��������Ҫ�Ƕ�����̼��
�������������壬������̼���γ�����ЧӦ�����壻���������ǹ⻯ѧ�����γɵ���Ҫ���壻���������������γ��������Ҫ���壬
��ѡA��
���������⿼���˳����������Ⱦ�����ʼ����Σ�
�����Ѷȣ�һ��
2��ѡ���� ���и������Ļ���ֻҪ������һ���������������ϣ���ȫȼ�պ����ɵ�CO2��H2O���Ǻ�������(? )
A��C2H2��C2H4
B��C2H4��C4H6
C��C2H6��C3H6
D��C6H6��C2H2
�ο��𰸣�D
������������Ļ�����������һ�������۰����������ϣ���ȫȼ�պ����ɵ�CO2��H2O���㶨�������ֻ����Ļ�ѧʽ�����ʽ��ͬ��A��C2H2��C2H4���ʽ����ͬ������B��C2H4��C4H6?���ʽ����ͬ������C��C2H6��C3H6���ʽ����ͬ������D��C6H6��C2H2���ʽ����CH����ͬ����ȷ��
�����Ѷȣ�һ��
3��ѡ���� ���е������������ڲⶨ�л������Է����������ǣ�
A��������
B��Ԫ�ط�����
C�����������
D���˴Ź�����
�ο��𰸣�A
���������B�DzⶨԪ��ԭ�ӵĸ���֮�ȵģ�C�Dzⶨ�����ŵģ�D�Dzⶨ��ԭ������ģ�������ȷ�Ĵ���A��
�����Ѷȣ���
4��ѡ���� 25���101kPaʱ�����顢��Ȳ�ͱ�ϩ��ɵĻ����8mL,�����������ϲ���ȫȼ�գ���ȥˮ�������ָ���ԭ�����¶Ⱥ�ѹǿ�������������С��18mL��ԭ���������Ȳ���������Ϊ(? )
A��12��5%
B��25%
C��50%
D��75%
�ο��𰸣�B
���������������ȫȼ�յĻ�ѧ����ʽΪC2H6+3��5O2=2CO2+3H2O����ȥˮ���������������С������1+3��5-2=2��5������Ȳ��ȫȼ�յĻ�ѧ����ʽΪC2H2+2��5O2=2CO2+H2O����ȥˮ���������������С������1+2��5-2=1��5������ϩ��ȫȼ�յĻ�ѧ����ʽΪC3H6+4��5O2=3CO2+3H2O����ȥˮ���������������С������1+4��5-3=2��5����������ͱ�ϩ�������С����ͬ�Ŀɿ���һ�����ʣ����������С�ǻ�������18��8=2��25��������ʮ�ֽ��淨2��5�v2��25�u0��75
1��5�u�v0��25?��������Ȳռ��������0��25/(0��25+0��75)=25%,��ѡB��
�����Ѷȣ�һ��
5��ʵ���� ��֪ij��ȼ�Ϻ���̼���⡢������Ԫ�ء�Ϊ�˲ⶨ����ȼ����̼��������Ԫ�ص������ȣ��ɽ���̬ȼ�Ϸ���������������ȼ�գ���ʹ����������ȫ��ͨ����ͼ��ʾ��װ�ã��õ����±����е�ʵ����(���������������ȫ������)��
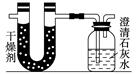
?
| ʵ��ǰ
| ʵ���
|
(�������U�ι�)������
| 101.1 g
| 102.9 g
|
(ʯ��ˮ�����ƿ)������
| 312.0 g
| 314.2 g
|
?
����ʵ��������
(1)ʵ����Ϻ���������ˮ������Ϊ________ g��
������ƿ������һ�����Σ�������Ϊ________ g��
(2)���ɵ�ˮ����Ԫ�ص�����Ϊ________ g��
(3)���ɵĶ�����̼��̼Ԫ�ص�����Ϊ________ g��
(4)��ȼ����̼Ԫ������Ԫ�ص�������Ϊ________��
(5)��֪���ִ���ÿ�������к���һ����ԭ�ӣ���ô��ķ���ʽΪ__________���ṹ��ʽΪ_______________________________��
�ο��𰸣�(1)1.8��5��(2)0.2��(3)0.6��(4)3��1
(5)CH4O��CH3OH
���������(1)m(H2O)��102.9 g��101.1 g��1.8 g
m(CO2)��314.2 g��312.0 g��2.2 g
��n(CaCO3)��n(CO2)��0.05 mol
m(CaCO3)��5 g
(2)m (H)��m(H2O)��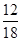 ��1.8 g��
��1.8 g��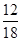 ��0.2 g
��0.2 g
(3)m(C)��m(CO2)��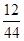 ��2.2 g��
��2.2 g��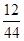 ��0.6 g
��0.6 g
(4)m(C)��m(H)��0.6 g��0.2 g��3��1
(5)��ȼ�Ϸ�����C��H��ԭ�Ӹ�����Ϊ��
N(C)��N(H)��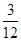 ��
�� ��1��4��
��1��4��
��̼�ļ۵�ԭ���֪�����л�������е�̼��ԭ�Ӹ�����Ϊ1��4ʱ��������ֻ�ܺ�CH4��������ΪCH4��������������Ϊÿ�������к���һ����ԭ�ӣ���ô��ķ���ʽΪCH4O���ṹ��ʽΪCH3OH��
�����Ѷȣ�һ��