��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������£�RO3n-��I-�ɷ������·�Ӧ��RO3n-+6I-+6H+=R-+3I2+3H2O����RO3n-��RԪ�صĻ��ϼ�Ϊ
A.+1
B.+3
C.+5
D.+7
�ο��𰸣�C
����������������������ӷ���ʽ�ĵ���غ��Լ����ϼ۹��������㣮
������ӷ���ʽǰ����ѭ����غ㣬����n=1�����ݻ��ϼ۹���RO3-����Ԫ�ػ��ϼ�Ϊ-2�ۣ�����RԪ�صĻ��ϼ�Ϊ+5�ۣ�
��ѡC��
���������⿼�����ӷ���ʽ�еĵ���غ��Լ����ϼ۵��йؼ���֪ʶ�����Ը�����ѧ֪ʶ���лش��ѶȲ���
�����Ѷȣ���
2��ѡ���� ��25�棬101KPa����HCHO��g����H2��CO��ɵĻ�����干6.72g��������������ܶ�Ϊ14������������2.24L��������״������ַ�Ӧ��IJ���ͨ��������Na2O2��ĩ��ʹNa2O2��ĩ���ص�����Ϊ
A.����6.72g
B.��6.72g
C.����6.72g
D.������
�ο��𰸣�B
���������������H2��CO��������Ӧ���ɶ�����̼��ˮ��������̼��ˮ��������Ʒ�Ӧ����ʹNa2O2��ĩ���أ����ݷ���ʽ��֪��������̼��������Ʒ�Ӧ����Ϊ��ʼCO��������ˮ��������Ʒ�Ӧ����Ϊ��ʼH2��������HCHO��g����������Ӧ���ɶ�����̼��ˮ��
HCHO�൱��H2��CO��1��1��ϣ���ȼ�����ɶ�����̼��ˮ������ʹNa2O2��ĩ����ΪHCHO��������
��������������ܶ�Ϊ14������������ƽ��Ħ������������������������ʵ��������ݷ���ʽ�жϻ�����Ƿ���ȫȼ�գ���HCHO��g����H2��CO��ɵĻ��������ȫȼ�գ���Na2O2��ĩ����Ϊ����������������������ȫȼ����Na2O2��ĩ����С�ڻ�������������
��𣺻����������������ܶ�Ϊ14�����Ի������ƽ��Ħ������Ϊ2g/mol��14=28g/mol��
6.72g�����������ʵ���Ϊ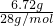 =0.24mol��
=0.24mol��
���������ʵ���Ϊ =0.1mol��
=0.1mol��
���ݷ���ʽ
2CO+O2=2CO2��
2H2+O2=2H2O��
HCHO+O2=CO2+H2O��
��֪�������ȫȼ�������������ʵ�������0.24mol�� =0.12mol��0.1mol�����Ի���ﲻ����ȫȼ�գ�Na2O2��ĩ����С�ڻ���������������С��6.72g��
=0.12mol��0.1mol�����Ի���ﲻ����ȫȼ�գ�Na2O2��ĩ����С�ڻ���������������С��6.72g��
��ѡ��B��
����������ؼ������1����HCHO��g����H2��CO��ɵĻ��������ȫȼ�գ���Na2O2��ĩ����Ϊ����������������������ȫȼ����Na2O2��ĩ����С�ڻ�������������2�����ݷ���ʽ�жϻ������ȫȼ������������
�����Ѷȣ���
3��ѡ���� ���������в������Ʒ�����Ӧ����
A.�Ҵ�
B.����
C.ˮ
D.ú��
�ο��𰸣�D
�������������������Ҵ��������ˮ�����Ʒ�Ӧ������������ú�Ͳ��ܣ���һ�㱣����ú���У���ѡD��
���㣺�����Ƶ�����
�����������ǻ���������Ŀ��飬����ע�ػ��������ضԽ��������ʵĿ��飬�����ڹ���ѧ���Ļ���֪ʶ�����ѧ��������û���֪ʶ���ʵ������������������ѶȲ���ס���ɡ�
�����Ѷȣ�����
4��ѡ���� �ڻ�ѧ��Ӧ�У���ʱ���ڡ�һ�����ʹ�������һ�������Բ�����ȫ��Ӧ������������з�Ӧ�����������������
�ٹ�����п��Ũ���ᷴӦ��?
�ڹ�����������������N2�ڹ�ҵ���������·�Ӧ��
�۹�����Ũ������̼��Ʒ�Ӧ��?
�ܹ���������������Ҵ���Ũ���ᡢ���������·�Ӧ��
�ݹ�������������Ũ�����ڼ��������·�Ӧ��?
������ͭ��Ũ�����ڼ��������·�Ӧ
A.�ڢۢܢ�
B.�ڢܢݢ�
C.�٢ڢܢ�
D.�ۢܢݢ�
�ο��𰸣�B
���������пҲ�ܺ�ϡ���ᷴӦ�������������Ԣ�������ȫ��Ӧ��ѡ��ں͢��з�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ����ȫת��Ϊ����������̼��Ƶķ�Ӧ����ȫ���У����ڶ������̲�������ϡ���ᣬ����ѡ��ݲ�����ȫ���У�ͬ��ͭ��ϡ�����Ӧ������Ҳ������ȫ���У���ѡB��
�����Ѷȣ�����
5��ѡ���� �й�Na2CO3��NaHCO3����������ȷ����
A.NaHCO3��Na2CO3���ȶ���ǿ
B.Na2CO3��NaHCO3���������ʯ��ˮ��Ӧ
C.Na2CO3��NaHCO3������NaOH��Һ��Ӧ
D.��ͬ������Na2CO3��NaHCO3�ֱ�������ϡ��������ʱ������������������ͬ
�ο��𰸣�B
���������������NaHCO3��Na2CO3��ȣ�NaHCO3�����ȶ��Բ����Ӧ����̼���Σ�NaHCO3��Na2CO3�������ᷴӦ���ɶ�����̼���壺
Na2CO3+2HCl=2NaCl+H2O+CO2����NaHCO3+HCl=NaCl+H2O+CO2�����Դ˽����⣮
���A��NaHCO3��Na2CO3��ȣ�NaHCO3�����ȶ��Բ��A����
B��Na2CO3��Ca��OH��2��Ϻ�����CaCO3������Na2CO3+Ca��OH��2=CaCO3��+2NaOH��NaHCO3�������ʯ��ˮ����Ca��OH��2+NaHCO3�TCaCO3��+NaOH+H2O��Ca��OH��2+2NaHCO3�TCaCO3��+Na2CO3+2H2O����B��ȷ��
C��Na2CO3��NaOH����Ӧ����C����
D��NaHCO3��Na2CO3�������ᷴӦ���ɶ�����̼���壺Na2CO3+2HCl=2NaCl+H2O+CO2����NaHCO3+HCl=NaCl+H2O+CO2���������ʵ�����Na2CO3��NaHCO3�ֱ���������ᷴӦ���ų�CO2������ȣ�NaHCO3��Na2CO3�������ʱ�����ʵ�������ȣ�����ͬ��ͬѹ�£����ɵ�CO2�����һ������D����
��ѡB��
���������⿼��Na2CO3��NaHCO3���ʵ���ͬ����Ŀ�ѶȲ���ע�����Na2CO3��NaHCO3���ʣ��״���ΪB��C��ע�����ֶ������ķ�Ӧ��
�����Ѷȣ�����