微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:C(s)+H2O(g)=CO(g)+H2(g)?△H=a kJ/mol
2C(s)+O2(g)=2CO(g)?△H=-220 kJ/mol
H-H、O=O和O-H键的键能分别为436、496和462 kJ/mol,则a为
A.-332
B.-118
C.+350
D.+130
参考答案:D
本题解析:已知热化学方程式①C(s)+H2O(g)=CO(g)+H2(g)?△H="a" kJ/mol,②2C(s)+O2(g)="2CO(g)" △H=-220kJ/mol,则根据盖斯定律可知②-①×2即得到热化学方程式O2(g)+2H2(g)=2H2O(g)?△H=-(220+2a)kJ/mol。由于反应热等于断键吸收的能量与形成新化学键所放出的能量的差值,则496 kJ/mol+2×436 kJ/mol-2×2×462 kJ/mol=-(220+2a)kJ/mol,解得a=+130,答案选D。
本题难度:一般
2、选择题 下列推论正确的是( )
A.S(g)+O2(g)=SO2(g)△H=a;S(s)+O2(g)=SO2(g)△H=b;则a>b
B.C(石墨,s)=C(金刚石,s);△H=+1.9kJ/mol,则可判定金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol,则含20gNaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7kJ
D.CaCO3(s)=CaO(s)+CO2(g)△H>0,则该反应任何温度下都能自发进行
参考答案:A.S(s)→S(g)为吸热过程,S的燃烧为放热过程,△H<0,固体硫燃烧放出的热量较少,则a<b,故A错误;
B.由热化学方程式可知,石墨总能量小于金刚石,则石墨较稳定,故B错误;
C.n(NaOH)=0.5mol,放出的热量为0.5mol×57.4kJ/mol=28.7kJ,故C正确;
D.CaCO3(s)=CaO(s)+CO2(g)△H>0,△S>0,由△G=△H-T?△S可知,当在较高温度下反应才能自发进行,故D错误.
故选C.
本题解析:
本题难度:一般
3、选择题 某反应的△H=+100kJ/mol,下列有关该反应的叙述正确的是
[? ]
A.正反应活化能小于100kJ/mol
B.逆反应活化能一定小于100kJ/mol
C.正反应活化能不小于100kJ/mol
D.逆反应活化能比正反应活化能大100kJ/mol
参考答案:C
本题解析:
本题难度:简单
4、简答题 298K、101 kPa时,合成氨反应的热化学方程式为N2 (g) +3H2 ( g) 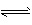 2NH3 (g) △H = - 92. 38 kJ・mol-1。在该温度下,取1 mol N2(g)和3mol H2 (g)放在一密闭容器中,在催化剂存在的情况下进行反应,测得反应放出的热量总是小于92. 38 kJ,其原因是什么?
2NH3 (g) △H = - 92. 38 kJ・mol-1。在该温度下,取1 mol N2(g)和3mol H2 (g)放在一密闭容器中,在催化剂存在的情况下进行反应,测得反应放出的热量总是小于92. 38 kJ,其原因是什么?
参考答案:该反应是可逆反应,1 mol N2(g)和3 mol H2(g)不能完全反应生成2 mol NH3 (g),因而放出的热量总小于 92.38 kJ。
本题解析:
本题难度:一般
5、选择题 强酸与强碱的稀溶液发生中和反应的热化学方程式为:
H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ・mol-1。向3份同体积0.2 mol/L的NaOH溶液中分别加入适量的下列物质:①稀醋酸:②浓硫酸;③稀硝酸,恰好完全反应时的热效应分别为△H1、△H2、△H3的关系正确的是
[? ]
A.△H1>△H2>△H3
B.△H2>△H3>△H1
C.△H2>△H1>△H3
D.△H1>△H3>△H2
参考答案:D
本题解析:
本题难度:一般